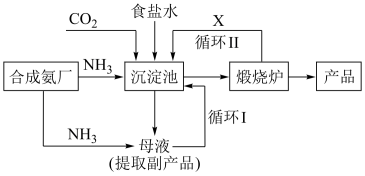
我国化学家侯德榜发明了联合制碱法,对世界制碱工业做出了巨大贡献。联合制碱法的主要过程如图所示,沉淀池反应 NaCl+CO2+NH3+H2O= NaHCO3↓+NH4Cl
(1)“侯氏制碱法”誉满全球,其中的“碱”为___________ (填化学式),俗称___________ 。
(2)沉淀反应中涉及的物质属于强电解质的为___________ (填化学式)
(3)实验室模拟“侯氏制法”,下列操作未涉及的是___________ 。
(4)煅烧炉中发生反应的化学方程式为___________ 。
(5)使用原料氯化钠的利用率从70%提高到90%以上,主要是设计了___________ (填“循环Ⅰ”或“循环Ⅱ”),流程中物质X为___________ (填化学式)。
(6)简单的检验方案的一般叙述过程为:①取试样,②加检验试剂,③现象,④结论。为验证产品纯碱中含有杂质NaCl,简单的检验方案是:取少量试样溶于水后,___________ 。

(1)“侯氏制碱法”誉满全球,其中的“碱”为
(2)沉淀反应中涉及的物质属于强电解质的为
(3)实验室模拟“侯氏制法”,下列操作未涉及的是___________ 。
A.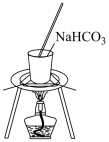 | B. |
C.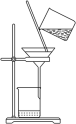 | D.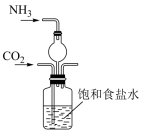 |
(5)使用原料氯化钠的利用率从70%提高到90%以上,主要是设计了
(6)简单的检验方案的一般叙述过程为:①取试样,②加检验试剂,③现象,④结论。为验证产品纯碱中含有杂质NaCl,简单的检验方案是:取少量试样溶于水后,
更新时间:2022-02-18 22:08:43
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
【推荐1】某同学设计如图实验方案分离KCl和BaCl2两种固体混合物:
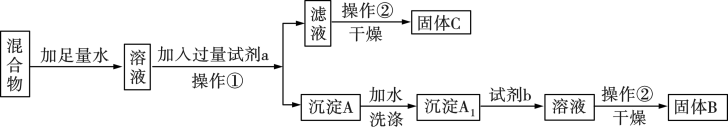
供选择的试剂:Na2SO4溶液、K2CO3溶液、K2SO4溶液、稀盐酸。
回答下列问题:
(1)操作①的名称是____ ,操作②的名称是____ 。
(2)试剂a是____ (填化学式,下同),试剂b是____ 。
(3)判断沉淀A已经洗涤干净的方法及现象是____ 。
(4)加入试剂b所发生反应的化学方程式为____ 。
(5)有同学认为该方案不能达到实验目的,改进的方法是____ 。
(6)若要测定原混合物中BaCl2的质量分数,除了要准确称量混合物的质量外,至少还要获得的数据是____ (填“A1”、“A”、“B”或“C”)的质量。

供选择的试剂:Na2SO4溶液、K2CO3溶液、K2SO4溶液、稀盐酸。
回答下列问题:
(1)操作①的名称是
(2)试剂a是
(3)判断沉淀A已经洗涤干净的方法及现象是
(4)加入试剂b所发生反应的化学方程式为
(5)有同学认为该方案不能达到实验目的,改进的方法是
(6)若要测定原混合物中BaCl2的质量分数,除了要准确称量混合物的质量外,至少还要获得的数据是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】已知某废水试样中可能含有下表中的某些离子:
现将废水试样分成甲、乙、丙、丁四份,进行如图所示的探究实验。
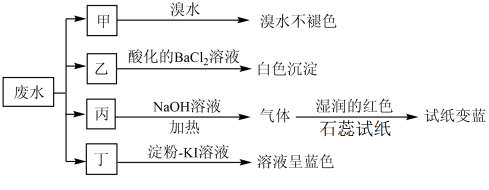
请回答下列问题:
(1)离子X为___________ (填化学式,下同),离子Y为___________ 。
(2)表中不能确定是否存在的阴离子是___________ ,能证明该阴离子存在的简单实验操作为___________ 。
(3)写出向废水试样中滴加淀粉-KI溶液所发生反应的离子方程式___________ 。
| 阳离子 |  |
| 阴离子 |  |

请回答下列问题:
(1)离子X为
(2)表中不能确定是否存在的阴离子是
(3)写出向废水试样中滴加淀粉-KI溶液所发生反应的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】某无色透明溶液中可能大量存在Ag+、Mg2+、Cu2+、Fe3+、Na+中的几种。请填写下列空白:
(1)不做任何实验就可以肯定原溶液中不存在 的离子是______ 。
(2)取少量原溶液,加入过量稀盐酸,有白色沉淀生成。说明原溶液中,肯定存在的离子是______ ,有关离子方程式为______ 。
(3)取(2)中的滤液,加入过量的NaOH,出现白色沉淀,说明原溶液中肯定有______ ,有关的离子方程式为______ 。
(4)原溶液可能大量存在的阴离子是下列的______(填选项)。
(1)不做任何实验就可以肯定原溶液中
(2)取少量原溶液,加入过量稀盐酸,有白色沉淀生成。说明原溶液中,肯定存在的离子是
(3)取(2)中的滤液,加入过量的NaOH,出现白色沉淀,说明原溶液中肯定有
(4)原溶液可能大量存在的阴离子是下列的______(填选项)。
A. | B. | C. | D. |
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】我国化学家侯德榜发明了联合制碱法,对世界制碱工业做出了巨大贡献。联合制碱法的主要过程如图所示,沉淀池反应NaCl+CO2+NH3+H2O NaHCO3↓+NH4Cl。
NaHCO3↓+NH4Cl。
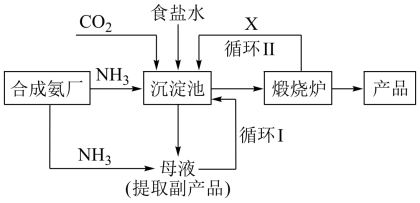
(1)“侯氏制碱法”誉满全球,其中的“碱”为________ (填化学式),俗称________ 。
(2)实验室模拟“侯氏制碱法”,下列操作未涉及的是___________。
(3)煅烧炉中发生反应的化学方程式为___________ 。
(4)简单的检验方案的一般叙述过程为:①取试样,②加检验试剂,③现象,④结论。为验证产品纯碱中含有杂质NaCl,简单的检验方案是:取少量试样溶于水后,___________ 。
(5)用Na2CO3固体配制100mL0.200mol•L﹣1Na2CO3溶液。
①用到的仪器有:天平、药匙、量筒、烧杯、玻璃棒、胶头滴管和___________ 。
②下列情况中,会使所配溶液浓度偏高的是___________ 。(填字母)
a.转移时,没有洗涤烧杯和玻璃棒
b.定容时,眼睛俯视刻度线
c.摇匀后,发现液面低于刻度线,继续加水至液面与刻度线相切
(6)探究Na2CO3与盐酸的反应。向0.200mol•L﹣1Na2CO3溶液中滴加稀盐酸,开始无气泡,继续滴加,产生气泡,反应的离子方程式为: +H+═
+H+═ 、
、___________ 。
 NaHCO3↓+NH4Cl。
NaHCO3↓+NH4Cl。
(1)“侯氏制碱法”誉满全球,其中的“碱”为
(2)实验室模拟“侯氏制碱法”,下列操作未涉及的是___________。
A. | B. |
C. | D.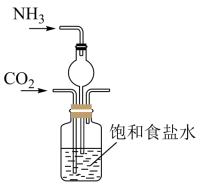 |
(4)简单的检验方案的一般叙述过程为:①取试样,②加检验试剂,③现象,④结论。为验证产品纯碱中含有杂质NaCl,简单的检验方案是:取少量试样溶于水后,
(5)用Na2CO3固体配制100mL0.200mol•L﹣1Na2CO3溶液。
①用到的仪器有:天平、药匙、量筒、烧杯、玻璃棒、胶头滴管和
②下列情况中,会使所配溶液浓度偏高的是
a.转移时,没有洗涤烧杯和玻璃棒
b.定容时,眼睛俯视刻度线
c.摇匀后,发现液面低于刻度线,继续加水至液面与刻度线相切
(6)探究Na2CO3与盐酸的反应。向0.200mol•L﹣1Na2CO3溶液中滴加稀盐酸,开始无气泡,继续滴加,产生气泡,反应的离子方程式为:
 +H+═
+H+═ 、
、
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】“侯氏制碱法”促进了我国纯碱工业的发展。某化学兴趣小组在实验室中模拟并改进侯氏制碱法用碳酸氢铵(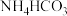 )和氯化钠为主要原料制备碳酸钠的实验流程如图。
)和氯化钠为主要原料制备碳酸钠的实验流程如图。

回答下列问题:
(1)“加热搅拌”中发生反应的化学方程式是___________ ,该反应属于___________ (填基本反应类型)。
(2)“300℃加热”需用到的仪器除酒精灯、坩埚、坩埚钳、泥三角、三角架外,还有___________ 。
(3)除去 溶液中混有的少量
溶液中混有的少量 的最佳方法是
的最佳方法是___________ ,化学方程式为___________ 。
(4)检验 中阳离子的实验方法是
中阳离子的实验方法是___________ 。
(5)现将 和
和 的固体均匀混合物等分成两份。第一份充分加热至恒重,固体质量减少6.2g;第二份与足量稀盐酸充分反应后,加热、蒸干、灼烧,得到固体23.4g。则混合物中
的固体均匀混合物等分成两份。第一份充分加热至恒重,固体质量减少6.2g;第二份与足量稀盐酸充分反应后,加热、蒸干、灼烧,得到固体23.4g。则混合物中 和
和 的物质的量之比为
的物质的量之比为___________ 。
(6)若将 和
和 的固体混合物溶于水,向溶液中加入盐酸,所加盐酸的体积与产生
的固体混合物溶于水,向溶液中加入盐酸,所加盐酸的体积与产生 的体积关系如图所示,则线段)
的体积关系如图所示,则线段)
___________ 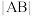 (填“>”“<”或“=”),OA段发生反应的离子方程式为
(填“>”“<”或“=”),OA段发生反应的离子方程式为___________ 。

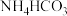 )和氯化钠为主要原料制备碳酸钠的实验流程如图。
)和氯化钠为主要原料制备碳酸钠的实验流程如图。
回答下列问题:
(1)“加热搅拌”中发生反应的化学方程式是
(2)“300℃加热”需用到的仪器除酒精灯、坩埚、坩埚钳、泥三角、三角架外,还有
(3)除去
 溶液中混有的少量
溶液中混有的少量 的最佳方法是
的最佳方法是(4)检验
 中阳离子的实验方法是
中阳离子的实验方法是(5)现将
 和
和 的固体均匀混合物等分成两份。第一份充分加热至恒重,固体质量减少6.2g;第二份与足量稀盐酸充分反应后,加热、蒸干、灼烧,得到固体23.4g。则混合物中
的固体均匀混合物等分成两份。第一份充分加热至恒重,固体质量减少6.2g;第二份与足量稀盐酸充分反应后,加热、蒸干、灼烧,得到固体23.4g。则混合物中 和
和 的物质的量之比为
的物质的量之比为(6)若将
 和
和 的固体混合物溶于水,向溶液中加入盐酸,所加盐酸的体积与产生
的固体混合物溶于水,向溶液中加入盐酸,所加盐酸的体积与产生 的体积关系如图所示,则线段)
的体积关系如图所示,则线段)
 (填“>”“<”或“=”),OA段发生反应的离子方程式为
(填“>”“<”或“=”),OA段发生反应的离子方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】某校化学课外小组为了鉴别碳酸钠和碳酸氢钠两种白色固体,用不同的方法做了以下实验,具体情况如图所示。

(1)根据图Ⅰ、Ⅱ所示实验,能够达到实验目的的是_______ (填序号)
(2)图Ⅲ、Ⅳ所示实验均能鉴别这两种物质,其反应的化学方程式为_______ 。
(3)若用实验Ⅳ确定碳酸钠和碳酸氢钠的稳定性,则试管B中装入的固体最好是_______ (填化学式)。
(4)将碳酸氢钠溶液与过量澄清石灰水反应时的离子方程式为_______ 。
(5)下列实验方案中,能测定出 和
和 混合物中物质的质量分数的是_______。
混合物中物质的质量分数的是_______。

(1)根据图Ⅰ、Ⅱ所示实验,能够达到实验目的的是
(2)图Ⅲ、Ⅳ所示实验均能鉴别这两种物质,其反应的化学方程式为
(3)若用实验Ⅳ确定碳酸钠和碳酸氢钠的稳定性,则试管B中装入的固体最好是
(4)将碳酸氢钠溶液与过量澄清石灰水反应时的离子方程式为
(5)下列实验方案中,能测定出
 和
和 混合物中物质的质量分数的是_______。
混合物中物质的质量分数的是_______。| A.取m克混合物充分加热,质量减少n克 |
B.取m克混合物与足量 溶液充分反应,得到n克溶液 溶液充分反应,得到n克溶液 |
| C.取m克混合物与足量稀盐酸反应,加热、蒸干、灼烧,得到n克固体 |
| D.取m克混合物与足量稀硫酸反应,逸出气体经充分干燥后用碱石灰吸收,质量增加n克 |
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】现有①铁片②NaNO3③NH3·H2O ④FeCl3⑤酒精⑥H2S其中属于电解质的是(填写序号)____________ ,属于非电解质的是_______ ,属于强电解质的是_____________ ,属于弱电解质的是____________ 。写出其中可发生水解的物质的水解离子方程式__________ 。
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】
(1)下面所列物质中,属于强电解质的是________ (填序号,下同),属于弱电解质的是________ ,属于非电解质的是________ 。
①硝酸钠 ②葡萄糖 ③醋酸 ④二氧化碳 ⑤乙醇 ⑥硫化氢 ⑦硫酸氢钾 ⑧一水合氨 ⑨氯气 ⑩硫酸钡 ⑪铜
(2)在新制氯水中加入少量的KCl固体,水的电离平衡________ 移动(填“向右”、“向左”、或“不”)。
(3)已知室温下,H2CO3的电离常数为Ka1=4.4×10-7;Ka2=4.7×10-11,HClO次氯酸的电离平衡常数为Ka=3.0×10-8。向0.2mol/LNa2CO3溶液中加入HClO,离子方程式为___________ ,_____ (填“能”或“不能”)观察到气泡逸出。
(4)某二元酸H2A溶液中检测出含有H+、HA-、A2-三种溶质粒子,则H2A电离方程式为_________ 。
(1)下面所列物质中,属于强电解质的是
①硝酸钠 ②葡萄糖 ③醋酸 ④二氧化碳 ⑤乙醇 ⑥硫化氢 ⑦硫酸氢钾 ⑧一水合氨 ⑨氯气 ⑩硫酸钡 ⑪铜
(2)在新制氯水中加入少量的KCl固体,水的电离平衡
(3)已知室温下,H2CO3的电离常数为Ka1=4.4×10-7;Ka2=4.7×10-11,HClO次氯酸的电离平衡常数为Ka=3.0×10-8。向0.2mol/LNa2CO3溶液中加入HClO,离子方程式为
(4)某二元酸H2A溶液中检测出含有H+、HA-、A2-三种溶质粒子,则H2A电离方程式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】(1)某次实验中将含11.2 g KOH的稀溶液与1 L 0.1 mol·L-1的H2SO4溶液充分反应共放出12.46 kJ的热量,表示该反应的中和热的热化学方程式为_______ 。
(2)下列物质:①氯化钠晶体②盐酸③氨气④NH4Cl固体⑤汞⑥熔融的KNO3 ⑦硫酸钡⑧纯醋酸,其中能导电的是______ 属于强电解质的是_______ 属于非电解质的是_______ 。
(3)已知H2O2为一种二元弱酸,写出其第二步电离的电离方程式________ 。
(4)某溶液中,c(H+)=10-amol/L,c(OH-)=10-bmol/L,a+b=13,则此时温度T____ 25℃。(填“>”、“<”或“=”),若a>b,则该溶液可以是通过给纯水中加入下列哪些物质或操作来实现____
A.稀硫酸 B.金属钠 C.将纯水加热煮沸 D. 氨气
(2)下列物质:①氯化钠晶体②盐酸③氨气④NH4Cl固体⑤汞⑥熔融的KNO3 ⑦硫酸钡⑧纯醋酸,其中能导电的是
(3)已知H2O2为一种二元弱酸,写出其第二步电离的电离方程式
(4)某溶液中,c(H+)=10-amol/L,c(OH-)=10-bmol/L,a+b=13,则此时温度T
A.稀硫酸 B.金属钠 C.将纯水加热煮沸 D. 氨气
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】皮革工业污泥中含较多的Cr,工业采用以下工艺制得M:Cr(OH)(H2O)5SO4。

已知:①工艺中硫酸浸取液中的金属离子主要是Cr3+,其次是Fe3+、Al3+、Mg2+。
②常温下部分阳离子以氢氧化物沉淀形式存在时溶液的pH见表:
(1)酸浸时,为了提高浸取效率可采取的措施是_____ (任写一条)。
(2)调节pH所用X可以选用_____ 。pH调节的范围是____ 。
A.NaOH B.Na2CO3 C.H2SO4 D.HNO3
(3)调滤液至pH=8,Al3+和Mg2+中的_____ 将转化为沉淀。此时pH不宜调节至12以上,否则会造成部分沉淀溶解,写出沉淀溶解的离子方程式_____ 。
(4)加入H2O2目的是把Cr(OH)3沉淀转化为Cr2O ,写出该反应的离子方程式
,写出该反应的离子方程式_____ 。

已知:①工艺中硫酸浸取液中的金属离子主要是Cr3+,其次是Fe3+、Al3+、Mg2+。
②常温下部分阳离子以氢氧化物沉淀形式存在时溶液的pH见表:
| 阳离子 | Fe3+ | Al3+ | Mg2+ | Cr3+ |
| 开始沉淀时的pH | 1.9 | 4.0 | 9.3 | --- |
| 沉淀完全时的pH | 3.2 | 5.3 | 11.1 | 9(>9溶解) |
(1)酸浸时,为了提高浸取效率可采取的措施是
(2)调节pH所用X可以选用
A.NaOH B.Na2CO3 C.H2SO4 D.HNO3
(3)调滤液至pH=8,Al3+和Mg2+中的
(4)加入H2O2目的是把Cr(OH)3沉淀转化为Cr2O
 ,写出该反应的离子方程式
,写出该反应的离子方程式
您最近一年使用:0次
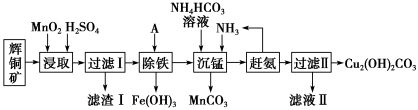
【推荐2】铜及其化合物在工业生产上有许多用途。某工厂以辉铜矿(主要成分为 Cu2S,含少量 Fe2O3、SiO2 等杂质)为原料制备不溶于水的碱式碳酸铜的流程如下:
已知:
①常温下几种物质开始形成沉淀与完全沉淀时的pH如下表
② Ksp[Fe(OH)3]=4.0×10-38
(1)加快“浸取”速率,除适当增加硫酸浓度外,还可采取的措施有__________ (任写一种)。
(2)滤渣I中的主要成分是MnO2、S、SiO2,请写出“浸取”反应中生成S的化学方程式:______________ 。
(3)常温下“除铁”时加入的试剂A可用CuO等,调节pH调的范围为_________ ,若加 A 后溶液的 pH调为4.0,则溶液中 Fe3+的浓度为_________ mol/L。
(4)写出“沉锰”(除 Mn2+)过程中反应的离子方程式:_________________________ 。
(5)“赶氨”时,最适宜的操作方法是________________ 。
(6)过滤Ⅱ得到的沉淀经过洗涤、干燥可以得到碱式碳酸铜,判断沉淀是否洗净的操作是________________ 。

已知:
①常温下几种物质开始形成沉淀与完全沉淀时的pH如下表
| 金属离子 | Fe2+ | Fe3+ | Cu2+ | Mn2+ |
| 开始沉淀 | 7.5 | 2.7 | 5.6 | 8.3 |
| 完全沉淀 | 9.0 | 3.7 | 6.7 | 9.8 |
② Ksp[Fe(OH)3]=4.0×10-38
(1)加快“浸取”速率,除适当增加硫酸浓度外,还可采取的措施有
(2)滤渣I中的主要成分是MnO2、S、SiO2,请写出“浸取”反应中生成S的化学方程式:
(3)常温下“除铁”时加入的试剂A可用CuO等,调节pH调的范围为
(4)写出“沉锰”(除 Mn2+)过程中反应的离子方程式:
(5)“赶氨”时,最适宜的操作方法是
(6)过滤Ⅱ得到的沉淀经过洗涤、干燥可以得到碱式碳酸铜,判断沉淀是否洗净的操作是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】实验室里需要纯净的氯化钠溶液,但身边只有有杂质硫酸钠、碳酸氢铵的氯化钠固体。
某学生设计了提纯方案如下图:

如若该方案可行,请回答下列问题:
(1)操作①中加热固体时,所用到的玻璃和陶瓷仪器有:酒精灯、玻璃棒、________ (填名称);此时发生的化学方程式为_________________ 。
(2)操作②反应的试剂能否改用硝酸钡溶液?__________ (填“能”或“不能”),理由是__________ 。
(3)操作②发生反应的离子方程式为__________________ 。
(4)操作③的目的是_______________ ;操作④的名称是____________ 。
(5)操作⑤的目的是______________________________ ;
要从制得的纯净氯化钠溶液获得氯化钠晶体,可采用的方法是:________________ 。
某学生设计了提纯方案如下图:

如若该方案可行,请回答下列问题:
(1)操作①中加热固体时,所用到的玻璃和陶瓷仪器有:酒精灯、玻璃棒、
(2)操作②反应的试剂能否改用硝酸钡溶液?
(3)操作②发生反应的离子方程式为
(4)操作③的目的是
(5)操作⑤的目的是
要从制得的纯净氯化钠溶液获得氯化钠晶体,可采用的方法是:
您最近一年使用:0次



