某化学兴趣小组为探究 的性质,按下图所示装置进行实验。
的性质,按下图所示装置进行实验。
请回答下列问题:
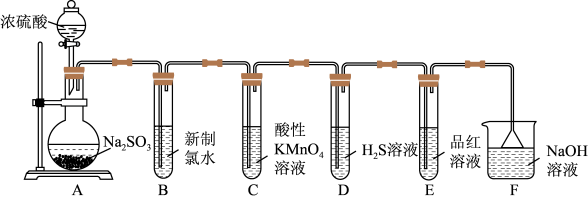
(1)装置A中盛放浓硫酸和亚硫酸钠的仪器名称分别是_______ 、_______ 。
(2)反应后,装置B中发生的现象是_______ ,反应的离子方程式为_______ ;装置C中的现象是_______ ,表现了 的
的_______ ;装置D中现象是_______ ,发生反应的化学方程式为_______ 。
(3)装置E的目的是探究 与品红溶液作用的可逆性,请写出实验操作及现象:
与品红溶液作用的可逆性,请写出实验操作及现象:_______ 。
(4)F装置的作用是_______ ,漏斗的作用是_______ 。
 的性质,按下图所示装置进行实验。
的性质,按下图所示装置进行实验。
请回答下列问题:
(1)装置A中盛放浓硫酸和亚硫酸钠的仪器名称分别是
(2)反应后,装置B中发生的现象是
 的
的(3)装置E的目的是探究
 与品红溶液作用的可逆性,请写出实验操作及现象:
与品红溶液作用的可逆性,请写出实验操作及现象:(4)F装置的作用是
2017高一·全国·课时练习 查看更多[15]
(已下线)4.3.1 硫及其氧化物高中化学人教版 必修1 第四章 非金属及其化合物 3.硫和氮的氧化物 二氧化硫和三氧化硫陕西省汉中市汉台中学、西乡中学2017-2018学年高一上学期期末联考化学试题2018年高一化学(人教版)必修1综合题型练习卷:非金属及其化合物(已下线)2018年11月27日 《每日一题》人教必修1-二氧化硫和三氧化硫、二氧化碳的性质与比较(已下线)2019年12月1日《每日一题》人教版(必修1)—— 每周一测云南省贡山县第三中学2017-2018学年高一上学期期末考试化学试题(已下线)练习9 硫和二氧化硫-2020-2021学年【补习教材·寒假作业】高一化学(人教版2019)四川省遂宁市射洪中学2020—2021学年高一下学期第一次月考化学试题安徽省淮北市树人高级中学2020-2021学年高一下学期期中考试化学试题(已下线)4.1.1 二氧化硫的性质和应用(备作业)-【上好课】2021-2022学年高一化学同步备课系列(苏教版2019必修第一册)山西省太原师范学院附属中学、太原市师苑中学校2021-2022学年高一下学期3月月考化学试题云南省昆明光华学校2021-2022学年高一3月月考化学试题广西桂林市第十九中学2021-2022学年高一下学期期中考试化学试题安徽省宿州市第二中学2022-2023学年高一上学期第一次月考化学试题
更新时间:2022-03-25 10:33:20
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
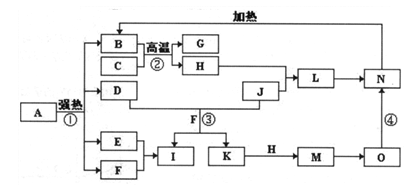
【推荐1】下图中,A为FeSO4 • 7H2O, B、D、E、F、G是氧化物,F、K是氢化物,C、H是日常生活中最常见的金属单质,J是黄绿色气态非金属单质。M与氨水反应生成的0是白色沉淀,且B、H、L、M、N、0中含有同种元素,I的产量是衡量一个国家化工生产水平的重要标志(图中部分反应物和生成物没有列出)。
请按要求回答:
(1)写出G、L的化学式G:_________ ,L:_____________ 。
(2)反应②的化学方程式________________ 。
(3)反应③的离子方程式_________________ 。
(4)反应①是分解反应,反应中生成的B、D、E、F的物质的量之比为1 : 1 : 1 : 14,则该反应的化学方程式为____________ 。
(5)由L的饱和溶液可以制得胶体,胶体中粒子直径的大小范围是________ 。若要提纯该胶体,采用的方法叫__________ 。

请按要求回答:
(1)写出G、L的化学式G:
(2)反应②的化学方程式
(3)反应③的离子方程式
(4)反应①是分解反应,反应中生成的B、D、E、F的物质的量之比为1 : 1 : 1 : 14,则该反应的化学方程式为
(5)由L的饱和溶液可以制得胶体,胶体中粒子直径的大小范围是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】某小组用如下装置制备并探索 的性质:
的性质:

(1)能体现 与水反应生成酸性物质的实验现象是
与水反应生成酸性物质的实验现象是___________ 。
(2)②中观察到淡黄色固体生成,说明 具有
具有___________ (填“氧化”或“还原”)性。
(3)③中观察到蓝色褪去, 发生反应的离子方程式为
发生反应的离子方程式为___________ 。
(4)蘸有 溶液的棉花的作用是
溶液的棉花的作用是___________ ,用离子方程式表示为___________ ( 过量)。
过量)。
 的性质:
的性质:
(1)能体现
 与水反应生成酸性物质的实验现象是
与水反应生成酸性物质的实验现象是(2)②中观察到淡黄色固体生成,说明
 具有
具有(3)③中观察到蓝色褪去,
 发生反应的离子方程式为
发生反应的离子方程式为(4)蘸有
 溶液的棉花的作用是
溶液的棉花的作用是 过量)。
过量)。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】运用化学反应原理研究硫单质及其化合物的反应,对生产、生活、环境保护等领域有着重要的意义。
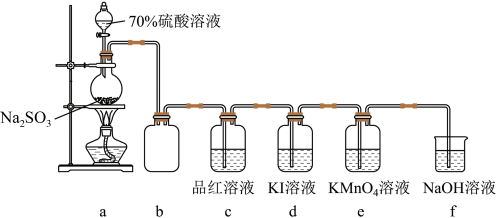
学习小组在实验室中利用如图所示装置制备SO2并进行相关性质的探究。
回答下列问题:
(1)实验用70%的硫酸而不用浓硫酸的原因是___________ 。
(2)装置e中出现___________ 填现象可证明SO2具有还原性,反应离子方程式为___________ 。
(3)实验开始后,发现装置d中的溶液迅速变黄,继续通入SO2,装置d中出现乳黄色浑浊。该小组同学查阅资料得知,存在可逆反应:SO2+4I-+4H+ S↓+2I2+2H2O。
S↓+2I2+2H2O。
探究:SO2在KI溶液体系中的反应产物
有同学提出上述可逆反应生成的I2可与SO2发生反应:SO2+I2+2H2O=SO +2I-+4H+。
+2I-+4H+。
为进一步探究体系中的产物,完成下列实验方案。
综上可知,SO2在KI溶液中发生了歧化反应,其反应的离子方程式为:___________ 。
(4)晶体碘酸钾(KIO3)是一种常用的食品添加剂,常用硫代硫酸钠滴定测定碘酸钾纯度:准确称取1.000gKIO3产品转移至200mL容量瓶中定容,精确量取20.00mL该溶液置于锥形瓶中,加入足量碘化钾,用5mL盐酸酸化(IO +5I−+6H+=3I2+3H2O),盖紧塞子,置于避光处3min,用0.1004mol/L硫代硫酸钠溶液滴定,当溶液呈淡黄色时,加入少许淀粉溶液,继续滴定至终点(I2+2S2O
+5I−+6H+=3I2+3H2O),盖紧塞子,置于避光处3min,用0.1004mol/L硫代硫酸钠溶液滴定,当溶液呈淡黄色时,加入少许淀粉溶液,继续滴定至终点(I2+2S2O =2I−+S4O
=2I−+S4O )。平行滴定三次,平均消耗0.1004mol/LNa2S2O3溶液的体积为25.00mL。
)。平行滴定三次,平均消耗0.1004mol/LNa2S2O3溶液的体积为25.00mL。
计算产品的纯度___________ 。(请写出计算过程,结果保留三位有效数字)。
学习小组在实验室中利用如图所示装置制备SO2并进行相关性质的探究。

回答下列问题:
(1)实验用70%的硫酸而不用浓硫酸的原因是
(2)装置e中出现
(3)实验开始后,发现装置d中的溶液迅速变黄,继续通入SO2,装置d中出现乳黄色浑浊。该小组同学查阅资料得知,存在可逆反应:SO2+4I-+4H+
 S↓+2I2+2H2O。
S↓+2I2+2H2O。探究:SO2在KI溶液体系中的反应产物
有同学提出上述可逆反应生成的I2可与SO2发生反应:SO2+I2+2H2O=SO
 +2I-+4H+。
+2I-+4H+。为进一步探究体系中的产物,完成下列实验方案。
| 方案 | 操作 | 预期现象 | 结论 |
| ⅰ | 取适量装置d中浊液,向其中滴加几滴① | 无明显变化 | 浊液中无I2 |
| ⅱ | 将装置d中浊液进行分离 | 得淡黄色固体和澄清溶液 | |
| 取适量分离后的澄清溶液于试管中,② | ③ | ④ |
(4)晶体碘酸钾(KIO3)是一种常用的食品添加剂,常用硫代硫酸钠滴定测定碘酸钾纯度:准确称取1.000gKIO3产品转移至200mL容量瓶中定容,精确量取20.00mL该溶液置于锥形瓶中,加入足量碘化钾,用5mL盐酸酸化(IO
 +5I−+6H+=3I2+3H2O),盖紧塞子,置于避光处3min,用0.1004mol/L硫代硫酸钠溶液滴定,当溶液呈淡黄色时,加入少许淀粉溶液,继续滴定至终点(I2+2S2O
+5I−+6H+=3I2+3H2O),盖紧塞子,置于避光处3min,用0.1004mol/L硫代硫酸钠溶液滴定,当溶液呈淡黄色时,加入少许淀粉溶液,继续滴定至终点(I2+2S2O =2I−+S4O
=2I−+S4O )。平行滴定三次,平均消耗0.1004mol/LNa2S2O3溶液的体积为25.00mL。
)。平行滴定三次,平均消耗0.1004mol/LNa2S2O3溶液的体积为25.00mL。计算产品的纯度
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】某化学实验小组的同学为探究和比较SO2和氯水的漂白性,设计了如下的实验装置。
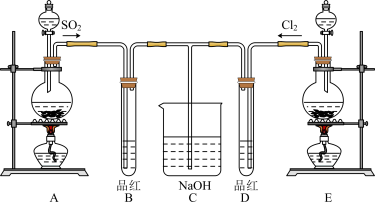
(1)实验室用装置A制备SO2。从物质类别看,SO2属于______ (填“酸性”、“两性”或“碱性”)氧化物;
(2)实验室用装置E制备Cl2,写出该反应的离子方程式:_________________________ 。反应中的液体反应物在反应中所表现出的性质为:____________ ;
(3)反应开始一段时间后,观察到B、D两个试管中的品红溶液均褪色。停止通气后,再给B、D两个试管分别加热,两个试管中的现象分别为B:_____________________ ,D:_________________ 。
(4)另一个实验小组的同学认为SO2和氯水都有漂白性,二者混合后的漂白性肯定会更强,他们将制得的SO2和Cl2按1:1同时通入到品红溶液中,结果发现褪色效果并不像想象那样。请你分析该现象的原因(用化学方程式表示)____________________________ 。
(5)有人预测SO2能使酸性高锰酸钾溶液褪色,你认为该预测是否合理?______ (填“合理”或“不合理”),理由是___________________________________________ 。

(1)实验室用装置A制备SO2。从物质类别看,SO2属于
(2)实验室用装置E制备Cl2,写出该反应的离子方程式:
(3)反应开始一段时间后,观察到B、D两个试管中的品红溶液均褪色。停止通气后,再给B、D两个试管分别加热,两个试管中的现象分别为B:
(4)另一个实验小组的同学认为SO2和氯水都有漂白性,二者混合后的漂白性肯定会更强,他们将制得的SO2和Cl2按1:1同时通入到品红溶液中,结果发现褪色效果并不像想象那样。请你分析该现象的原因(用化学方程式表示)
(5)有人预测SO2能使酸性高锰酸钾溶液褪色,你认为该预测是否合理?
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】(1)为探究黑色固体X(仅含两种元素)的组成和性质,设计并完成如下实验:
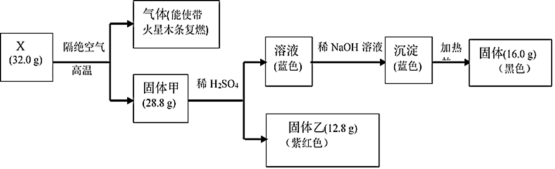
①X的化学式是___________ 。
②固体甲与稀硫酸反应的离子方程式是___________ 。
③热的氨气被固体X氧化成一种气体单质,该反应方程式___________ 。
(2)FeSO4受热分解的化学方程式为:2FeSO4 Fe2O3+SO2↑+SO3↑。
Fe2O3+SO2↑+SO3↑。
①将FeSO4受热产生的气体按图示装置进行实验,证实含有SO2和SO3,能说明SO2存在的实验现象是:___________ ;

②为测定BaSO4沉淀的质量,后续的操作步骤依次为___________ 、洗涤、干燥、称量。
③试剂一个实验方案,用化学方法验证FeSO4受热后固体的成分(不考虑其他反应):___________ 。

①X的化学式是
②固体甲与稀硫酸反应的离子方程式是
③热的氨气被固体X氧化成一种气体单质,该反应方程式
(2)FeSO4受热分解的化学方程式为:2FeSO4
 Fe2O3+SO2↑+SO3↑。
Fe2O3+SO2↑+SO3↑。①将FeSO4受热产生的气体按图示装置进行实验,证实含有SO2和SO3,能说明SO2存在的实验现象是:

②为测定BaSO4沉淀的质量,后续的操作步骤依次为
③试剂一个实验方案,用化学方法验证FeSO4受热后固体的成分(不考虑其他反应):
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】硫及其化合物对人类生存和社会发展意义重大,某实验小组设计了如图装置制备并探究二氧化硫的性质。
回答下列问题:
(1)仅器 的名称是
的名称是___________ ;导管b的作用是___________ 。
(2)装置 中反应的化学方程式为
中反应的化学方程式为___________ 。
(3)小组同学做了如下实验记录,请完成下列表格:
(4)小组同学预测装置 中没有白色沉淀产生,但随着反应的进行,装置
中没有白色沉淀产生,但随着反应的进行,装置 中出现了少量白色沉淀。该实验小组的同学通过实验验证白色沉淀为
中出现了少量白色沉淀。该实验小组的同学通过实验验证白色沉淀为 ,写出
,写出 中生成白色沉淀的化学方程式:
中生成白色沉淀的化学方程式:___________ 。

回答下列问题:
(1)仅器
 的名称是
的名称是(2)装置
 中反应的化学方程式为
中反应的化学方程式为(3)小组同学做了如下实验记录,请完成下列表格:
| 装置 | 实验现象 | 实验结论 |
| B | a. | b. |
| C | 品红溶液褪色 | c. |
| D | d. |  具有还原性 具有还原性 |
 中没有白色沉淀产生,但随着反应的进行,装置
中没有白色沉淀产生,但随着反应的进行,装置 中出现了少量白色沉淀。该实验小组的同学通过实验验证白色沉淀为
中出现了少量白色沉淀。该实验小组的同学通过实验验证白色沉淀为 ,写出
,写出 中生成白色沉淀的化学方程式:
中生成白色沉淀的化学方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】某小组设计实验探究 的还原性(部分夹持仪器省略)。
的还原性(部分夹持仪器省略)。
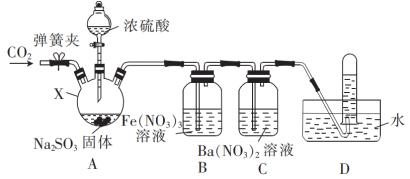
回答下列问题:
(1)分液漏斗中浓硫酸的浓度宜选择_______ (填标号)。
a.98.3% b.70% c.10%
(2)仪器X的名称是_______ ,装置A中发生反应的化学方程式为_______ 。
(3)为了探究装置B中 、
、 是否与
是否与 发生反应,设计如下实验:
发生反应,设计如下实验:
由操作Ⅰ及其现象可知
_______ (填“部分”或“全部”,下同)参与了反应,由操作Ⅱ及其现象可知
_______ 参与了反应。
(4)测定装置B溶液中 的浓度(只考虑
的浓度(只考虑 与
与 的反应)。用
的反应)。用 的酸性
的酸性 溶液滴定20mL装置B中溶液,共消耗酸性
溶液滴定20mL装置B中溶液,共消耗酸性 溶液16mL,则装置B溶液中
溶液16mL,则装置B溶液中
_______  。
。
(5)经分析,装置C中反应可能有两种情况:
①若通入少量 ,则反应为
,则反应为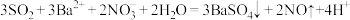 ;
;
②若通入过量 ,则反应为
,则反应为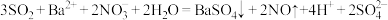 。
。
为了探究发生了哪一种情况,取装置C中溶液分别装入甲、乙、丙、丁四支试管中,进行如下实验:
能说明发生的是情况①的实验是_______ (填标号,下同),能说明发生的是情况②的实验是_______ 。
(6)设计实验验证装置D中试管收集的气体是NO:_______ 。
 的还原性(部分夹持仪器省略)。
的还原性(部分夹持仪器省略)。
回答下列问题:
(1)分液漏斗中浓硫酸的浓度宜选择
a.98.3% b.70% c.10%
(2)仪器X的名称是
(3)为了探究装置B中
 、
、 是否与
是否与 发生反应,设计如下实验:
发生反应,设计如下实验:| 实验操作 | 现象 |
| Ⅰ.取装置B中溶液于试管,滴加KSCN溶液 | 溶液不变红 |
| Ⅱ.取装置B中溶液于试管,加入适量浓硫酸,再加入铜粉 | 铜粉不溶解,溶液不变蓝 |
Ⅲ.取装置B中溶液于试管,滴加 溶液和盐酸 溶液和盐酸 | 产生白色沉淀 |


(4)测定装置B溶液中
 的浓度(只考虑
的浓度(只考虑 与
与 的反应)。用
的反应)。用 的酸性
的酸性 溶液滴定20mL装置B中溶液,共消耗酸性
溶液滴定20mL装置B中溶液,共消耗酸性 溶液16mL,则装置B溶液中
溶液16mL,则装置B溶液中
 。
。(5)经分析,装置C中反应可能有两种情况:
①若通入少量
 ,则反应为
,则反应为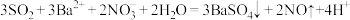 ;
;②若通入过量
 ,则反应为
,则反应为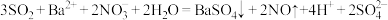 。
。为了探究发生了哪一种情况,取装置C中溶液分别装入甲、乙、丙、丁四支试管中,进行如下实验:
| 实验 | 操作及现象 |
| a | 向甲中加入锌粒,产生气泡 |
| b | 向乙中加入铜粉,溶液颜色发生了变化 |
| c | 向丙中加入 粉末,产生气泡 粉末,产生气泡 |
| d | 向丁中加入 溶液,产生沉淀 溶液,产生沉淀 |
(6)设计实验验证装置D中试管收集的气体是NO:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】MnSO4·H2O是一种易溶于水的微红色斜方晶体,实验室用SO2还原MnO2制备MnSO4。某同学设计下列装置制备硫酸锰。回答下列有关问题:

(1)装置B中试剂为___________ ,其作用是___________ ,装置C的作用___________
(2)写出装置D中发生反应的化学方程式:___________
(3)要从D中获得纯净的MnSO4·H2O,应在观察到___________ 现象时停止通入SO2。
(4)装置D中水浴温度应控制在80℃左右,温度过高时反应速率可能减慢的原因:___________ 。
(5)向含有1molNa2S的溶液中通入足量的SO2,最多消耗___________ molSO2。

(1)装置B中试剂为
(2)写出装置D中发生反应的化学方程式:
(3)要从D中获得纯净的MnSO4·H2O,应在观察到
(4)装置D中水浴温度应控制在80℃左右,温度过高时反应速率可能减慢的原因:
(5)向含有1molNa2S的溶液中通入足量的SO2,最多消耗
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】 和
和 是主要的大气污染物。某小组认为一定条件下,用
是主要的大气污染物。某小组认为一定条件下,用 与
与 反应转化为无污染物质可进行汽车尾气无害化处理。
反应转化为无污染物质可进行汽车尾气无害化处理。
(1)氨气的制备
①实验室制氨气的化学方程式为___________ 。
②制备和收集纯净、干燥的氨气,可以选择下图装置___________ (填字母),C中试剂为___________ 。
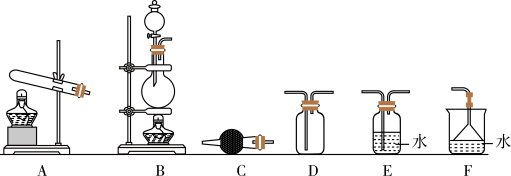
(2)氨气与二氧化氮的反应(已知: )。
)。

①在硬质玻璃管Y中加入少量催化剂,将 气体注入Y管中,Z中应盛装
气体注入Y管中,Z中应盛装___________ 。
②打开 ,将注射器X中的
,将注射器X中的 缓慢注入Y中,发生反应的化学方程式为
缓慢注入Y中,发生反应的化学方程式为___________ 。
③将注射器活塞退回原处并固定,待装置恢复到室温,打开K2,Y中出现倒吸现象,原因
是___________ 。
(3)该小组进一步研究 的性质,探究
的性质,探究 能否与
能否与 发生氧化还原反应。实验室用铜丝和浓硫酸反应生成
发生氧化还原反应。实验室用铜丝和浓硫酸反应生成 的化学方程式为
的化学方程式为___________ 。利用(2)中装置,将Y中的药品更换为少量 ,将注射器X中
,将注射器X中 缓慢推入Y中,Y装置中淡黄色粉末颜色变成白色。设计方案检验生成的白色物质中含有
缓慢推入Y中,Y装置中淡黄色粉末颜色变成白色。设计方案检验生成的白色物质中含有 ,其方案为
,其方案为___________ 。
 和
和 是主要的大气污染物。某小组认为一定条件下,用
是主要的大气污染物。某小组认为一定条件下,用 与
与 反应转化为无污染物质可进行汽车尾气无害化处理。
反应转化为无污染物质可进行汽车尾气无害化处理。(1)氨气的制备
①实验室制氨气的化学方程式为
②制备和收集纯净、干燥的氨气,可以选择下图装置

(2)氨气与二氧化氮的反应(已知:
 )。
)。
①在硬质玻璃管Y中加入少量催化剂,将
 气体注入Y管中,Z中应盛装
气体注入Y管中,Z中应盛装②打开
 ,将注射器X中的
,将注射器X中的 缓慢注入Y中,发生反应的化学方程式为
缓慢注入Y中,发生反应的化学方程式为③将注射器活塞退回原处并固定,待装置恢复到室温,打开K2,Y中出现倒吸现象,原因
是
(3)该小组进一步研究
 的性质,探究
的性质,探究 能否与
能否与 发生氧化还原反应。实验室用铜丝和浓硫酸反应生成
发生氧化还原反应。实验室用铜丝和浓硫酸反应生成 的化学方程式为
的化学方程式为 ,将注射器X中
,将注射器X中 缓慢推入Y中,Y装置中淡黄色粉末颜色变成白色。设计方案检验生成的白色物质中含有
缓慢推入Y中,Y装置中淡黄色粉末颜色变成白色。设计方案检验生成的白色物质中含有 ,其方案为
,其方案为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】某同学欲用右图装置制备乙酸乙酯,其中a试管中是浓硫酸、乙醇、乙酸的混合液, b试管盛饱和Na2CO3溶液。回答下列问题:

(1)指出装置中一个明显的错误______________________________
(2)配制浓硫酸、乙醇、乙酸的混合液的正确操作顺序是_______________________ 。
(3)写出试管a中所发生反应的化学方程式_______________ ,其反应类型为_________ 。
(4)反应结束后振荡b试管的混合液,可观察到b试管中有细小气泡冒出,写出表示该反应的离子方程式_____________ 。
(5)从b试管中分离出乙酸乙酯的分离方法是__________________ 。
(6)浓硫酸在此反应中的作用是_____________ 。

(1)指出装置中一个明显的错误
(2)配制浓硫酸、乙醇、乙酸的混合液的正确操作顺序是
(3)写出试管a中所发生反应的化学方程式
(4)反应结束后振荡b试管的混合液,可观察到b试管中有细小气泡冒出,写出表示该反应的离子方程式
(5)从b试管中分离出乙酸乙酯的分离方法是
(6)浓硫酸在此反应中的作用是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】图中为实验室制取氯气及性质验证的装置图:

回答下列问题:
(1)仪器a的名称_______ ,写出装置A中反应的化学方程式_______ 。装置F中可观察到的现象是_______ 。
(2)装置B的作用为_______ ,装置C的作用为_______ ,装置H的作用为_______ ,写出装置H的化学方程式_______ 。

回答下列问题:
(1)仪器a的名称
(2)装置B的作用为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】生活中常用一定浓度的过氧乙酸(CH3COOOH)溶液作消毒液。某化学小组对过氧乙酸的制备和性质进行如图探究(夹持、加热及搅拌装置均未画出)。
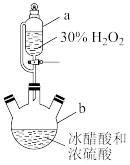
I.在磁力搅拌作用下,向仪器b中加入一定量的冰醋酸和浓硫酸,打开开关K,缓缓滴入适量30%的H2O2溶液,控制温度在20~30℃。
已知:过氧乙酸的氧化性强于高锰酸钾的。
(1)仪器b的名称为___ 。
(2)仪器a与分液漏斗相比,其优点是____ 。
(3)控制温度在20~30℃的目的是____ 。
Ⅱ.过氧乙酸样品中常含有残留的H2O2。样品中过氧乙酸的浓度为c0mol·L-1时,发生如下反应:
①CH3COOOH+2I-+2H+=CH3COOH+I2+H2O;
②H2O2+2I-+2H+=I2+2H2O;
③2S2O +I2=2I-+S4O
+I2=2I-+S4O 。
。
ⅰ.取V0mL待测液并用硫酸酸化,再用c1mol·L-1的KMnO4标准溶液滴定待测液至溶液呈粉红色,消耗V1mLKMnO4标准溶液。
ii.另取V2mL(V2≠V0)待测液,加入过量的KI溶液和几滴淀粉,并用硫酸酸化,再用c2mol·L-1的Na2S2O3标准溶液滴定,达到滴定终点时消耗V3mLNa2S2O3标准溶液。
(4)i中发生反应的离子方程式为___ 。ii中用Na2S2O3标准溶液进行滴定时,达到滴定终点的标志是___ ,过氧乙酸的浓度c0mol·L-1=___ mol·L-1(用含V0、c1、V1、c2、V2、V3的代数式表示)。

I.在磁力搅拌作用下,向仪器b中加入一定量的冰醋酸和浓硫酸,打开开关K,缓缓滴入适量30%的H2O2溶液,控制温度在20~30℃。
已知:过氧乙酸的氧化性强于高锰酸钾的。
(1)仪器b的名称为
(2)仪器a与分液漏斗相比,其优点是
(3)控制温度在20~30℃的目的是
Ⅱ.过氧乙酸样品中常含有残留的H2O2。样品中过氧乙酸的浓度为c0mol·L-1时,发生如下反应:
①CH3COOOH+2I-+2H+=CH3COOH+I2+H2O;
②H2O2+2I-+2H+=I2+2H2O;
③2S2O
 +I2=2I-+S4O
+I2=2I-+S4O 。
。ⅰ.取V0mL待测液并用硫酸酸化,再用c1mol·L-1的KMnO4标准溶液滴定待测液至溶液呈粉红色,消耗V1mLKMnO4标准溶液。
ii.另取V2mL(V2≠V0)待测液,加入过量的KI溶液和几滴淀粉,并用硫酸酸化,再用c2mol·L-1的Na2S2O3标准溶液滴定,达到滴定终点时消耗V3mLNa2S2O3标准溶液。
(4)i中发生反应的离子方程式为
您最近一年使用:0次



