氮的氧化物既是可导致酸雨的物质,也是造成空气污染的重要物质,加大对氨的氧化物的治理是环境保护重要举措。
回答下列问题:
(1)在一定条件下氨气可用来将氮氧化物转化为无污染的物质。写出氨气和二氧化氮在一定条件下反应的化学方程式:___________ ,该反应中氧化剂是___________ ,还原剂是___________ 。
(2)汽车尾气中含有CO和NO,消除这两种物质对大气的污染的方法是安装催化转化器,使它们发生反应生成对大气无污染的气体,该反应的化学方程式为___________ 。
(3)用氢氧化钠溶液可以吸收废气中的氮氧化物,反应的化学方程式如下:
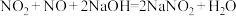
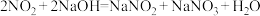
现有VL某NaOH溶液能完全吸收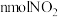 和
和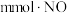 组成的大气污染物。
组成的大气污染物。
①所用烧碱溶液的物质的量浓度至少为___________  。
。
②若所得溶液中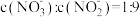 ,则原混合气体中
,则原混合气体中 和NO的物质的量之比
和NO的物质的量之比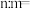
___________ 。
回答下列问题:
(1)在一定条件下氨气可用来将氮氧化物转化为无污染的物质。写出氨气和二氧化氮在一定条件下反应的化学方程式:
(2)汽车尾气中含有CO和NO,消除这两种物质对大气的污染的方法是安装催化转化器,使它们发生反应生成对大气无污染的气体,该反应的化学方程式为
(3)用氢氧化钠溶液可以吸收废气中的氮氧化物,反应的化学方程式如下:
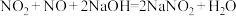
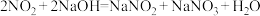
现有VL某NaOH溶液能完全吸收
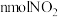 和
和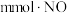 组成的大气污染物。
组成的大气污染物。①所用烧碱溶液的物质的量浓度至少为
 。
。②若所得溶液中
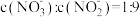 ,则原混合气体中
,则原混合气体中 和NO的物质的量之比
和NO的物质的量之比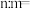
更新时间:2022-03-29 06:39:56
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】航天飞机释放出的CO2通过含有LiOH(LiOH与NaOH的化学性质相似)的滤毒罐而被除去,完成下列问题:
(1)CO2与足量LiOH反应的化学方程式为___________ ,该化学反应的类型为___________ 反应(填“复分解”,“非氧化还原”或“氧化还原”)。
(2)若有标况下4.48×104L的CO2被足量的LiOH吸收,则消耗LiOH___________ 克。(写出具体解题过程)
(1)CO2与足量LiOH反应的化学方程式为
(2)若有标况下4.48×104L的CO2被足量的LiOH吸收,则消耗LiOH
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】Ⅰ.工业生产硝酸的尾气中含有氮氧化物 (假设仅为NO和
(假设仅为NO和 的混合物),影响生态环境。
的混合物),影响生态环境。
(1)氮氧化物 对环境主要影响有两点
对环境主要影响有两点___________ 、___________ 。
Ⅱ.工业上可用氨催化吸收法处理 ,反应原理为:
,反应原理为: 某化学兴趣小组模拟该处理过程的实验装置如图:
某化学兴趣小组模拟该处理过程的实验装置如图:

(2)装置A中发生反应的化学方程式为___________ 。
(3)装置C的作用有两个:一个作用是通过气泡产生的速率来控制反应物的比例,另一个作用是___________ 。
(4)反应 可用于处理
可用于处理 。当转移3.6mol电子时,消耗
。当转移3.6mol电子时,消耗 的物质的量为
的物质的量为___________ mol。
Ⅲ.工业上也常用NaOH溶液吸收法处理 :
:


(5)2240mL(标准状况)NO和 的混合气体溶于200mLNaOH溶液中,恰好完全反应,并无气体放出,则NaOH溶液物质的量浓度是
的混合气体溶于200mLNaOH溶液中,恰好完全反应,并无气体放出,则NaOH溶液物质的量浓度是 ___________ 。
 (假设仅为NO和
(假设仅为NO和 的混合物),影响生态环境。
的混合物),影响生态环境。(1)氮氧化物
 对环境主要影响有两点
对环境主要影响有两点Ⅱ.工业上可用氨催化吸收法处理
 ,反应原理为:
,反应原理为: 某化学兴趣小组模拟该处理过程的实验装置如图:
某化学兴趣小组模拟该处理过程的实验装置如图:
(2)装置A中发生反应的化学方程式为
(3)装置C的作用有两个:一个作用是通过气泡产生的速率来控制反应物的比例,另一个作用是
(4)反应
 可用于处理
可用于处理 。当转移3.6mol电子时,消耗
。当转移3.6mol电子时,消耗 的物质的量为
的物质的量为Ⅲ.工业上也常用NaOH溶液吸收法处理
 :
:

(5)2240mL(标准状况)NO和
 的混合气体溶于200mLNaOH溶液中,恰好完全反应,并无气体放出,则NaOH溶液物质的量浓度是
的混合气体溶于200mLNaOH溶液中,恰好完全反应,并无气体放出,则NaOH溶液物质的量浓度是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】写出下列反应的化学方程式,并注明反应的基本类型。
(1)加热高锰酸钾制氧气:____ 、____ 。
(2)常温下铝与氧气反应:____ 、____ 。
(3)碳酸钠溶液与氢氧化钙溶液反应:_____ 、____ 。
(4)煤的气化是使煤变成清洁能源的有效途径,煤气化的主要反应有:①2C+O2=2CO②C+H2O=CO+H2③CO+H2O=H2+CO2。反应①的基本反应类型是____ 反应。反应②和反应③的相同点是___ (填序号)。
A.都是置换反应 B.水都发生了还原反应
C.生成物都是可燃性气体 D.反应后碳元素的化合价都升高
(1)加热高锰酸钾制氧气:
(2)常温下铝与氧气反应:
(3)碳酸钠溶液与氢氧化钙溶液反应:
(4)煤的气化是使煤变成清洁能源的有效途径,煤气化的主要反应有:①2C+O2=2CO②C+H2O=CO+H2③CO+H2O=H2+CO2。反应①的基本反应类型是
A.都是置换反应 B.水都发生了还原反应
C.生成物都是可燃性气体 D.反应后碳元素的化合价都升高
您最近一年使用:0次
【推荐2】NaNO2因外观和食盐相似,又有咸味,容易使人误食中毒。已知NaNO2能发生反应:2NaNO2+4HI=2NO↑+I2+2NaI+2H2O。
(1)上述反应中还原剂是________ 。
(2)根据上述反应,鉴别NaNO2和NaCl。可选用的物质有①水、②淀粉碘化钾试纸、③淀粉、④白酒、⑤食醋,你认为必须选用的物质有________ (填序号)。
(3)请配平以下化学方程式:□Al+□NaNO3+□NaOH=□NaAlO2+□N2↑+□H2O___ ,若反应过程中转移0.5mol电子,则生成标准状况下N2的体积为________ L。
(1)上述反应中还原剂是
(2)根据上述反应,鉴别NaNO2和NaCl。可选用的物质有①水、②淀粉碘化钾试纸、③淀粉、④白酒、⑤食醋,你认为必须选用的物质有
(3)请配平以下化学方程式:□Al+□NaNO3+□NaOH=□NaAlO2+□N2↑+□H2O
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】从物质类别和元素化合价两个维度研究物质的性质及转化是重要的化学学习方法。氯及其化合物有重要用途,以下是氯元素的“价类二维图”的部分信息。请回答下列问题:

(1)根据图中信息写出Y、Z的化学式____ 、___ 。
(2)已知高氯酸( )是强酸,常温下表现弱氧化性,写出高氯酸与铁反应的离子方程式
)是强酸,常温下表现弱氧化性,写出高氯酸与铁反应的离子方程式___ 。
(3)有一种“地康法”制取氯气的反应原理如下图所示:

①写出总反应化学方程式_______ 。
②反应II属于_______ 反应(填基本反应类型)。
(4)实验室可用二氧化锰与浓盐酸在加热条件下制得氯气。该反应中盐酸表现_______(填字母)。

(1)根据图中信息写出Y、Z的化学式
(2)已知高氯酸(
 )是强酸,常温下表现弱氧化性,写出高氯酸与铁反应的离子方程式
)是强酸,常温下表现弱氧化性,写出高氯酸与铁反应的离子方程式(3)有一种“地康法”制取氯气的反应原理如下图所示:

①写出总反应化学方程式
②反应II属于
(4)实验室可用二氧化锰与浓盐酸在加热条件下制得氯气。该反应中盐酸表现_______(填字母)。
| A.酸性 | B.氧化性 | C.还原性 | D.挥发性 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】氮的化合物研究是环境科学的热点课题之一。
金属与不同密度硝酸溶液反应时,还原产物百分比与硝酸密度的关系下图所示:
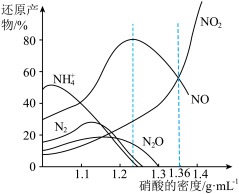
(1)当硝酸溶液的密度为1.36g.cm-3时,下列化学方程式中,能较准确表达Fe与过量硝酸反应的是(填序号)________________ 。
A.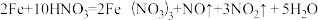
B.
C.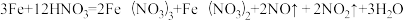
(2)现有一定量铝粉和铜粉的混合物与一定量很稀的硝酸溶液充分反应,反应过程中无气体放出。在反应结束后的溶液中,逐滴加入5mo/L的NaOH溶液,所加NaOH溶液的体积与产生沉淀的物质的量关系如下图所示:
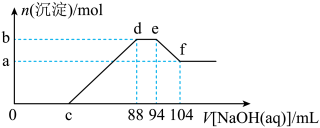
①c点对应NaOH溶液的体积为________________ mL;
②ef段发生反应的离子方程式为________________ 。
(3)研究表明硝酸与金属反应时,最容易生成亚硝酸(HNO2,弱酸),然后才转化成NO2,如果溶液中存在更强的氧化剂,如过氧化氢,它完全有能力将新产生的HNO2再氧化成HNO3,如图为金属在不同浓度的HNO3-H2O2混合溶液中的溶解速率和生成NOx的体积V的变化示意图:

①最佳溶解金属的混合溶液中HNO3的质量分数________________ 。
②H2O2与HNO2反应的化学方程式为________________ 。
(4)NSR技术可有效降低柴油发动机在空气过量条件下的NOx排放。NOx的储存和还原在不同时段交替进行,如图1所示:若用H2模拟尾气中还原性气体研究Ba(NO3)2的催化还原过程,该过程分两步进行,图2表示该过程相关物质浓度随时间的变化关系。

①根据图1分析可以得出BaO的作用是________________ 。
②根据图2分析用H2模拟尾气中还原性气体研究Ba(NO3)2的催化还原过程,第一步反应的化学方程为________________ 。
③还原过程中,有时会产生笑气(N2O)。用同位素示踪法研究发现笑气的产生与NO有关。在有O2条件下15NO与NH3以一定比例反应时,得到的笑气几乎都是15NNO。请写出该反应的化学方程式________________ 。
金属与不同密度硝酸溶液反应时,还原产物百分比与硝酸密度的关系下图所示:

(1)当硝酸溶液的密度为1.36g.cm-3时,下列化学方程式中,能较准确表达Fe与过量硝酸反应的是(填序号)
A.
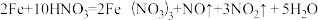
B.

C.
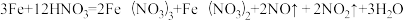
(2)现有一定量铝粉和铜粉的混合物与一定量很稀的硝酸溶液充分反应,反应过程中无气体放出。在反应结束后的溶液中,逐滴加入5mo/L的NaOH溶液,所加NaOH溶液的体积与产生沉淀的物质的量关系如下图所示:

①c点对应NaOH溶液的体积为
②ef段发生反应的离子方程式为
(3)研究表明硝酸与金属反应时,最容易生成亚硝酸(HNO2,弱酸),然后才转化成NO2,如果溶液中存在更强的氧化剂,如过氧化氢,它完全有能力将新产生的HNO2再氧化成HNO3,如图为金属在不同浓度的HNO3-H2O2混合溶液中的溶解速率和生成NOx的体积V的变化示意图:

①最佳溶解金属的混合溶液中HNO3的质量分数
②H2O2与HNO2反应的化学方程式为
(4)NSR技术可有效降低柴油发动机在空气过量条件下的NOx排放。NOx的储存和还原在不同时段交替进行,如图1所示:若用H2模拟尾气中还原性气体研究Ba(NO3)2的催化还原过程,该过程分两步进行,图2表示该过程相关物质浓度随时间的变化关系。

①根据图1分析可以得出BaO的作用是
②根据图2分析用H2模拟尾气中还原性气体研究Ba(NO3)2的催化还原过程,第一步反应的化学方程为
③还原过程中,有时会产生笑气(N2O)。用同位素示踪法研究发现笑气的产生与NO有关。在有O2条件下15NO与NH3以一定比例反应时,得到的笑气几乎都是15NNO。请写出该反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】完成以下离子方程式:
(1)向酸性高锰酸钾溶液中加入草酸溶液_______ 。
(2)向硫酸铝铵溶液中加入过量的氢氧化钡溶液_______ 。
(3)用亚硫酸钠溶液吸收少量氯气_______ 。
(4)泡沫灭火器的工作原理_______ 。
(5)向氯化镁溶液中滴加碳酸钠溶液,生成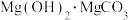
_______ 。
(1)向酸性高锰酸钾溶液中加入草酸溶液
(2)向硫酸铝铵溶液中加入过量的氢氧化钡溶液
(3)用亚硫酸钠溶液吸收少量氯气
(4)泡沫灭火器的工作原理
(5)向氯化镁溶液中滴加碳酸钠溶液,生成
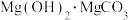
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】学习元素化合物时可以借助“价类二维图”预测物质性质。如下是部分含硫化合物的二维图的相关信息。

(1)图中“X”代表的物质类别是_______ ;Y转化为Z体现了Y的_______ 性。
(2)SO2是重要的大气污染物,会导致“酸雨”。SO2产生硫酸型酸雨有两条途径:途径一是SO2→SO3→H2SO4;另一途径是:SO2→_______ 。
(3)将装有SO2的试管倒立在水槽中,可观察到_______ 。取出试管中的溶液,分别进行如下实验:
①滴加品红溶液,振荡,观察到红色褪去,说明SO2具有_______ 性。
②滴加BaCl2溶液,无明显现象,再滴入FeCl3溶液后出现白色沉淀。出现白色沉淀的原因_______ 。
(4)根据SO2的性质,提出一种燃煤脱硫的方法_______ 。

(1)图中“X”代表的物质类别是
(2)SO2是重要的大气污染物,会导致“酸雨”。SO2产生硫酸型酸雨有两条途径:途径一是SO2→SO3→H2SO4;另一途径是:SO2→
(3)将装有SO2的试管倒立在水槽中,可观察到
①滴加品红溶液,振荡,观察到红色褪去,说明SO2具有
②滴加BaCl2溶液,无明显现象,再滴入FeCl3溶液后出现白色沉淀。出现白色沉淀的原因
(4)根据SO2的性质,提出一种燃煤脱硫的方法
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】氮氧化物(NO、NO2)、SO2是大气污染物。回答下列问题:
(1)以上污染物会造成的环境问题有_______ (写一种即可)。
(2)如图包含气体发生装置和收集装置(部分装置的夹持仪器已省略),实验室以Cu与浓HNO3反应制备并收集NO2,应选择的装置是_______ (填字母)。

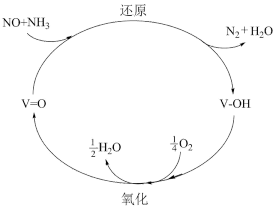
(3)SCR脱硝技术已成为使用广泛和成熟的烟气净化技术,脱硝效率高达90%以上。值,化反应机理如图所示,写出该反应发生的化学方程式:_______
(4)目前,NaClO溶液广泛地应用于脱硫脱硝。某课外小组同学设计了如图喷淋吸收塔装置(如图)。设计该装置的优点是_______ 脱硝(NO)反应的离子方程式为_______ 。

(5)某兴趣小组用Fe2(SO4);溶液吸收含SO2的尾气(SO2的体积分数约10%,其余为空气),实验装置如图所示:

①装置A中用Fe2(SO4);溶液吸收SO2反应的离子方程式:_______ 。
②反应后,若要检验SO2是否过量,可用试剂为_______ 。
③若实验测得反应后的装置A中不含有SO2,为测定其中所含FeSO4的物质的量浓度,现进行如下实验:取20.00mL装置A中溶液,向其中逐滴加入0.1000mol·L-1Ce(SO4)2溶液,发生反应Fe2++Ce4+=Ce3++Fe3+,当反应恰好完全时,共消耗Ce(SO4)2溶液18.00mL。请通过计算确定FeSO4的物质的量浓度_______ 。
(1)以上污染物会造成的环境问题有
(2)如图包含气体发生装置和收集装置(部分装置的夹持仪器已省略),实验室以Cu与浓HNO3反应制备并收集NO2,应选择的装置是

(3)SCR脱硝技术已成为使用广泛和成熟的烟气净化技术,脱硝效率高达90%以上。值,化反应机理如图所示,写出该反应发生的化学方程式:

(4)目前,NaClO溶液广泛地应用于脱硫脱硝。某课外小组同学设计了如图喷淋吸收塔装置(如图)。设计该装置的优点是

(5)某兴趣小组用Fe2(SO4);溶液吸收含SO2的尾气(SO2的体积分数约10%,其余为空气),实验装置如图所示:

①装置A中用Fe2(SO4);溶液吸收SO2反应的离子方程式:
②反应后,若要检验SO2是否过量,可用试剂为
③若实验测得反应后的装置A中不含有SO2,为测定其中所含FeSO4的物质的量浓度,现进行如下实验:取20.00mL装置A中溶液,向其中逐滴加入0.1000mol·L-1Ce(SO4)2溶液,发生反应Fe2++Ce4+=Ce3++Fe3+,当反应恰好完全时,共消耗Ce(SO4)2溶液18.00mL。请通过计算确定FeSO4的物质的量浓度
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】自然界中的含硫物质通过各种化学过程建立起硫循环,其循环过程如下图所示:
1.下列说法错误的是___________。
2.空气中粉尘可能在过程①中起到___________ 作用,收集一定量的酸雨,发现短时间内样品的 值一直在
值一直在___________ (填“变大”或“变小”),说明其溶质不仅仅是 。
。
Ⅱ.过程②
微生物的厌氧活动可产生 并将其排向大气中,
并将其排向大气中, 可在空气中被氧化为
可在空气中被氧化为
3.实验室产生多余 ,可用
,可用 溶液进行吸收,当
溶液进行吸收,当 吸收了过量
吸收了过量 时,其溶质的电离方程式为:
时,其溶质的电离方程式为:___________ 。
4.还可用硫酸铜溶液吸收 ,现象是溶液中产生黑色沉淀,写出反应的离子方程式:
,现象是溶液中产生黑色沉淀,写出反应的离子方程式:___________ 。
5. 还是工业制硫酸的重要中间物质,它可以通过硫酸厂的沸腾炉中
还是工业制硫酸的重要中间物质,它可以通过硫酸厂的沸腾炉中 (过硫化亚铁)与氧气的反应得到,用单线桥法标明电子转移:
(过硫化亚铁)与氧气的反应得到,用单线桥法标明电子转移:___________ 。

6. 与酸反应时生成
与酸反应时生成 与
与 相似,易分解。实验室用过量稀硫酸与
相似,易分解。实验室用过量稀硫酸与 颗粒混合,不可能生成的物质是___________。
颗粒混合,不可能生成的物质是___________。
Ⅲ.过程③7.海水中硫酸根离子含量大约为 ,会干扰海水中
,会干扰海水中 的检验,写出检验海水中
的检验,写出检验海水中 的实验方法
的实验方法___________ 。IV.过程④生物体内少量的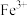 和
和 反应生成
反应生成 和S,说明
和S,说明 具有还原性8.某种卤离子也能与
具有还原性8.某种卤离子也能与 在溶液中作用生成亚铁盐与卤素单质,它应该是___________。
在溶液中作用生成亚铁盐与卤素单质,它应该是___________。
9.由于化石能源的开采与使用量的不断增长,直接导致硫循环中的过程___________加剧,对环境造成了一定程度的破坏,请提出减缓这一过程的措施。
10.措施:___________ 。

1.下列说法错误的是___________。
A.工厂废气中的 与 与 可能来自于煤炭中的含硫物质。 可能来自于煤炭中的含硫物质。 |
| B.火山口产生的气体可以使酸性高锰酸钾溶液褪色,说明其具有漂白性 |
C. 有毒,其含量是空气污染程度指标之一 有毒,其含量是空气污染程度指标之一 |
D. 可添加到红酒中,起到一定的杀菌、抗氧化作用 可添加到红酒中,起到一定的杀菌、抗氧化作用 |
 值一直在
值一直在 。
。Ⅱ.过程②
微生物的厌氧活动可产生
 并将其排向大气中,
并将其排向大气中, 可在空气中被氧化为
可在空气中被氧化为
3.实验室产生多余
 ,可用
,可用 溶液进行吸收,当
溶液进行吸收,当 吸收了过量
吸收了过量 时,其溶质的电离方程式为:
时,其溶质的电离方程式为:4.还可用硫酸铜溶液吸收
 ,现象是溶液中产生黑色沉淀,写出反应的离子方程式:
,现象是溶液中产生黑色沉淀,写出反应的离子方程式:5.
 还是工业制硫酸的重要中间物质,它可以通过硫酸厂的沸腾炉中
还是工业制硫酸的重要中间物质,它可以通过硫酸厂的沸腾炉中 (过硫化亚铁)与氧气的反应得到,用单线桥法标明电子转移:
(过硫化亚铁)与氧气的反应得到,用单线桥法标明电子转移:
6.
 与酸反应时生成
与酸反应时生成 与
与 相似,易分解。实验室用过量稀硫酸与
相似,易分解。实验室用过量稀硫酸与 颗粒混合,不可能生成的物质是___________。
颗粒混合,不可能生成的物质是___________。A. | B.S | C. | D. |
 ,会干扰海水中
,会干扰海水中 的检验,写出检验海水中
的检验,写出检验海水中 的实验方法
的实验方法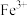 和
和 反应生成
反应生成 和S,说明
和S,说明 具有还原性8.某种卤离子也能与
具有还原性8.某种卤离子也能与 在溶液中作用生成亚铁盐与卤素单质,它应该是___________。
在溶液中作用生成亚铁盐与卤素单质,它应该是___________。A. | B. | C. | D. |
| A.① | B.② | C.③ | D.④ |
您最近一年使用:0次

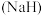 广泛应用于工业生产。
广泛应用于工业生产。 能与水剧烈反应:
能与水剧烈反应: ,该反应中的氧化剂是
,该反应中的氧化剂是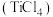 还原成金属钛,该反应的化学方程式为
还原成金属钛,该反应的化学方程式为

