
根据上述装置,回答下列问题:
(1)C装置的作用是
(2)已知:1,2—二溴乙烷的密度比水的大,难溶于水,易溶于四氯化碳。
预测:A装置中的现象是
(3)D装置中溶液由紫色变无色,D装置中发生反应的类型为
(4)写出A装置中发生反应的化学方程式
(5)做乙烯燃烧实验之前必须进行的操作是
(6)丙烯(CH2=CHCH3)与乙烯具有相似的化学性质(写结构简式)。
①丙烯与Br2的加成产物为
②在一定条件下丙烯与H2O的加成产物可能为
相似题推荐
【推荐1】I.在最新的家用汽车的调查中发现,新车中气体的质量不符合标准.汽车污染主要来源于汽车配件及材料,它们都会产生大量的有毒有机物.其中一种有毒物质A,为了测定有机物A的结构,做如下实验:
①将9.2g该有机物完全燃烧,生成标况下15.68L的CO2和7.2g水;
②用质谱仪测定其相对分子质量,得如图一所示的质谱图;
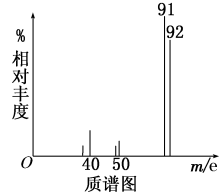
则由图可知该分子的相对分子质量是
II. 已知:A是石油裂解气的主要成分,A的产量通常用来衡量一个国家的石油化工水平;由A通过聚合反应生成高分子化合物F,F可用于工业合成塑料,现以A为主要原料合成G,以A为原料的合成路线如下图所示。回答下列问题:
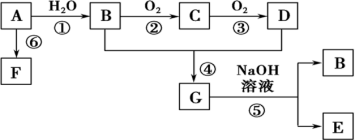
(1)写出②、④ 、⑤两步反应的化学方程式,并注明反应类型:
②
④
⑤
(2)写出由C与新制氢氧化铜反应的化学方程式及实验现象:
| 密度(g∙cm-3) | 熔点(℃) | 沸点(℃) | 溶解性 | |||
| 环己醇 | 0.96 | 25 | 161 | 能溶于水 | ||
| 环己烯 | 0.81 | -103 | 83 | 难溶于水 | ||
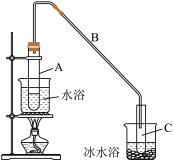
①写出生成环己烯的方程式
②试管C置于冰水浴中的目的是
(2)制备精品:
①环己烯粗品中含有环己醇和少量有机酸性杂质等。加入饱和食盐水,振荡、静置、分层,环己烯在
a.
 溶液 B.稀
溶液 B.稀 C.
C. 溶液 D.
溶液 D.
②再将环己烯按如图装置蒸馏,冷却水从
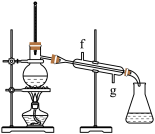
③收集产品时,控制的温度应在
a.蒸馏时从70℃开始收集产品
b.环己醇实际用量多了
c.制备粗品时环己醇随产品一起蒸出
(3)以下区分环己烯精品和粗品的方法,合理的是
a.用酸性高锰酸钾溶液 b.用金属钠 c.测定沸点
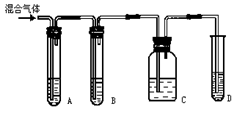
(1)如图所示A、B、C、D装置中可盛放的试剂是(填序号)
A.
①CuSO4溶液 ②NaOH溶液 ③溴水 ④KMnO4酸性溶液
(2)能说明H2S气体存在的现象是
(3)使用装置B的目的是
(4)使用装置C的目的是
(5)确证含有乙炔的现象是
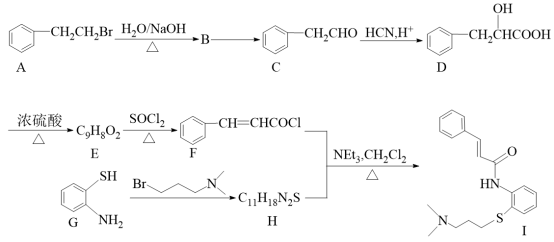
回答下列问题:
(1)肉桂硫胺(I)能使溴的四氯化碳溶液褪色是因为分子中含有
(2)B→C的反应类型为
(3)G→H反应的化学方程式为
(4)化合物Y与D互为同分异构体,且满足下列条件:
①能水解,且能发生银镜反应;
②与NaOH溶液反应时,1 mol Y最多可消耗3 mol NaOH;
③核磁共振氢谱有4组峰,峰面积之比为1∶1∶2∶6。
则Y的结构简式为
(5)根据上述路线中的相关知识,设计以
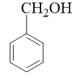 为原料合成
为原料合成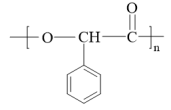 的路线
的路线(1)傅瑞德尔一克拉福茨反应是在苯环上引入烷基的反应:
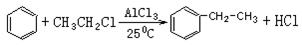
(2)
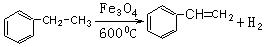
(3)烯烃与HX(X为原子或原子团)加成时,氢原子总是加在含氢较多的不饱和碳上,
即:

某同学给出了以乙烯、苯、食盐、水等为原料合成
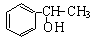 的部分流程图:
的部分流程图:
试回答下列问题:
(1)反应物A可由食盐、水经一系列反应获得,则反应物A为 (填化学式),写出制备A 的化学方程式
(2)反应物B为 (填化学式)
(3)反应Ⅰ~ Ⅳ中,属于加成反应的是 (填序号)
(4)中间产物C的属于芳香烃的同分异构体有 种(不包括自身),其中苯环上的一氯代物有2种的是 (写结构简式)
(5)下列关于中间产物D的说法不正确的是
| A.既能使酸性高锰酸钾溶液褪色,也能使溴水褪色 |
| B.既能溶于水,也能溶于苯中 |
| C.1mol 中间产物D最多可与4mol H2完全反应 |
| D.所有原子不可能共平面 |
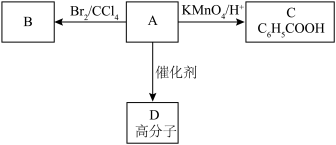
已知:苯环侧链上的烃基在一定条件下可以被氧化成羧基
(1)有机化合物A的结构简式为
(2)下列关于有机化合物A的说法正确的是___________(填字母)。
| A.属于芳香烃 | B.属于苯的同系物 | C.侧链中含碳碳双键 | D.有顺反异构体 |
(4)D具有优良的绝缘、绝热性能,可用作包装材料和建筑材料,在工业上以A为原料生产。写出相关反应的化学方程式
 ,含少量Fe、Al、Mg等杂质元素)制备高纯碳酸锰的实验过程如下,其中植物粉的作用是作还原剂。
,含少量Fe、Al、Mg等杂质元素)制备高纯碳酸锰的实验过程如下,其中植物粉的作用是作还原剂。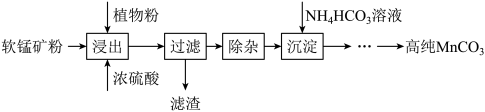
(1)浸出:漫出时温度控制在90℃~95℃之间,并且要连续搅拌3小时的目的是
(2)除杂:①向浸出液中加入一定量的碳酸锰矿,调节浸出液的pH为3.5-5.5;
②再加入一定量的软锰矿和双氧水,过滤;
③…
操作②中加入双氧水不仅能将
 氧化为
氧化为 ,而且能提高软锰矿的浸出率。写出双氧水提高软锰矿浸出率的离子方程式
,而且能提高软锰矿的浸出率。写出双氧水提高软锰矿浸出率的离子方程式(3)制备:①在30℃~35℃下,将碳酸氢铵溶液滴加到硫酸锰净化液中,控制反应液的最终pH在6.5~7.0,得到
 沉淀。该反应的化学方程式为
沉淀。该反应的化学方程式为②生成的
 沉淀需经充分洗涤,洗涤
沉淀需经充分洗涤,洗涤 沉淀的实验操作是:
沉淀的实验操作是:③检验沉淀是否洗涤干净的方法是
(4)计算:室温下,
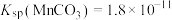 ,
,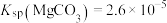 ,已知离子浓度小于
,已知离子浓度小于 mol·L
mol·L 时,表示该离子沉淀完全。若净化液中的
时,表示该离子沉淀完全。若净化液中的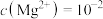 mol/L,试计算说明
mol/L,试计算说明 的存在是否会影响
的存在是否会影响 的纯度
的纯度 的熔点为
的熔点为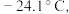 ,沸点为
,沸点为 ,在潮湿空气中易水解。回答下列问题:
,在潮湿空气中易水解。回答下列问题: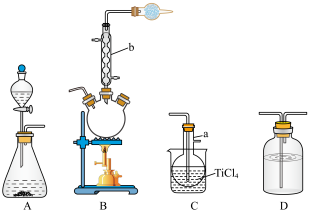
(1)B装置中仪器b的名称为
a.温水浴 b.热水浴 c.油浴
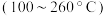 d.沙浴
d.沙浴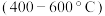
(2)写出B装置中制备
 的化学方程式为
的化学方程式为(3)测定产品中
 (产品中其他杂质不发生下述化学反应)的纯度的方法是:精确称取0.2000g产品放入锥形瓶中,加入热的硫酸和硫酸铵的混合溶液,使其溶解。冷却,稀释,得到含
(产品中其他杂质不发生下述化学反应)的纯度的方法是:精确称取0.2000g产品放入锥形瓶中,加入热的硫酸和硫酸铵的混合溶液,使其溶解。冷却,稀释,得到含 的溶液。加入金属铝,将
的溶液。加入金属铝,将 全部转化为
全部转化为 加入指示剂,用
加入指示剂,用 溶液滴定至终点。重复操作3次,平均消耗0.1000mol·
溶液滴定至终点。重复操作3次,平均消耗0.1000mol· 溶液20.00mL(已知:ˊ
溶液20.00mL(已知:ˊ
①配制
 ,标准溶液时,需使用的仪器除玻璃棒、托盘天平、药匙、量筒外,还需要下图中的
,标准溶液时,需使用的仪器除玻璃棒、托盘天平、药匙、量筒外,还需要下图中的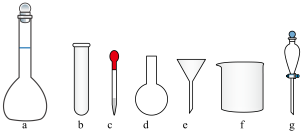
②滴定时用到的指示剂为
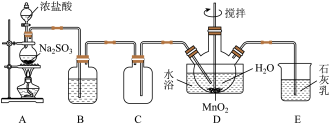
(2)装置B中的试剂为
(3)装置D中发生反应的化学方程式为
(4)装置D中水浴温度应控制在80°C左右,温度不能过高的原因是
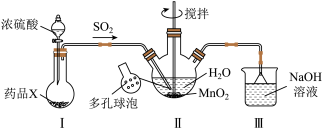
(5)乙同学认为甲同学的设计过于复杂,设计了仅用如图所示装置制备硫酸锰:
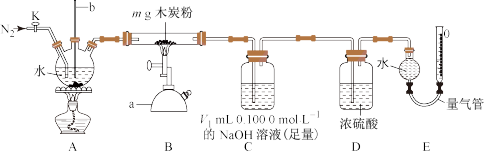
(1)仪器a的名称为
(2)实验步骤:连接好装置,检查装置的气密性;
①向装置A、B、C、D中分别加入相应试剂,打开活塞K,通入一段时间N2。
②加热装置B处硬质玻璃管。
③关闭活塞K,连接盛有适量水的量气管。
④点燃装置A处酒精灯。
⑤待装置B处木炭粉完全反应后,停止加热。
(3)装置B处硬质玻璃管中发生的所有反应的化学方程式为
(4)读取B气管读数时,应注意的事项为冷却至室温、
(5)实验后所得气体体积为V2 mL(标准状况);取装置C中液体,加入足量BaCl2溶液,过滤、洗涤,将滤液和洗涤液合并,以甲基橙为指示剂,用0.1000 mol·L−1的盐酸标准溶液滴定,达到滴定终点时,消耗标准溶液的体积为V3mL。
①达到滴定终点时的现象为
②H2的产率为
③还可通过
(6)从安全角度考虑,该实验装置的缺陷为
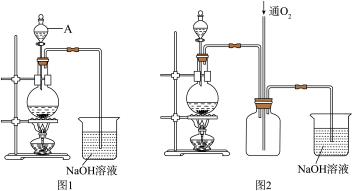
(1)图1中A仪器的名称
(2)图2是图1的改进装置,其优点有:①
(3)为符合绿色化学的要求,某研究性学习小组进行如下设计:
第一组:以空气为氧化剂法
方案1:以空气为氧化剂。将铜粉在仪器B中反复灼烧,使铜与空气充分反应生成氧化铜,再将氧化铜与稀硫酸反应。
方案2:将空气或氧气直接通入到铜粉与稀硫酸的混合物中,发现在常温下几乎不反应。向反应液中加FeSO4或Fe2(SO4)3,即发生反应。反应完全后向其中加物质甲调节pH到3~4,产生Fe(OH)3沉淀,过滤、蒸发、结晶,滤渣作催化剂循环使用。(已知Fe(OH)3和Cu(OH)2完全沉淀时的pH分别为3.7、6.4。)
请回答下列问题:
①方案1中的B仪器名称是
②方案2中甲物质是
a.CaO b.CuCO3 c.CaCO3 d.NH3▪H2O
第二组:过氧化氢为氧化剂法
将3.2g铜丝放到45 mL 1.5mol/L的稀硫酸中,控温在50℃。加入18mL 10%的H2O2,反应0.5小时后,升温到60℃,持续反应1 小时后,过滤.蒸发结晶.减压抽滤等,用少量95%的酒精淋洗后晾干,得CuSO4·5H2O10.6g。
请回答下列问题:
③加热时温度不宜过高的原因是
④上述两种氧化法中,更符合绿色化学理念的是
A.固态氯化铵加热分解
B.氢氧化钠溶液中滴加稀氨水
C.氯化铵溶液与氢氧化钠溶液共热
D.固态氯化铵与氢氧化钙混合加热
②检验氨气是否已经收集满的方法是
③为了得到干燥的NH3,用
A.碱石灰 B.浓H2SO4 C.无水CaCl2 D.P2O5
(2)为了验证木炭可被浓H2SO4氧化成CO2,选用下图所示仪器(内含物质)组装成实验装置。
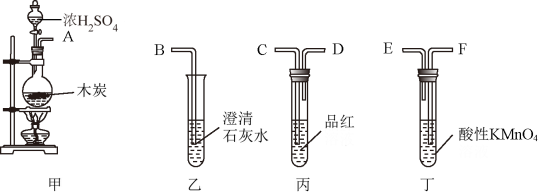
①如按气流由左向右流向,连接上述装置(各装置只用一次)的正确顺序是(填各接口字母):A→
②什么样的实验现象才表明已检验出CO2?
③写出甲中反应的化学方程式



