海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在。实验室从海藻中提取碘的流程如图 :
:
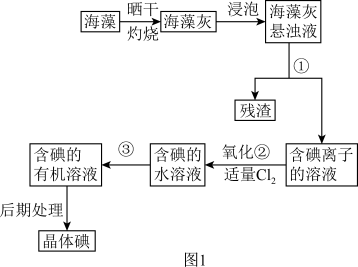
(1)指出提取碘的过程中有关的实验操作名称:③_______ ;
(2)提取碘的过程中,可供选择的有关试剂是_______ 。
A.甲苯、酒精 B.四氯化碳、苯 C.汽油、乙酸
(3)为使海藻灰中碘离子转化为碘的有机溶液,实验室准备了烧杯、玻璃棒、集气瓶、酒精灯、导管、圆底烧瓶、石棉网以及必要的夹持仪器、物品,尚缺少的玻璃仪器是_______ 。
(4)从含碘的有机溶液中提取碘和回收有机溶剂,还需经过蒸馏,指出如图 所示实验装置中的错误有
所示实验装置中的错误有_______ 处。
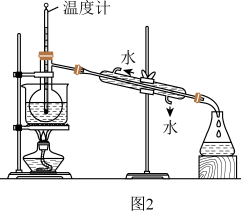
(5)进行上述蒸馏操作时,使用水浴的原因是_______ 。
 :
:
(1)指出提取碘的过程中有关的实验操作名称:③
(2)提取碘的过程中,可供选择的有关试剂是
A.甲苯、酒精 B.四氯化碳、苯 C.汽油、乙酸
(3)为使海藻灰中碘离子转化为碘的有机溶液,实验室准备了烧杯、玻璃棒、集气瓶、酒精灯、导管、圆底烧瓶、石棉网以及必要的夹持仪器、物品,尚缺少的玻璃仪器是
(4)从含碘的有机溶液中提取碘和回收有机溶剂,还需经过蒸馏,指出如图
 所示实验装置中的错误有
所示实验装置中的错误有
(5)进行上述蒸馏操作时,使用水浴的原因是
更新时间:2022-03-15 14:41:40
|
相似题推荐
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐1】Ag是高新技术产业的基础材料之一,依据下列回收Ag的方案回答下列问题:
(1)利用废旧电池中的 可将有毒气体甲醛(HCHO)氧化成
可将有毒气体甲醛(HCHO)氧化成 ,将上述反应设计成原电池,在
,将上述反应设计成原电池,在___________ (填“正”或“负”)极可获得Ag。
(2)以含 的废定影液为原料提取银的主要步骤为:加入过量
的废定影液为原料提取银的主要步骤为:加入过量 溶液后,过滤、洗涤、干燥。将获得的
溶液后,过滤、洗涤、干燥。将获得的 在足量空气中充分焙烧制得Ag。实验室焙烧
在足量空气中充分焙烧制得Ag。实验室焙烧 在
在___________ (填仪器名称)中完成,焙烧 的化学方程式是
的化学方程式是___________ ,常温下, 饱和溶液中
饱和溶液中 的浓度为a mol/L,则常温下
的浓度为a mol/L,则常温下 的溶度积常数
的溶度积常数 为
为___________ 。
(3)从光盘金属层中提取Ag(其他微量金属忽略不计)的流程如下图所示:
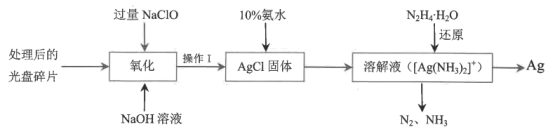
①“氧化”阶段需在80℃条件下进行,最适合的加热方式为___________ ,操作Ⅰ的名称为___________ 。
②“还原”过程 的氧化产物为
的氧化产物为 ,理论上消耗1mol
,理论上消耗1mol 可生成单质Ag的质量为
可生成单质Ag的质量为___________ 克。
③NaClO溶液与Ag反应有 生成,该反应的离子方程式为
生成,该反应的离子方程式为___________ 。
(1)利用废旧电池中的
 可将有毒气体甲醛(HCHO)氧化成
可将有毒气体甲醛(HCHO)氧化成 ,将上述反应设计成原电池,在
,将上述反应设计成原电池,在(2)以含
 的废定影液为原料提取银的主要步骤为:加入过量
的废定影液为原料提取银的主要步骤为:加入过量 溶液后,过滤、洗涤、干燥。将获得的
溶液后,过滤、洗涤、干燥。将获得的 在足量空气中充分焙烧制得Ag。实验室焙烧
在足量空气中充分焙烧制得Ag。实验室焙烧 在
在 的化学方程式是
的化学方程式是 饱和溶液中
饱和溶液中 的浓度为a mol/L,则常温下
的浓度为a mol/L,则常温下 的溶度积常数
的溶度积常数 为
为(3)从光盘金属层中提取Ag(其他微量金属忽略不计)的流程如下图所示:

①“氧化”阶段需在80℃条件下进行,最适合的加热方式为
②“还原”过程
 的氧化产物为
的氧化产物为 ,理论上消耗1mol
,理论上消耗1mol 可生成单质Ag的质量为
可生成单质Ag的质量为③NaClO溶液与Ag反应有
 生成,该反应的离子方程式为
生成,该反应的离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐2】碘在生产生活和医疗中都有重要用途,海带中含有碘元素。从海带中提取碘的实验过程如图:

(1)实验步骤①需用到下列仪器中的___________ (填标号) ,实验操作步骤③的名称为___________ 。
A.酒精灯
B.漏斗
C.坩埚
D.泥三角
(2)步骤④中发生反应的离子方程式为___________ 。
(3)海带灰中含有硫酸盐、碳酸盐等,在步骤___________ (填序号)中实现与碘分离。
(4)某课题组以碘为对象,经多年研究,获得一种安全 、稳定高效的水系碘一氢气电池 ,其工作原理如图。
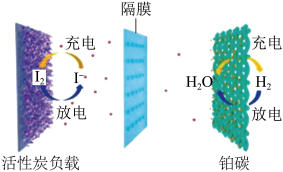
①该电池属于___________ (填“一次”或“二次”)电池。
②该电池对外提供电能时,I2在___________ (填“正”或“负”)极,发生___________ (填“氧化”或“还原”)反应,溶液中阴离子向___________ (填“活性炭负载”或“铂碳”)电极移动。

(1)实验步骤①需用到下列仪器中的
A.酒精灯
B.漏斗
C.坩埚
D.泥三角
(2)步骤④中发生反应的离子方程式为
(3)海带灰中含有硫酸盐、碳酸盐等,在步骤
(4)某课题组以碘为对象,经多年研究,获得一种安全 、稳定高效的水系碘一氢气电池 ,其工作原理如图。

①该电池属于
②该电池对外提供电能时,I2在
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
【推荐3】MnO2是重要的化工原料,软锰矿制备MnO2的一种工艺流程如图:

资料:①软锰矿的主要成分为MnO2,主要杂质有Al2O3和SiO2
②金属离于沉淀的pH
③该工艺条件下,MnO2与H2SO4反应。
(1)溶出
①溶出前,软锰矿需研磨。目的是___________ 。
②溶出时,Fe的氧化过程及得到Mn2+的主要途径如图所示:

i.步骤 是从软锰矿中溶出Mn2+的主要反应,反应的离子方程式是
是从软锰矿中溶出Mn2+的主要反应,反应的离子方程式是___________ 。
ii.若Fe2+全部来自于反应Fe+2H+=Fe2++H2↑,完全溶出Mn2+所需Fe与MnO2的物质的量比值为2。而实际比值(0.9)小于2,原因是___________ 。
(2)纯化。已知:MnO2的氧化性与溶液pH有关。纯化时先加入MnO2,目的是___________ ,后加入NH3·H2O,调节溶液pH的区间是:___________ 。
(3)电解Mn2+纯化液经电解得MnO2。生成MnO2的电极反应式是___________ 。
(4)写出铁原子26Fe的电子排布式:___________ 。

资料:①软锰矿的主要成分为MnO2,主要杂质有Al2O3和SiO2
②金属离于沉淀的pH
| Fe3+ | Al3+ | Mn2+ | Fe2+ | |
| 开始沉淀时 | 1.5 | 3.4 | 5.8 | 6.3 |
| 完全沉淀时 | 2.8 | 4.7 | 7.8 | 8.3 |
(1)溶出
①溶出前,软锰矿需研磨。目的是
②溶出时,Fe的氧化过程及得到Mn2+的主要途径如图所示:

i.步骤
 是从软锰矿中溶出Mn2+的主要反应,反应的离子方程式是
是从软锰矿中溶出Mn2+的主要反应,反应的离子方程式是ii.若Fe2+全部来自于反应Fe+2H+=Fe2++H2↑,完全溶出Mn2+所需Fe与MnO2的物质的量比值为2。而实际比值(0.9)小于2,原因是
(2)纯化。已知:MnO2的氧化性与溶液pH有关。纯化时先加入MnO2,目的是
(3)电解Mn2+纯化液经电解得MnO2。生成MnO2的电极反应式是
(4)写出铁原子26Fe的电子排布式:
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐1】某学习小组按如下实验流程探究海带中碘含量的测定和碘的制取。
实验(一) 碘含量的测定

取100.00 mL 海带浸取原液于锥形瓶中,用 0.0100 mol•L-1的AgNO3标准溶液测定其中的碘,消耗标准溶液体积的平均值为20.00 mL。
(1)仪器A 的名称为___________ ;所用仪器B为___________ 。
(2)计算海带中碘的百分含量为___________ %(保留3位有效数字)。
实验(二) 碘的制取
另取海带浸取原液,甲、乙两种实验方案如下:
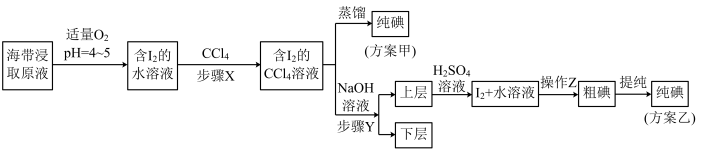
已知:3I2+6NaOH=5NaI+NaIO3+3H2O,酸性条件下I2在水中的溶解度很小。
(3)“适量O2”中能代替O2的最佳物质的电子式为___________ 。
(4)下列有关步骤Y 的说法中正确的是___________ (填选项字母),步骤Y 中的方法称为___________ 。
A.应控制 NaOH 溶液的浓度和体积
B.将碘转化成离子进入水层
C.主要是除浸取原液中的有机杂质
D.NaOH 溶液可由乙醇代替
(5)方案乙中液体中加入 H2SO4溶液,反应的离子方程式为__________________ ,其中操作Z的名称是___________ 。
实验(一) 碘含量的测定

取100.00 mL 海带浸取原液于锥形瓶中,用 0.0100 mol•L-1的AgNO3标准溶液测定其中的碘,消耗标准溶液体积的平均值为20.00 mL。
(1)仪器A 的名称为
(2)计算海带中碘的百分含量为
实验(二) 碘的制取
另取海带浸取原液,甲、乙两种实验方案如下:

已知:3I2+6NaOH=5NaI+NaIO3+3H2O,酸性条件下I2在水中的溶解度很小。
(3)“适量O2”中能代替O2的最佳物质的电子式为
(4)下列有关步骤Y 的说法中正确的是
A.应控制 NaOH 溶液的浓度和体积
B.将碘转化成离子进入水层
C.主要是除浸取原液中的有机杂质
D.NaOH 溶液可由乙醇代替
(5)方案乙中液体中加入 H2SO4溶液,反应的离子方程式为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐2】(1)实验室从海带中提取碘的流程如下:
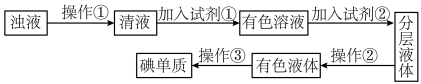
①指出过程中有关的实验操作①和②名称:①___ ,②___ 。
②下列物质中,能使湿润的KI-淀粉试纸变蓝的是___ 。
A.碘蒸气 B.Cl2 C.KI溶液 D.饱和氯化钠溶液
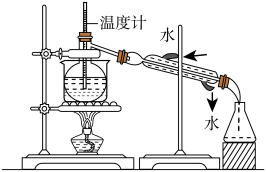
③有同学试图利用蒸馏方法来实现第③步操作,该同学设计了如图蒸馏实验装置,此装置中的明显错误之处为____ 、____ 。
④试剂①若用H2O2溶液和稀硫酸,请写出发生反应的离子方程式___ 。
(2)SO2的排放是造成酸雨的主要因素,某同学通过实验探究,得出酸雨pH随时间的增加而减小的结论。为进一步研究酸雨的成分,该同学取某一时段的这种雨水VL加入0.50mol/LBa(OH)2溶液至不再产生沉淀时,恰好消耗40.00mLBa(OH)2溶液。请完成
①该酸雨pH随时间的增加而减小的原因是___ (用化学方程式解释),
②若生成沉淀物的质量为4.50g,则沉淀物的组成为___ (填写化学式)。

①指出过程中有关的实验操作①和②名称:①
②下列物质中,能使湿润的KI-淀粉试纸变蓝的是
A.碘蒸气 B.Cl2 C.KI溶液 D.饱和氯化钠溶液
③有同学试图利用蒸馏方法来实现第③步操作,该同学设计了如图蒸馏实验装置,此装置中的明显错误之处为

④试剂①若用H2O2溶液和稀硫酸,请写出发生反应的离子方程式
(2)SO2的排放是造成酸雨的主要因素,某同学通过实验探究,得出酸雨pH随时间的增加而减小的结论。为进一步研究酸雨的成分,该同学取某一时段的这种雨水VL加入0.50mol/LBa(OH)2溶液至不再产生沉淀时,恰好消耗40.00mLBa(OH)2溶液。请完成
①该酸雨pH随时间的增加而减小的原因是
②若生成沉淀物的质量为4.50g,则沉淀物的组成为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐3】以下海带提碘的实验方案可以缩短实验时间,避免氯气和四氯化碳的毒性。实验流程如下:
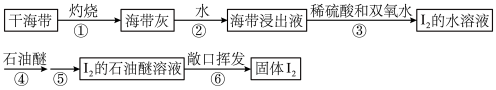
(1)步骤①所需的主要仪器有玻璃棒、______ 和______ 。
(2)步骤③中加入双氧水后发生反应的化学方程式为_________ ;选择用双氧水做氧化剂的因是________ 。
(3)检验I2的水溶液中含有单质碘的方法是取样于试管中,加入____ ,如溶液显___ 色,则可证明含有碘单质。
(4)步骤④的操作名称是_____ ;石油醚能提取碘水中的碘,说明石油醚具有的性质是________ 。
(5)步骤⑥通过敞口挥发就能得到固体碘,说明石油醚具有良好的______ 性。

(1)步骤①所需的主要仪器有玻璃棒、
(2)步骤③中加入双氧水后发生反应的化学方程式为
(3)检验I2的水溶液中含有单质碘的方法是取样于试管中,加入
(4)步骤④的操作名称是
(5)步骤⑥通过敞口挥发就能得到固体碘,说明石油醚具有良好的
您最近一年使用:0次



