A、B、C、D、E、W为六种前四周期元素,它们的原子序数依次增大。A与C同主族,可形成CA型离子化合物,D是同周期元素中简单离子半径最小的元素,B与E同主族,E2-与Ar原子具有相同的电子层结构,W的合金用量最大、用途最广。回答下列问题:
(1)C在元素周期表中的位置是___________ 。
(2)A分别与B、E形成的最简单化合物中沸点较高的是______ (填化学式),原因是___________ 。
(3)A、B、C三种元素形成的物质中含有的化学键类型是______ 。
(4)D单质与C的最高价氧化物对应水化物的溶液反应,反应的化学方程式为___________ 。
(5)向盛有A2B2溶液的试管中加入几滴酸化的WEB4溶液,溶液变成棕黄色,发生反应的离子方程式为___________ 。
(1)C在元素周期表中的位置是
(2)A分别与B、E形成的最简单化合物中沸点较高的是
(3)A、B、C三种元素形成的物质中含有的化学键类型是
(4)D单质与C的最高价氧化物对应水化物的溶液反应,反应的化学方程式为
(5)向盛有A2B2溶液的试管中加入几滴酸化的WEB4溶液,溶液变成棕黄色,发生反应的离子方程式为
更新时间:2022-04-03 19:58:13
|
相似题推荐
解答题-实验探究题
|
较易
(0.85)
名校
【推荐1】Ⅰ.氯气广泛应用于杀菌、消毒及化工领域,某化学小组设计如图装置制备少量干燥纯净的氯气,试回答下列问题:

(1)盛有浓盐酸仪器名称___________ ,装置的正确连接顺序为___________ ;E→________→_______→________→________→________→________→F。
(2)气体发生装置中发生反应的化学方程式为___________ ,该反应中体现HCl的酸性和___________ 性。
(3)题给装置中饱和食盐水的作用是___________ ,检验氯气是否收集满的方法是___________ 。
(4)写出尾气吸收装置中反应的离子方程式___________ 。
Ⅱ.以上实验所用的氢氧化钠溶液为0.5mol/L,若要配制450mL 0.5mol/L的氢氧化钠溶液
(5)则需要用托盘天平称量___________ g的NaOH固体;若定容时俯视容量瓶,所配制的氢氧化钠溶液浓度会___________ (填“偏低”,“偏高”或“不变”)

(1)盛有浓盐酸仪器名称
(2)气体发生装置中发生反应的化学方程式为
(3)题给装置中饱和食盐水的作用是
(4)写出尾气吸收装置中反应的离子方程式
Ⅱ.以上实验所用的氢氧化钠溶液为0.5mol/L,若要配制450mL 0.5mol/L的氢氧化钠溶液
(5)则需要用托盘天平称量
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐2】水合肼( )常用作航天器燃料,也广泛应用于医药生产。实验室制取水合肼并模拟处理铜氨
)常用作航天器燃料,也广泛应用于医药生产。实验室制取水合肼并模拟处理铜氨 溶液回收铜粉的实验流程如图:
溶液回收铜粉的实验流程如图:
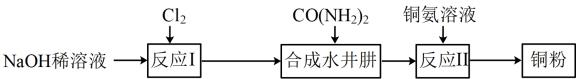
(1)“反应Ⅰ”中温度升高时易产生副产物 。若要提高NaClO产率,可采取的措施有
。若要提高NaClO产率,可采取的措施有_______ (任写一点)。
(2)实验室常采用 固体和浓盐酸在加热条件下制备氯气,该反应的化学方程式为
固体和浓盐酸在加热条件下制备氯气,该反应的化学方程式为_______ 。
(3)“合成水合肼”的过程中,理论上尿素 与NaClO的物质的量之比为1∶1,实际操作时,尿素的用量一般比NaClO的略大,其原因可能是
与NaClO的物质的量之比为1∶1,实际操作时,尿素的用量一般比NaClO的略大,其原因可能是_______ 。
(4)向硫酸铜溶液中逐滴加入氨水至过量,可观察到的实验现象为_______ ;在铜氨 中,配体为
中,配体为_______ ,配位数为_______ 。
(5)由铜氨废液回收铜粉的实验方案如下:收一定量水合肼溶液,加入适量蒸馏水稀释,再滴加适量NaOH溶液,边搅拌边逐滴加入铜氨废液,加热使其充分反应,同时用稀硫酸吸收反应中放出的 ,直至溶液中无气泡产生,停止滴加,静置、过滤、洗涤、干燥。反应中水合肼被氧化,生成
,直至溶液中无气泡产生,停止滴加,静置、过滤、洗涤、干燥。反应中水合肼被氧化,生成 和水,写出水合肼还原铜氨的离子方程式:
和水,写出水合肼还原铜氨的离子方程式:_______ 。
 )常用作航天器燃料,也广泛应用于医药生产。实验室制取水合肼并模拟处理铜氨
)常用作航天器燃料,也广泛应用于医药生产。实验室制取水合肼并模拟处理铜氨 溶液回收铜粉的实验流程如图:
溶液回收铜粉的实验流程如图:
(1)“反应Ⅰ”中温度升高时易产生副产物
 。若要提高NaClO产率,可采取的措施有
。若要提高NaClO产率,可采取的措施有(2)实验室常采用
 固体和浓盐酸在加热条件下制备氯气,该反应的化学方程式为
固体和浓盐酸在加热条件下制备氯气,该反应的化学方程式为(3)“合成水合肼”的过程中,理论上尿素
 与NaClO的物质的量之比为1∶1,实际操作时,尿素的用量一般比NaClO的略大,其原因可能是
与NaClO的物质的量之比为1∶1,实际操作时,尿素的用量一般比NaClO的略大,其原因可能是(4)向硫酸铜溶液中逐滴加入氨水至过量,可观察到的实验现象为
 中,配体为
中,配体为(5)由铜氨废液回收铜粉的实验方案如下:收一定量水合肼溶液,加入适量蒸馏水稀释,再滴加适量NaOH溶液,边搅拌边逐滴加入铜氨废液,加热使其充分反应,同时用稀硫酸吸收反应中放出的
 ,直至溶液中无气泡产生,停止滴加,静置、过滤、洗涤、干燥。反应中水合肼被氧化,生成
,直至溶液中无气泡产生,停止滴加,静置、过滤、洗涤、干燥。反应中水合肼被氧化,生成 和水,写出水合肼还原铜氨的离子方程式:
和水,写出水合肼还原铜氨的离子方程式:
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐3】有 、
、 、
、 、
、 、
、 、
、 六种短周期的主族元素,部分信息如下表所示:
六种短周期的主族元素,部分信息如下表所示:
请回答下列问题:
(1) 在元素周期表中的位置是
在元素周期表中的位置是___________ 。
(2) 的单质与
的单质与 的最高价氧化物对应水化物的水溶液反应的离子方程式为
的最高价氧化物对应水化物的水溶液反应的离子方程式为___________ 。
(3)Z、M、Q的简单离子的半径由小到大的顺序为___________ (用离子符号表示)。
(4)简单氢化物稳定性:M___________ R(填“>”或“<”)。
(5)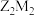 属于
属于___________ 化合物(填“离子”或“共价”),写出它的电子式:___________ 。
(6)写出一条能说明 的金属性比
的金属性比 强的依据:
强的依据:___________ 。
 、
、 、
、 、
、 、
、 、
、 六种短周期的主族元素,部分信息如下表所示:
六种短周期的主族元素,部分信息如下表所示:| 元素 |  |  |  |  |  |  |
| 原子半径/nm | 0.186 | 0.074 | 0.099 | 0.160 | ||
| 主要化合价 | +3 |  |  、 、 | |||
| 其它信息 | 某种核素无中子 | 氧化物具有两性 | 短周期主族元素中原子半径最大 | 次外层电子数是最外层电子数的4倍 |
(1)
 在元素周期表中的位置是
在元素周期表中的位置是(2)
 的单质与
的单质与 的最高价氧化物对应水化物的水溶液反应的离子方程式为
的最高价氧化物对应水化物的水溶液反应的离子方程式为(3)Z、M、Q的简单离子的半径由小到大的顺序为
(4)简单氢化物稳定性:M
(5)
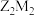 属于
属于(6)写出一条能说明
 的金属性比
的金属性比 强的依据:
强的依据:
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
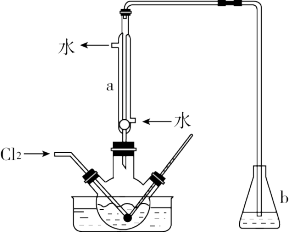
【推荐1】实验室从含碘废液(除H2O外,含有CCl4、I2、I-等)中回收碘,实验过程如图:
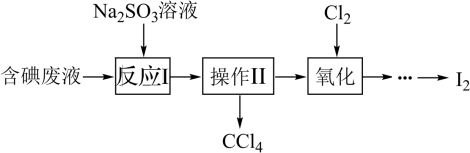
(1)反应I中将I2____ (填“氧化”或“还原”)。
(2)操作II的名称为____ ,实验室进行操作II使用的玻璃仪器有____ 。
(3)氧化时,在三颈瓶中将含I-的水溶液用盐酸调至pH约为2,缓慢通入Cl2,在40℃左右反应(实验装置如图所示)。实验控制在较低温度下进行的原因是____ ;仪器a的名称为____ ;仪器b中盛放的溶液为____ 。
(4)某含碘废水(pH约为8)中一定存在I2,可能存在I-、IO 中的一种或两种。请补充完整检验含碘废水中是否含有I-、IO
中的一种或两种。请补充完整检验含碘废水中是否含有I-、IO 实验方案(实验中可供选择的试剂:稀盐酸、淀粉溶液、FeCl3溶液、Na2SO3溶液)。
实验方案(实验中可供选择的试剂:稀盐酸、淀粉溶液、FeCl3溶液、Na2SO3溶液)。
①取适量含碘废水用CCl4多次萃取、分液,直到水层用淀粉溶液检验不出有碘单质存在;
②另从水层中取少量溶液,加入1~2mL淀粉溶液,加盐酸酸化后,滴加Na2SO3溶液,若溶液变蓝说明废水中含有IO ,发生反应的离子方程式
,发生反应的离子方程式____ 。
③简述溶液中是否含I-:另从水层中取少量溶液,____ 。

(1)反应I中将I2
(2)操作II的名称为
(3)氧化时,在三颈瓶中将含I-的水溶液用盐酸调至pH约为2,缓慢通入Cl2,在40℃左右反应(实验装置如图所示)。实验控制在较低温度下进行的原因是

(4)某含碘废水(pH约为8)中一定存在I2,可能存在I-、IO
 中的一种或两种。请补充完整检验含碘废水中是否含有I-、IO
中的一种或两种。请补充完整检验含碘废水中是否含有I-、IO 实验方案(实验中可供选择的试剂:稀盐酸、淀粉溶液、FeCl3溶液、Na2SO3溶液)。
实验方案(实验中可供选择的试剂:稀盐酸、淀粉溶液、FeCl3溶液、Na2SO3溶液)。①取适量含碘废水用CCl4多次萃取、分液,直到水层用淀粉溶液检验不出有碘单质存在;
②另从水层中取少量溶液,加入1~2mL淀粉溶液,加盐酸酸化后,滴加Na2SO3溶液,若溶液变蓝说明废水中含有IO
 ,发生反应的离子方程式
,发生反应的离子方程式③简述溶液中是否含I-:另从水层中取少量溶液,
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
【推荐2】海带中含有丰富的碘元素。海带灼烧后的海带灰中,碘元素主要以I-形式存在。实验室里,从海带灰中提取碘的甲、乙两种方案如下:
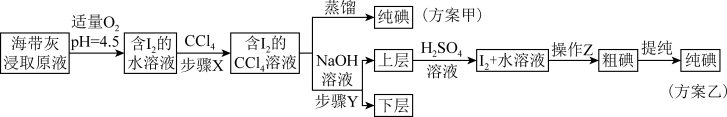
已知:3I2+6NaOH=5NaI+NaIO3+3H2O;酸性条件下,I2在水中的溶解度很小。
回答下列问题:
(1)灼烧海带实验用到的主要仪器有酒精灯、三脚架、泥三角、玻璃棒、___________ 等。
(2)“适量O2”也可以用双氧水替代,酸性条件下双氧水氧化碘离子的离子方程式为___________ 。
(3)上述方案乙中,“含I2的水溶液”经三步转化为含“I2+水溶液”,主要目的是___________ 。
(4)步骤X中,萃取后分液漏斗内观察到的现象是___________ 。
(5)下列有关步骤Y的说法中正确的是___________(填标号)
(6)方案甲中采用蒸馏分离效果不佳,原因是___________ ;方案乙中操作Z的名称是___________ 。

已知:3I2+6NaOH=5NaI+NaIO3+3H2O;酸性条件下,I2在水中的溶解度很小。
回答下列问题:
(1)灼烧海带实验用到的主要仪器有酒精灯、三脚架、泥三角、玻璃棒、
(2)“适量O2”也可以用双氧水替代,酸性条件下双氧水氧化碘离子的离子方程式为
(3)上述方案乙中,“含I2的水溶液”经三步转化为含“I2+水溶液”,主要目的是
(4)步骤X中,萃取后分液漏斗内观察到的现象是
(5)下列有关步骤Y的说法中正确的是___________(填标号)
| A.主要是除浸取原液中的有机杂质 |
| B.将碘转化成离子进入水层 |
| C.应控制NaOH溶液的浓度和体积 |
| D.NaOH溶液可由乙醇代替 |
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐3】高铁酸钾(K2FeO4)是一种多功能的新型水处理剂。一种湿法制备高铁酸钾的新工艺流程如图所示:
已知:高铁酸盐热稳定性差,在碱性环境中比酸性环境中相对稳定。回答以下问题:

(1)滤渣1的主要成分为(写化学式)_______ 。
(2)写出氧化过程的离子方程式_______ 。
(3)氧化时控温20~25℃,温度不能高于25℃原因是_______ 。
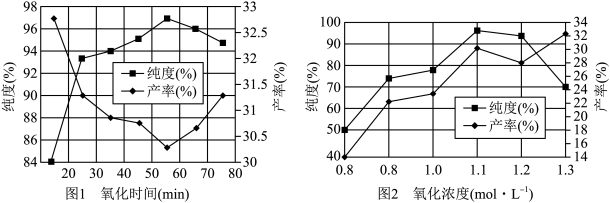
(4)实验测得氧化时间、氧化剂浓度与K2FeO4产率、纯度的实验数据分别如图l、图2所示。为了获取更纯的高铁酸钾,反应时间应控制在_______ min,氧化剂浓度应控制在_______  。
。
(5)高铁酸钾产品纯度测定方法如下(杂质不参与反应):在一定条件下,将1.32g样品与过量KI溶液反应后配成100mL溶液,每次取10.00mL用0.1000 的Na2S2O3标准溶液滴定,三次滴定消耗Na2S2O3标准溶液体积平均为19.20mL,则原样品中高铁酸钾的质量分数为
的Na2S2O3标准溶液滴定,三次滴定消耗Na2S2O3标准溶液体积平均为19.20mL,则原样品中高铁酸钾的质量分数为_______ 。(已知: ,
, )
)
已知:高铁酸盐热稳定性差,在碱性环境中比酸性环境中相对稳定。回答以下问题:

(1)滤渣1的主要成分为(写化学式)
(2)写出氧化过程的离子方程式
(3)氧化时控温20~25℃,温度不能高于25℃原因是
(4)实验测得氧化时间、氧化剂浓度与K2FeO4产率、纯度的实验数据分别如图l、图2所示。为了获取更纯的高铁酸钾,反应时间应控制在
 。
。
(5)高铁酸钾产品纯度测定方法如下(杂质不参与反应):在一定条件下,将1.32g样品与过量KI溶液反应后配成100mL溶液,每次取10.00mL用0.1000
 的Na2S2O3标准溶液滴定,三次滴定消耗Na2S2O3标准溶液体积平均为19.20mL,则原样品中高铁酸钾的质量分数为
的Na2S2O3标准溶液滴定,三次滴定消耗Na2S2O3标准溶液体积平均为19.20mL,则原样品中高铁酸钾的质量分数为 ,
, )
)
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐1】A、B均是前18号元素,已知A元素原子第三电子层上有6个电子,B元素与A元素的原子核外电子层数相同,B元素原子最外电子层上只有1个电子。试回答下列问题:
(1)写出两种元素的名称和符号A__________ B_________
(2)画出两种元素的原子的结构示意图为A_________ B_________
(3)A、B两元素形成的常见化合物的名称是_______________ ,此化合物中含有的化学键有__________ 。
(4)A的最高价氧化物对应水化物化学式__________ ,B的最高价氧化物对应水化物化学式__________ 。
(1)写出两种元素的名称和符号A
(2)画出两种元素的原子的结构示意图为A
(3)A、B两元素形成的常见化合物的名称是
(4)A的最高价氧化物对应水化物化学式
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐2】A、B、C、D、E五种短周期主族元素,原子序数依次增大,A的最外层电子数是次外层的3倍;A、D同主族,A、B的最外层电子数之和与E的最外层电子数相等,C是地壳中含量最多的金属元素。回答下列问题:
(1)D在元素周期表中的位置是______ ,E的离子结构示意图为______ 。
(2)A、B、C三种元素中,形成的简单离子的半径最小的是______ (填离子符号)。
(3)B、C、D、E形成的最高价氧化物对应的水化物中:
①酸性最强的是______ (用化学式填写)。
②C单质能与B的最高价氧化物的水化物溶液反应,其反应的化学方程式是:______ 。
(4)用电子式表示A和B形成B2A化合物的形成过程______ 。
(5)下列事实能说明E元素的非金属性比D元素的非金属性强的是______ 。
①最高价氧化物对应水化物的酸性:E>D
②E原子得到电子的数目比D原子少
③E元素的最高正价比D元素的最高正价要高
④元素的简单气态氢化物的稳定性:E>D
⑤气态氢化物溶于水后的酸性:E>D
(1)D在元素周期表中的位置是
(2)A、B、C三种元素中,形成的简单离子的半径最小的是
(3)B、C、D、E形成的最高价氧化物对应的水化物中:
①酸性最强的是
②C单质能与B的最高价氧化物的水化物溶液反应,其反应的化学方程式是:
(4)用电子式表示A和B形成B2A化合物的形成过程
(5)下列事实能说明E元素的非金属性比D元素的非金属性强的是
①最高价氧化物对应水化物的酸性:E>D
②E原子得到电子的数目比D原子少
③E元素的最高正价比D元素的最高正价要高
④元素的简单气态氢化物的稳定性:E>D
⑤气态氢化物溶于水后的酸性:E>D
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐3】Q、W、X、Y、Z为短周期元素,Q是原子半径最小的元素,W是地壳中含量最高的元素,X原子的质子数等于Z与Y的质子数之和: Z与Y位于同一周期, Y原子核外最外层电子比次外层多3个电子,非金属Z的一种固体单质可导电。回答下列问题:
(1)Y、 Z的元素名称分别为___________ 、___________ 。
(2)X在周期表中的位置是______________________ ,其离子结构示意图为___________ ;Y与Z之间形成的化学键属于___________ 。
(3)X、Y、Z三种元素原子半径由大到小的顺序为___________ (填元素符号);X单质既可与盐酸反应,又可溶于氢氧化钠溶液,写出X单质与氢氧化钠溶液反应的化学方程式 ___________ 。
(4)化合物X4Z3遇Q2W发生反应生成ZQ4, ZQ4的空间构型为___________ ,请完成该反应的化学方程式___________ 。
(1)Y、 Z的元素名称分别为
(2)X在周期表中的位置是
(3)X、Y、Z三种元素原子半径由大到小的顺序为
(4)化合物X4Z3遇Q2W发生反应生成ZQ4, ZQ4的空间构型为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐1】U、V、W、X、Y、Z是六种常见的前18号元素,且原子序数依次增大。已知U的一种核素的质量数为14,中子数为7;V的单核离子与 具有相同的质子、电子数目;W的电子层数与最外层电子数相等;X的最高正化合价和负化合价代数和为0;Y的最外层电子数是电子层数的2倍;Z的氢化物溶于水后形成的溶液是一种常见的强酸。请按要求回答下列问题:
具有相同的质子、电子数目;W的电子层数与最外层电子数相等;X的最高正化合价和负化合价代数和为0;Y的最外层电子数是电子层数的2倍;Z的氢化物溶于水后形成的溶液是一种常见的强酸。请按要求回答下列问题:
(1)W的正离子结构示意图:__________ ;X、Y、Z的原子半径由大到小依次为__________ ;X、Y的氧化物中共同存在的化学键类型是__________ 。
(2)化合物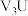 中正离子的电子式:
中正离子的电子式:__________ (填离子电子式); 的
的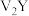 的电离方程式
的电离方程式__________ 。
 具有相同的质子、电子数目;W的电子层数与最外层电子数相等;X的最高正化合价和负化合价代数和为0;Y的最外层电子数是电子层数的2倍;Z的氢化物溶于水后形成的溶液是一种常见的强酸。请按要求回答下列问题:
具有相同的质子、电子数目;W的电子层数与最外层电子数相等;X的最高正化合价和负化合价代数和为0;Y的最外层电子数是电子层数的2倍;Z的氢化物溶于水后形成的溶液是一种常见的强酸。请按要求回答下列问题:(1)W的正离子结构示意图:
(2)化合物
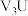 中正离子的电子式:
中正离子的电子式: 的
的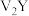 的电离方程式
的电离方程式
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
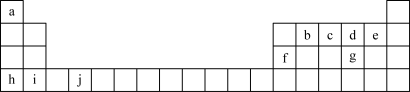
【推荐2】在1-18号的短周期主族元素中,表中的字母代表一种元素,回答下列问题:
(1)画出D的原子结构示意图________ ;
(2)A和F两种元素组成的化合物中含有的化学键是_____ (填“共价”或“离子”)键。;
(3)E和F分别形成的气态氢化物中最稳定的是_________ (填写氢化物的化学式)
(4)B的最高价氧化物的水化物的化学式_____________ 。
| A | |||||||||
| C | D | ||||||||
| B | E | F | |||||||
(2)A和F两种元素组成的化合物中含有的化学键是
(3)E和F分别形成的气态氢化物中最稳定的是
(4)B的最高价氧化物的水化物的化学式
您最近一年使用:0次

 的形成过程
的形成过程

