用下列实验装置进行的相应实验,不能达到实验目的的是
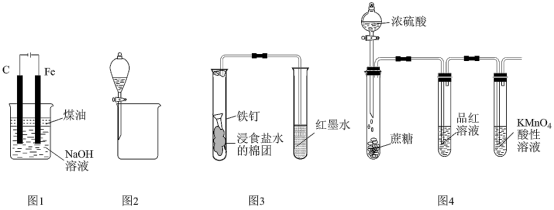

| A.图1所示装置可制备Fe(OH)2并能较长时间保持其颜色 |
| B.图2所示装置可分离CH3CH2OH和CH3COOC2H5混合液 |
| C.图3所示装置可用于观察铁的吸氧腐蚀 |
| D.图4所示装置可说明浓H2SO4具有脱水性、强氧化性,SO2具有漂白性、还原性 |
21-22高三上·湖南长沙·阶段练习 查看更多[6]
湖南省长沙市第一中学2021-2022学年高三上学期第五次月考化学试题(已下线)必刷卷04-2022年高考化学考前信息必刷卷(河北专用)(已下线)2022年北京高考真题变式题1-14湖南省株洲市第一中学2022-2023学年高三下学期开学考试化学试题(已下线)2022年北京高考真题化学试题变式题(选择题1-5)(已下线)2022年北京高考真题化学试题变式题(选择题1-5)
更新时间:2022-03-17 20:11:49
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】将6.4 g铜片和10 mL 18 mol·L-1的浓硫酸放在圆底烧瓶中共热,直到无气体生成,小李同学根据所学的化学知识认为还有一定量的硫酸剩余。为了定量或定性地分析剩余硫酸,下列实验方案设计可达到目的的是
| A.铁粉、氯化钡溶液和碳酸氢钠溶液均能够用来证明反应结束后的烧瓶中确有硫酸剩余 |
| B.为定量测定剩余硫酸浓度,可将产生的气体缓缓通过预先称量过的盛有碱石灰的干燥管,结束反应后再次称量,发现干燥管质量增加m1 g。 |
| C.为定量测定剩余硫酸浓度,将气体缓缓通入足量硝酸钡溶液中,然后过滤、洗涤、干燥,称得沉淀的质量为m2 g |
| D.为定量测定剩余硫酸浓度,分离出反应后的溶液(假定反应前后烧瓶中溶液的体积不变)并加蒸馏水稀释至1 000 mL,取20.00 mL于锥形瓶中,滴入2~3滴酚酞指示剂,用标准NaOH溶液进行滴定(已知氢氧化铜开始沉淀的pH约为5),可求出剩余硫酸的浓度 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】已知浓硫酸有强氧化性,沸点较高难挥发。溴为红棕色液体,但易挥发形成溴蒸气,碘为紫黑色固体。某小组比较Cl-、Br-、I-的还原性,实验如下表,下列对实验的分析不正确 的是
| 实验1 | 实验2 | 实验3 | |
| 装置 | 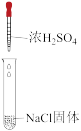 | 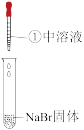 | 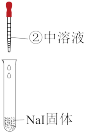 |
| 操作现象 | 微热后,溶液颜色无明显变化;试管口有白雾,经检验不能使湿润的淀粉碘化钾试纸变蓝(经检验无SO2气体) | 溶液变黄;试管口有红棕色气体生成 | 溶液变深紫色;试管口有紫色烟,能使湿润的淀粉碘化钾试纸变蓝 |
| A.实验1中可能生成了HCl气体 |
B.根据实验1和实验2能判断还原性: |
C.根据实验3能判断还原性: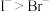 |
D.由上述3个实验可以比较出还原性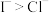 |
您最近一年使用:0次
【推荐1】能够使总反应 发生的是
发生的是
 发生的是
发生的是| A.铁片作原电池的负极,碳棒作原电池的正极,氯化钠作电解质溶液 |
| B.铁锌合金在潮湿空气中发生电化学腐蚀 |
| C.用铁片作阴、阳电极,电解氢氧化钠浴液 |
| D.用铁片作阴、阳电极,电解硫酸铜溶液 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】2,6-二氨基庚二酸(RH2)是1949年由科学家沃克(E.Work)从白喉棒杆菌的水解物中发现的一种氨基酸,对眼睛、呼吸道和皮肤有刺激作用,其结构简式为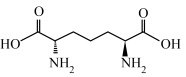 。其中一种三槽电渗析法制备2,6-二氨基庚二酸的装置工作原理如图所示(电极均为惰性电极)。下列说法
。其中一种三槽电渗析法制备2,6-二氨基庚二酸的装置工作原理如图所示(电极均为惰性电极)。下列说法不正确 的是
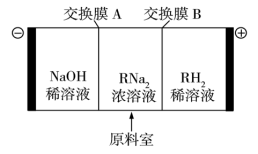
 。其中一种三槽电渗析法制备2,6-二氨基庚二酸的装置工作原理如图所示(电极均为惰性电极)。下列说法
。其中一种三槽电渗析法制备2,6-二氨基庚二酸的装置工作原理如图所示(电极均为惰性电极)。下列说法
| A.交换膜A为阳离子交换膜,B为阴离子交换膜 |
| B.装置工作一段时间后,阳极区可能生成氨基酸内盐类的结晶 |
| C.阴极反应式为2H2O+2e-=H2↑+2OH-,还可获得副产品氢氧化钠 |
| D.若用氢氧燃料电池作电源,当生成1 mol RH2时,电源的正极消耗气体11.2 L |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列关于金属腐蚀与防护的说法中正确的是( )
| A.牺牲阳极的阴极保护法是一种基于电解池原理的金属防护法 |
| B.钢铁的析氢腐蚀和吸氧腐蚀的负极反应式相同 |
| C.镀锌铁制品镀层受损后形成原电池,锌作负极,比破损前更耐腐蚀 |
| D.将变黑后的银器(表面被氧化为Ag2S)放入盛有食盐溶液的铝质容器中,黑色褪去是因为生成了AgCl |
您最近一年使用:0次
【推荐2】下列装置和操作不能达到实验目的的是
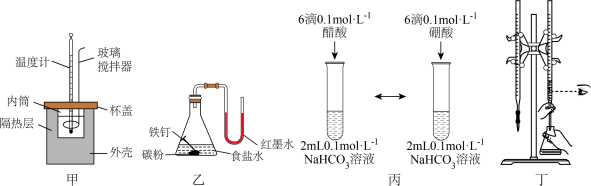

| A.甲装置:中和热的测定 |
| B.乙装置:验证铁的吸氧腐蚀 |
| C.丙装置:比较醋酸与硼酸的酸性强弱 |
| D.丁装置:用标准NaOH溶液滴定锥形瓶中的盐酸 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】鉴别甲苯、己烯、四氯化碳、乙醇、碘化钠五种无色溶液,应选用的一种试剂
| A.金属钠 | B.溴水 | C.银氨溶液 | D.高锰酸钾溶液 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
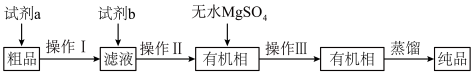
【推荐2】正丁醛经催化加氢可得到含少量正丁醛的1-丁醇粗品,为提纯1-丁醇设计如图路线。
②R-CHO+NaHSO3(饱和)→R-CH(OH)SO3Na↓。
下列说法错误的是
②R-CHO+NaHSO3(饱和)→R-CH(OH)SO3Na↓。
下列说法错误的是
| A.试剂a为饱和NaHSO3溶液,试剂b为乙醚 |
| B.操作I和操作III均为过滤 |
| C.无水MgSO4的作用是干燥除水 |
| D.蒸馏时冷却水应从球形冷凝管的上口进入 |
您最近一年使用:0次

 的原理如图所示。
的原理如图所示。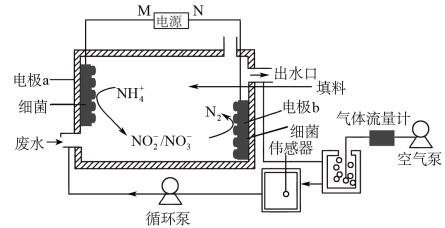
 +8H++8e-=N2↑+4H2O
+8H++8e-=N2↑+4H2O =3Cu2++2NO↑+4H2O
=3Cu2++2NO↑+4H2O Al(OH)3+3H+
Al(OH)3+3H+

