实验室用50mL浓盐酸跟足量的氯酸钾固体共热制取氯气,反应的化学方程式为(未配平)KClO3+HCl—KCl+Cl2↑+H2O。
(1)配平上述反应化学方程式:______ 。
(2)若产生0.1molCl2,则转移电子的物质的量为_______ mol。
(3)在该反应中,如有6molCl2生成,被氧化的HCl的物质的量是_____ mol,转移电子是______ mol。
(4)某温度下,将Cl2通入NaOH溶液中,反应得到含有ClO-与 物质的量之比为1∶1的混合液,反应的化学方程式是
物质的量之比为1∶1的混合液,反应的化学方程式是_____ 。
(5)报纸报道了多起卫生间清洗时,因混合使用“洁厕灵”(主要成分是盐酸)与“84消毒液”(主要成分是NaClO)发生氯气中毒的事件。试根据你的化学知识分析,原因是(用离子方程式表示)_____ 。
(1)配平上述反应化学方程式:
(2)若产生0.1molCl2,则转移电子的物质的量为
(3)在该反应中,如有6molCl2生成,被氧化的HCl的物质的量是
(4)某温度下,将Cl2通入NaOH溶液中,反应得到含有ClO-与
 物质的量之比为1∶1的混合液,反应的化学方程式是
物质的量之比为1∶1的混合液,反应的化学方程式是(5)报纸报道了多起卫生间清洗时,因混合使用“洁厕灵”(主要成分是盐酸)与“84消毒液”(主要成分是NaClO)发生氯气中毒的事件。试根据你的化学知识分析,原因是(用离子方程式表示)
更新时间:2022-03-22 20:34:12
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】工业及汽车尾气已成为城市空气的主要污染源,研究其反应机理对于环境治理有重要意义。
(1)硝酸厂尾气可以回收制备硝酸。已知:
①2NO(g)+O2(g)=2NO2(g) △H1=-113.0 kJ/mol
②3NO2(g)+H2O(g)=2HNO3(g)+NO(g) △H2=-138.0 kJ/mol
4NO2(g)+O2(g)+2H2O(g)=4HNO3(g) △H=___________ kJ/mol。
(2)液氨催化还原NO是重要的烟气脱硝技术。使用Fe2O3为催化剂,可能的反应过程如图所示。___________ 。
②反应过程图中,虚线方框里的过程可描述为___________ 。
③氨氮比会直接影响该方法的脱硝率。350℃时只改变氨气的投放量,NO的百分含量与氨氮比的关系如图所示。当 >1.0时,烟气中NO含量反而增大,主要原因是
>1.0时,烟气中NO含量反而增大,主要原因是___________ 。
NO2被Na2CO3溶液吸收生成的三种盐分别是NaNO2、NaNO3和___________ 。(填化学式)
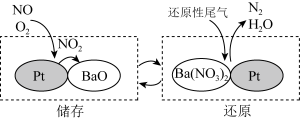
(4)NSR (NOX储存还原)可有效减少氮氧化物排放。工作原理:通过BaO和Ba(NO3)2的相互转化实现NOX的储存和还原,如图所示。___________ 。
(1)硝酸厂尾气可以回收制备硝酸。已知:
①2NO(g)+O2(g)=2NO2(g) △H1=-113.0 kJ/mol
②3NO2(g)+H2O(g)=2HNO3(g)+NO(g) △H2=-138.0 kJ/mol
4NO2(g)+O2(g)+2H2O(g)=4HNO3(g) △H=
(2)液氨催化还原NO是重要的烟气脱硝技术。使用Fe2O3为催化剂,可能的反应过程如图所示。
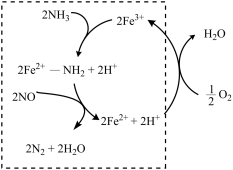
②反应过程图中,虚线方框里的过程可描述为
③氨氮比会直接影响该方法的脱硝率。350℃时只改变氨气的投放量,NO的百分含量与氨氮比的关系如图所示。当
 >1.0时,烟气中NO含量反而增大,主要原因是
>1.0时,烟气中NO含量反而增大,主要原因是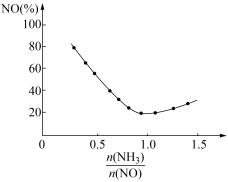
NO2被Na2CO3溶液吸收生成的三种盐分别是NaNO2、NaNO3和
(4)NSR (NOX储存还原)可有效减少氮氧化物排放。工作原理:通过BaO和Ba(NO3)2的相互转化实现NOX的储存和还原,如图所示。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】钠的化合物广泛应用于工业生产。
(1)氢化钠(NaH)中氢元素的化合价为___________ 。
(2)NaH能与水剧烈反应,反应方程式为 ,该反应中的氧化剂是
,该反应中的氧化剂是___________ ,NaH与液氨也有类似的反应,写出反应的化学方程式___________ 。
(3)在高温下氢化钠(NaH)可将四氯化钛( )还原成金属钛,写出该反应的化学方程式
)还原成金属钛,写出该反应的化学方程式___________ 。
(4)硼氢化钠( )与
)与 反应生成
反应生成 和
和 (已知反应过程中B的化合价不变)。写出该反应的化学方程式
(已知反应过程中B的化合价不变)。写出该反应的化学方程式___________ 。
(5)已知 在空气中完全燃烧,将燃烧产物全部通过足量的
在空气中完全燃烧,将燃烧产物全部通过足量的 ,则
,则 增加的质量是
增加的质量是___________ g。
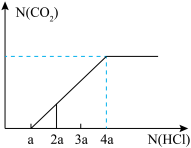
(6)现有由两种含钠化合物组成的混合物,溶于水后,逐滴加入某浓度盐酸,所得 的粒子数目与所耗HCl的粒子数目关系如图,两种含钠化合物的化学式和粒子数目之比为
的粒子数目与所耗HCl的粒子数目关系如图,两种含钠化合物的化学式和粒子数目之比为___________ 。
(1)氢化钠(NaH)中氢元素的化合价为
(2)NaH能与水剧烈反应,反应方程式为
 ,该反应中的氧化剂是
,该反应中的氧化剂是(3)在高温下氢化钠(NaH)可将四氯化钛(
 )还原成金属钛,写出该反应的化学方程式
)还原成金属钛,写出该反应的化学方程式(4)硼氢化钠(
 )与
)与 反应生成
反应生成 和
和 (已知反应过程中B的化合价不变)。写出该反应的化学方程式
(已知反应过程中B的化合价不变)。写出该反应的化学方程式(5)已知
 在空气中完全燃烧,将燃烧产物全部通过足量的
在空气中完全燃烧,将燃烧产物全部通过足量的 ,则
,则 增加的质量是
增加的质量是(6)现有由两种含钠化合物组成的混合物,溶于水后,逐滴加入某浓度盐酸,所得
 的粒子数目与所耗HCl的粒子数目关系如图,两种含钠化合物的化学式和粒子数目之比为
的粒子数目与所耗HCl的粒子数目关系如图,两种含钠化合物的化学式和粒子数目之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】新型冠状病毒肺炎爆发以来,各类杀菌消毒剂逐渐被人们所认识和使用。下列是我们常见的几种消毒剂:①“84”消毒液(有效成分NaClO);② (在水中一部分可以电离出阴、阳离子);③漂白粉;④
(在水中一部分可以电离出阴、阳离子);③漂白粉;④ ;⑤
;⑤ ;⑥碘酒;⑦75%酒精;⑧过氧乙酸(
;⑥碘酒;⑦75%酒精;⑧过氧乙酸(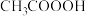 );⑨高铁酸钠(
);⑨高铁酸钠( )。回答下列问题:
)。回答下列问题:
(1)上述杀菌消毒剂属于电解质的是_______ (填序号),属于非电解质的是_______ (填序号),“84”消毒液中有效成分的电离方程式为_______ 。
(2)各类杀菌消毒剂使用时,必须严格按照使用说明。
①巴西奥运会期间,由于工作人员将“84”消毒液与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。一种可能原因是NaClO与 反应产生
反应产生 促进藻类快速生长。该反应说明氧化性:NaClO
促进藻类快速生长。该反应说明氧化性:NaClO_______  (填“>”或“<”)。
(填“>”或“<”)。
②若混合使用“洁厕灵”(盐酸是成分之一)与“84”消毒液会产生氯气。原因是_______ (用离子方程式表示)。
③漂白粉长时间露置在空气中会变质失效的原因是_______ (用两个化学方程式表示)。
(3)如图是一种“纳米药物分子运输车”,该技术可提高肿瘤的治疗效果。“纳米药物分子车”分散于水中所得的分散系属于_______ (填“溶液”“胶体”或“浊液”)。
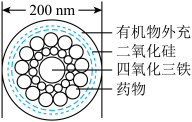
(4)高铁酸钠 是一种新型净水剂。高铁酸钠在水中可以发生如下反应并生成胶体:
是一种新型净水剂。高铁酸钠在水中可以发生如下反应并生成胶体: 。当反应转移电子的数目是
。当反应转移电子的数目是 时,生成标准状况下
时,生成标准状况下 的体积约为
的体积约为_______ 。用 代替
代替 处理饮用水的优点是
处理饮用水的优点是_______ (只答一条即可)。
 (在水中一部分可以电离出阴、阳离子);③漂白粉;④
(在水中一部分可以电离出阴、阳离子);③漂白粉;④ ;⑤
;⑤ ;⑥碘酒;⑦75%酒精;⑧过氧乙酸(
;⑥碘酒;⑦75%酒精;⑧过氧乙酸(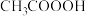 );⑨高铁酸钠(
);⑨高铁酸钠( )。回答下列问题:
)。回答下列问题:(1)上述杀菌消毒剂属于电解质的是
(2)各类杀菌消毒剂使用时,必须严格按照使用说明。
①巴西奥运会期间,由于工作人员将“84”消毒液与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。一种可能原因是NaClO与
 反应产生
反应产生 促进藻类快速生长。该反应说明氧化性:NaClO
促进藻类快速生长。该反应说明氧化性:NaClO (填“>”或“<”)。
(填“>”或“<”)。②若混合使用“洁厕灵”(盐酸是成分之一)与“84”消毒液会产生氯气。原因是
③漂白粉长时间露置在空气中会变质失效的原因是
(3)如图是一种“纳米药物分子运输车”,该技术可提高肿瘤的治疗效果。“纳米药物分子车”分散于水中所得的分散系属于

(4)高铁酸钠
 是一种新型净水剂。高铁酸钠在水中可以发生如下反应并生成胶体:
是一种新型净水剂。高铁酸钠在水中可以发生如下反应并生成胶体: 。当反应转移电子的数目是
。当反应转移电子的数目是 时,生成标准状况下
时,生成标准状况下 的体积约为
的体积约为 代替
代替 处理饮用水的优点是
处理饮用水的优点是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】已知常温常压下:① 3Cl2+2NH3→N2+6HCl ,②3Cl2+8NH3→N2+6NH4Cl
(1)完成并配平反应③的化学方程式,并标出电子转移方向和数目:
③ 3Cl2+4NH3→_______________________
(2)在反应③中:还原剂是_______ ,还原产物是__________ 。
(3)若按③反应后产生气体4.48 L(标准状况),则被氧化的气体的物质的量是___ mol。
(1)完成并配平反应③的化学方程式,并标出电子转移方向和数目:
③ 3Cl2+4NH3→
(2)在反应③中:还原剂是
(3)若按③反应后产生气体4.48 L(标准状况),则被氧化的气体的物质的量是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】铁有许多重要的化合物,除中学化学常见的三种氧化物和两种氢氧化物外,还有许多盐。 是一种浅绿色晶体,俗称绿矾,常用于处理含有氧化性离子的废水。现用绿矾对某工厂废水(含有强氧化性离子
是一种浅绿色晶体,俗称绿矾,常用于处理含有氧化性离子的废水。现用绿矾对某工厂废水(含有强氧化性离子 )进行处理。
)进行处理。
(1)绿矾除用铁粉与硫酸反应生成外,工业上还可用空气、水、黄铁矿(主要成分为 )来制取。已知该反应除生成硫酸亚铁,还生成一种中学化学常见的强酸,试写出该反应的化学方程式:
)来制取。已知该反应除生成硫酸亚铁,还生成一种中学化学常见的强酸,试写出该反应的化学方程式:___________ 。
(2)试配平:___________
___________Fe2++___________ +___________=___________Fe3++___________Cr3++___________H2O
+___________=___________Fe3++___________Cr3++___________H2O
 是一种浅绿色晶体,俗称绿矾,常用于处理含有氧化性离子的废水。现用绿矾对某工厂废水(含有强氧化性离子
是一种浅绿色晶体,俗称绿矾,常用于处理含有氧化性离子的废水。现用绿矾对某工厂废水(含有强氧化性离子 )进行处理。
)进行处理。(1)绿矾除用铁粉与硫酸反应生成外,工业上还可用空气、水、黄铁矿(主要成分为
 )来制取。已知该反应除生成硫酸亚铁,还生成一种中学化学常见的强酸,试写出该反应的化学方程式:
)来制取。已知该反应除生成硫酸亚铁,还生成一种中学化学常见的强酸,试写出该反应的化学方程式:(2)试配平:
___________Fe2++___________
 +___________=___________Fe3++___________Cr3++___________H2O
+___________=___________Fe3++___________Cr3++___________H2O
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】根据条件书写化学反应方程式。
(1)工业上从碳酸氢铵和镁硼石[Mg2B2O4(OH)2]在水溶液中反应制备硼酸______ 。
(2)从乏燃料提取钚元素的过程中,利用亚硝酸钠在强酸溶液中将 Pu3+氧化为 Pu4+_____ 。
(3)NaBH4 与氯化镍(摩尔比 2:1)在水溶液中反应,可得到两种硼化物:硼化镍和硼酸(摩尔比 1:3)_____ 。
(4)通过 KMnO4和H2O2在KF-HF质中反应获得化学法制 F2 的原料 K2MnF6_____
(5)磷化氢与甲醛的硫酸溶液反应,产物仅为硫酸鏻(盐)_____ 。
(1)工业上从碳酸氢铵和镁硼石[Mg2B2O4(OH)2]在水溶液中反应制备硼酸
(2)从乏燃料提取钚元素的过程中,利用亚硝酸钠在强酸溶液中将 Pu3+氧化为 Pu4+
(3)NaBH4 与氯化镍(摩尔比 2:1)在水溶液中反应,可得到两种硼化物:硼化镍和硼酸(摩尔比 1:3)
(4)通过 KMnO4和H2O2在KF-HF质中反应获得化学法制 F2 的原料 K2MnF6
(5)磷化氢与甲醛的硫酸溶液反应,产物仅为硫酸鏻(盐)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】从化合价和物质类别两个视角认识元素及其化合物性质是重要的化学学习方式。图1是 及其化合物的化合价—物质类别二维图。
及其化合物的化合价—物质类别二维图。
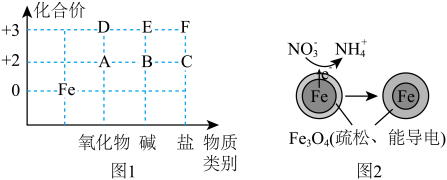
回答下列问题:
(1)工业上冶炼 常用的方法是
常用的方法是_______ (填字母)。
a.电解法 b.还原法 c.热分解法 d.物理方法
(2)若图1中的F为硫酸盐,请写出由D生成F的离子方程式:_______ 。
(3)图1中的B在潮湿的空气中很容易发生化合反应变成E,该反应的化学方程式为_______ 。
(4)图1中的F与C在水溶液中转化的离子反应有: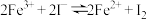 ,为了探究该反应存在一定的限度,某化学兴趣小组取
,为了探究该反应存在一定的限度,某化学兴趣小组取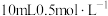 的
的 溶液于试管中,再加入
溶液于试管中,再加入 的
的 溶液,振荡,使试管中的物质充分反应一段时间。为了达到实验目的,还需要再向试管中加入下列试剂中的_______(填字母)。
溶液,振荡,使试管中的物质充分反应一段时间。为了达到实验目的,还需要再向试管中加入下列试剂中的_______(填字母)。
(5)用 可以去除水体中的
可以去除水体中的 (原理如图2)。若有
(原理如图2)。若有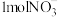 转化为
转化为 ,则参加反应的
,则参加反应的 失去的电子的物质的量为
失去的电子的物质的量为_______  。
。
 及其化合物的化合价—物质类别二维图。
及其化合物的化合价—物质类别二维图。
回答下列问题:
(1)工业上冶炼
 常用的方法是
常用的方法是a.电解法 b.还原法 c.热分解法 d.物理方法
(2)若图1中的F为硫酸盐,请写出由D生成F的离子方程式:
(3)图1中的B在潮湿的空气中很容易发生化合反应变成E,该反应的化学方程式为
(4)图1中的F与C在水溶液中转化的离子反应有:
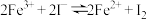 ,为了探究该反应存在一定的限度,某化学兴趣小组取
,为了探究该反应存在一定的限度,某化学兴趣小组取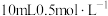 的
的 溶液于试管中,再加入
溶液于试管中,再加入 的
的 溶液,振荡,使试管中的物质充分反应一段时间。为了达到实验目的,还需要再向试管中加入下列试剂中的_______(填字母)。
溶液,振荡,使试管中的物质充分反应一段时间。为了达到实验目的,还需要再向试管中加入下列试剂中的_______(填字母)。| A.淀粉溶液 | B. 溶液 溶液 | C. | D.酸性高锰酸钾溶液 |
 可以去除水体中的
可以去除水体中的 (原理如图2)。若有
(原理如图2)。若有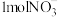 转化为
转化为 ,则参加反应的
,则参加反应的 失去的电子的物质的量为
失去的电子的物质的量为 。
。
您最近一年使用:0次
【推荐2】氢氧化氧镍(NiOOH)有良好的电化学活性,是合成锂离子电池材料的前驱体。某化工厂用含镍废料(主要成分为NiO,杂质为 、CaO、CuO)制备NiOOH的工艺流程如图。
、CaO、CuO)制备NiOOH的工艺流程如图。

已知几种金属离子沉淀的pH如表:
(1)为了提高“酸浸”中原料的浸出效率,采取的措施不合理的有_______。
(2)料渣1的主要成分是_______ (填化学式)。
(3)“除铜”中发生两个反应,写出其中生成CuS的化学方程式_______ 。
(4)“除铁”在40~50°C下进行,加入 的作用是
的作用是_______ , 的实际消耗量比理论值高的原因是
的实际消耗量比理论值高的原因是_______ ,NaOH用于调节溶液的pH,应调节pH的范围是_______ 。
(5)NiOOH中Ni的化合价为_______ 。“氧化”中会有 生成,反应的离子方程式为
生成,反应的离子方程式为_______ 。
(6)若用2.0t废料(含NiO75%)制得NiOOH 1.6t,则NiOOH的产率为_______ %(保留两位有效数字)。
 、CaO、CuO)制备NiOOH的工艺流程如图。
、CaO、CuO)制备NiOOH的工艺流程如图。
已知几种金属离子沉淀的pH如表:
| 金属离子 |  |  |  |
| 开始沉淀的pH | 1.5 | 6.5 | 7.2 |
| 沉淀完全的pH | 3.2 | 9.7 | 9.2 |
| A.研磨废料 | B.加入大量水 | C.搅拌 | D.适当升高温度 |
(3)“除铜”中发生两个反应,写出其中生成CuS的化学方程式
(4)“除铁”在40~50°C下进行,加入
 的作用是
的作用是 的实际消耗量比理论值高的原因是
的实际消耗量比理论值高的原因是(5)NiOOH中Ni的化合价为
 生成,反应的离子方程式为
生成,反应的离子方程式为(6)若用2.0t废料(含NiO75%)制得NiOOH 1.6t,则NiOOH的产率为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】按要求回答下列问题:
(l)已知反应H2S + 2HNO3(浓)=3S↓+ 2NO2+2H2O,该反应的还原剂是_______ ,氧化产物是____ ,生成16gS转移的电子数为____ 。
(2)Cu2S(Cu显+1价)与一定浓度的HNO3反应生成Cu(NO3)2、CuSO4、NO和H2O,反应的化学方程式为____ 。
(3)Na2Sx在碱性溶液中可被NaClO氧化为Na2SO4,而NaClO被还原为NaCl,若反应中Na2Sx与NaClO的物质的量之比为1:16,则x的值为____ 。
(l)已知反应H2S + 2HNO3(浓)=3S↓+ 2NO2+2H2O,该反应的还原剂是
(2)Cu2S(Cu显+1价)与一定浓度的HNO3反应生成Cu(NO3)2、CuSO4、NO和H2O,反应的化学方程式为
(3)Na2Sx在碱性溶液中可被NaClO氧化为Na2SO4,而NaClO被还原为NaCl,若反应中Na2Sx与NaClO的物质的量之比为1:16,则x的值为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】根据反应8NH3+3Cl2=6NH4Cl+N2,回答下列问题:
(1)氧化剂_____ ,还原剂_____ ;
(2)反应中转移电子数是_____ ;
(3)氧化剂与氧化产物的质量比_____ ;
(4)当生成2.8gN2时,被氧化的物质的质量是____ g。
(1)氧化剂
(2)反应中转移电子数是
(3)氧化剂与氧化产物的质量比
(4)当生成2.8gN2时,被氧化的物质的质量是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】为治理汽车尾气中的NO和CO对环境的污染,可在汽车排气管上安装催化转化器,发生的反应为2NO + 2CO  N2 + 2CO2。该反应中,作为氧化剂的物质是
N2 + 2CO2。该反应中,作为氧化剂的物质是_____ (填化学式);若反应中生成1 mol N2,则消耗标况下NO 的体积是________ L。
 N2 + 2CO2。该反应中,作为氧化剂的物质是
N2 + 2CO2。该反应中,作为氧化剂的物质是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】亚硝酸钠(NaNO2)是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒。亚硝酸钠加热到320℃以上会分解产生Na2O、N2和O2,其水溶液呈碱性,能与AgNO3溶液反应生成难溶于水、易溶于酸的AgNO2。由于NaNO2有毒性,将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。
(1)从物质分类角度来看,NaNO2是_______ (填字母代号)。
a.酸 b.碱 c.盐 d.氧化物 e.非电解质 f.电解质
(2)下列方法能用来区分固体NaNO2和NaCl的是_______(填序号)。
(3)误食NaNO2会导致人体血红蛋白中的Fe2+转化为Fe3+而中毒,该过程中NaNO2表现出的性质与下列_______(填序号)反应中H2O2表现出的性质相同。
(4)小铭通过查阅资料,可用NO制备NaNO2:2NO+Na2O2=2NaNO2.实验室制备NO的反应为:3Cu + 8HNO3=3Cu(NO3)2 + 2NO↑ + 4H2O,该反应中氧化剂是_______ ,氧化产物是_______ ;若有3.0g NO生成,有_______ mol HNO3被还原。
(1)从物质分类角度来看,NaNO2是
a.酸 b.碱 c.盐 d.氧化物 e.非电解质 f.电解质
(2)下列方法能用来区分固体NaNO2和NaCl的是_______(填序号)。
| A.分别溶于水 |
| B.分别溶于水并滴加HNO3酸化的AgNO3溶液 |
| C.分别加强热并收集气体检验 |
| D.用筷子分别蘸取固体品尝味道 |
A. |
B. |
C.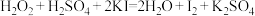 |
D. |
您最近一年使用:0次



