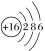为纪念元素周期表诞生150周年,IUPAC等向世界介绍118位优秀青年化学家,并形成一张“青年化学家元素周期表”。中国学者雷晓光、姜雪峰、刘庄分别成为“N、S、Hg”元素的代言人。回答下列问题:
(1)据汞的原子结构示意图 ,汞在第
,汞在第_______ 周期。
(2)①叠氮化钠(NaN3)可用于汽车安全气囊的产气药,NaN3在撞击时能发生分解反应生成两种单质。计算理论上65 gNaN3完全分解,释放出标准状况下的气体体积_______ L。
②氮化铝(AlN)具有耐高温、抗冲击、导热性好等优良性质,工业将氧化铝、氮气和碳在一定条件下反应制得AlN和CO,请将下列的化学反应方程式配平。_______
_______Al2O3+_______N2+_______C—______AlN+_______CO
(3)利用元素的化合价推测物质的性质是化学研究的重要于段。如图是硫元素的“价—类”二维图:

①从硫元素化合价变化的角度分析,图中既有氧化性又有还原性的化合物有_______ (填化学式)。
②Z的浓溶液与铁单质在加热条件下可以发生化学反应生成Y,该反应的化学方程式为_______ 。
(1)据汞的原子结构示意图
 ,汞在第
,汞在第(2)①叠氮化钠(NaN3)可用于汽车安全气囊的产气药,NaN3在撞击时能发生分解反应生成两种单质。计算理论上65 gNaN3完全分解,释放出标准状况下的气体体积
②氮化铝(AlN)具有耐高温、抗冲击、导热性好等优良性质,工业将氧化铝、氮气和碳在一定条件下反应制得AlN和CO,请将下列的化学反应方程式配平。
_______Al2O3+_______N2+_______C—______AlN+_______CO
(3)利用元素的化合价推测物质的性质是化学研究的重要于段。如图是硫元素的“价—类”二维图:

①从硫元素化合价变化的角度分析,图中既有氧化性又有还原性的化合物有
②Z的浓溶液与铁单质在加热条件下可以发生化学反应生成Y,该反应的化学方程式为
更新时间:2022-04-20 11:52:33
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】根据所学知识填空(NA表示阿伏加德罗常数):
(1)0.2molCl2含有___ molCl,在标准状况下体积为___ L。
(2)1.204×1022个CO2分子,含O的质量为___ 。
(3)1molOH-中含有__ mol电子,有___ 个质子。
(4)28g14N2所含的原子数为___ NA,中子数为___ NA。
(5)同温同压下,12C18O和14N2两种气体的密度之比为__ 。
(6)同温同压下,同体积的N2和SO2分子数之比为___ ,物质的量之比为___ ,质量之比为___ 。
(1)0.2molCl2含有
(2)1.204×1022个CO2分子,含O的质量为
(3)1molOH-中含有
(4)28g14N2所含的原子数为
(5)同温同压下,12C18O和14N2两种气体的密度之比为
(6)同温同压下,同体积的N2和SO2分子数之比为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】根据所学知识,回答下列问题:
(1)自来水厂用氯气杀菌、消毒,其消毒原理主要是氯气溶于水后生成了HClO,写出HClO的电子式:_____ 。
(2)6.0g氮的氧化物NOx中,含N物质的量为0.2mol,则NOx的摩尔质量为_____ 。
(3)已知反应:3Cu+8HNO3(浓)=3Cu(NO3)2+2NO↑+4H2O(稀)。若有64gCu被氧化,则被还原的HNO3的物质的量是_____ 。
(4)ClO2是一种黄绿色气体,被称为“第四代”饮用水消毒剂。制备ClO2的一种方法为在平底烧瓶中加入KClO3固体、足量草酸(H2C2O4)、稀硫酸,60℃~80℃水浴加热。该反应的化学方程式为_____ 。
(1)自来水厂用氯气杀菌、消毒,其消毒原理主要是氯气溶于水后生成了HClO,写出HClO的电子式:
(2)6.0g氮的氧化物NOx中,含N物质的量为0.2mol,则NOx的摩尔质量为
(3)已知反应:3Cu+8HNO3(浓)=3Cu(NO3)2+2NO↑+4H2O(稀)。若有64gCu被氧化,则被还原的HNO3的物质的量是
(4)ClO2是一种黄绿色气体,被称为“第四代”饮用水消毒剂。制备ClO2的一种方法为在平底烧瓶中加入KClO3固体、足量草酸(H2C2O4)、稀硫酸,60℃~80℃水浴加热。该反应的化学方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】(1)在标准状况下,CO和CO2的混合气体共8.96L,质量为12.8g,则两种气体的物质的量之和为___ mol,其中CO2为___ mol,CO占总体积的___ ,混合气体的摩尔质量为____ 。
(2)同温同压下,同体积的甲烷(CH4)和二氧化碳分子数之比为____ ,物质的量之比为___ ,原子总数之比为____ ,质量之比为___ ,密度之比为____ 。
(3)在标准状况下,4g H2、11.2L O2、1mol H2O中,所含分子数最多的是___ ,含原子数最多的是____ ,质量最大的是____ ,体积最小的是___ 。
(2)同温同压下,同体积的甲烷(CH4)和二氧化碳分子数之比为
(3)在标准状况下,4g H2、11.2L O2、1mol H2O中,所含分子数最多的是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】过氧化氢是用途很广的绿色氧化剂,它的水溶液俗称双氧水,常用于消毒、杀菌、漂白等。试回答下列问题:
(1)写出酸性高锰酸钾和H2O2反应的离子方程式___ 。
(2)Na2O2、K2O2以及BaO2都可与酸作用生成过氧化氢,目前实验室制取过氧化氢可通过上述某种过氧化物与适量稀硫酸作用,然后过滤。则上述最适合的过氧化物是___ 。
(3)甲酸钙[Ca(HCOO)2]广泛用于食品工业生产上,实验室制取甲酸钙的方法之一是将氢氧化钙和甲醛 溶液加入质量分数为30%~70%的过氧化氢溶液中,则该反应的化学方程式为
溶液加入质量分数为30%~70%的过氧化氢溶液中,则该反应的化学方程式为___ 。
(1)写出酸性高锰酸钾和H2O2反应的离子方程式
(2)Na2O2、K2O2以及BaO2都可与酸作用生成过氧化氢,目前实验室制取过氧化氢可通过上述某种过氧化物与适量稀硫酸作用,然后过滤。则上述最适合的过氧化物是
(3)甲酸钙[Ca(HCOO)2]广泛用于食品工业生产上,实验室制取甲酸钙的方法之一是将氢氧化钙和甲醛
 溶液加入质量分数为30%~70%的过氧化氢溶液中,则该反应的化学方程式为
溶液加入质量分数为30%~70%的过氧化氢溶液中,则该反应的化学方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】NaCN超标的电镀废水可用两段氧化法处理:
第一次:NaCN与NaClO反应,生成NaOCN和NaCl;
第二次:NaOCN与NaClO反应,生成Na2CO3.CO2.NaCl和N2。
已知HCN是一种有剧毒的挥发性弱酸;HCN.HOCN中N元素化合价相同。
完成下列填空:
(1)HCN是直线型分子,HCN是_____ 分子(选填“极性”、“非极性”)。HClO的电子式为_______ 。
(2)上述反应涉及到的元素中,氯原子核外电子能量最高的电子亚层是_______ ;H、C、N、O、Na的原子半径从小到大的顺序为_________ 。
(3)第一次氧化时,溶液的pH应调节为_______ (选填“酸性”、“碱性”或“中性”);原因是_______ 。
(4)写出第二次氧化时发生反应的离子方程式:_________ 。
(5)处理100m3含NaCN10.3mg/L的废水,实际至少需NaClO_______ g(实际用量应为理论值的4倍),才能使NaCN含量低于0.5mg/L,达到排放标准。
第一次:NaCN与NaClO反应,生成NaOCN和NaCl;
第二次:NaOCN与NaClO反应,生成Na2CO3.CO2.NaCl和N2。
已知HCN是一种有剧毒的挥发性弱酸;HCN.HOCN中N元素化合价相同。
完成下列填空:
(1)HCN是直线型分子,HCN是
(2)上述反应涉及到的元素中,氯原子核外电子能量最高的电子亚层是
(3)第一次氧化时,溶液的pH应调节为
(4)写出第二次氧化时发生反应的离子方程式:
(5)处理100m3含NaCN10.3mg/L的废水,实际至少需NaClO
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】“绿水青山就是金山银山”。近年来,绿色发展、生态保护成为中国展示给世界的一张新“名片”。
(1)硫酸工业排出的废气(主要含 )有多种处理方式。
)有多种处理方式。
①写出用过量氨水吸收废气的离子方程式:___________ 。
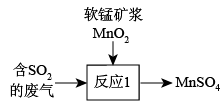
②废气也可用软锰矿浆( )吸收,写出如图所示“反应1”的化学方程式:
)吸收,写出如图所示“反应1”的化学方程式:______ 。
(2)治理汽车尾气中 和
和 的方法之一是在汽车的排气管上装一个催化转化装置,使
的方法之一是在汽车的排气管上装一个催化转化装置,使 和
和 在催化剂的作用下转化为无毒物质。写出该反应的化学方程式:
在催化剂的作用下转化为无毒物质。写出该反应的化学方程式:___________ 。
(3)某工厂拟综合处理含 的废水和工业废气(主要含
的废水和工业废气(主要含 、
、 、
、 ),设计了如图所示流程:
),设计了如图所示流程:
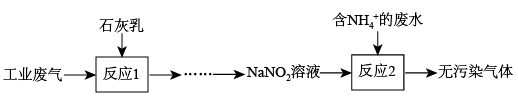
①“反应1”用于吸收 ,“反应1”的化学方程式为
,“反应1”的化学方程式为___________ 。
②“反应2”的离子方程式为___________ 。
(4)为实现燃煤脱硫,向煤中加入浆状 ,使燃料燃烧产生的
,使燃料燃烧产生的 转化为稳定的含镁化合物,写出该反应的化学方程式:
转化为稳定的含镁化合物,写出该反应的化学方程式:___________ 。
(1)硫酸工业排出的废气(主要含
 )有多种处理方式。
)有多种处理方式。①写出用过量氨水吸收废气的离子方程式:
②废气也可用软锰矿浆(
 )吸收,写出如图所示“反应1”的化学方程式:
)吸收,写出如图所示“反应1”的化学方程式:
(2)治理汽车尾气中
 和
和 的方法之一是在汽车的排气管上装一个催化转化装置,使
的方法之一是在汽车的排气管上装一个催化转化装置,使 和
和 在催化剂的作用下转化为无毒物质。写出该反应的化学方程式:
在催化剂的作用下转化为无毒物质。写出该反应的化学方程式:(3)某工厂拟综合处理含
 的废水和工业废气(主要含
的废水和工业废气(主要含 、
、 、
、 ),设计了如图所示流程:
),设计了如图所示流程:
①“反应1”用于吸收
 ,“反应1”的化学方程式为
,“反应1”的化学方程式为②“反应2”的离子方程式为
(4)为实现燃煤脱硫,向煤中加入浆状
 ,使燃料燃烧产生的
,使燃料燃烧产生的 转化为稳定的含镁化合物,写出该反应的化学方程式:
转化为稳定的含镁化合物,写出该反应的化学方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】浓H2SO4具有①酸性;②强氧化性;③吸水性;④脱水性等性质,根据题意填空(填序号):
(1)将浓硫酸滴到滤纸上,滤纸变黑,是因为浓硫酸具有__________ ;
(2)浓H2SO4与木炭共热生成二氧化碳、二氧化硫和水,该反应体现了浓H2SO4的__________ 。
(3)盛有浓硫酸的烧杯敞口放置一段时间后,质量增加.是因为浓硫酸具有__________ 。
(1)将浓硫酸滴到滤纸上,滤纸变黑,是因为浓硫酸具有
(2)浓H2SO4与木炭共热生成二氧化碳、二氧化硫和水,该反应体现了浓H2SO4的
(3)盛有浓硫酸的烧杯敞口放置一段时间后,质量增加.是因为浓硫酸具有
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】非金属元素在生产生活中扮演着重要角色。请根据题意填空:
(1)浓硫酸是一种重要的化工原料,在浓硫酸的运输过程中,可选择___________ (填“铁”或“铜”)作为罐体材料。
(2)浓硫酸能使蔗糖变黑,体现出的性质为___________ (填“吸水性”或“脱水性”或“氧化性”),并膨胀、产生大量CO2、SO2气体,可用___________ (填“品红溶液”或“石蕊溶液”或“澄清石灰水”)检验SO2。
(1)浓硫酸是一种重要的化工原料,在浓硫酸的运输过程中,可选择
(2)浓硫酸能使蔗糖变黑,体现出的性质为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】运用元素周期律和元素周期表,可以系统研究元素的性质。回答下列问题:
(1)碱金属元素中,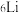 和
和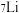 之间的关系是互为
之间的关系是互为_______ 。金属钾的氧化物有多种,其中过氧化钾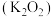 常作供氧剂,写出
常作供氧剂,写出 与
与 反应的化学方程式:
反应的化学方程式:_______ 。
(2)门捷列夫预言的“类硅”,后被发现,并命名为锗(Ge),周期表中排在硅的下一行。加上之前发现的碳(C)、铅(Pb)、锡(Sn),这一主族的元素趋于完善。
①锗在元素周期表中的位置是_______ ,根据锗在周期表中处于金属和非金属分界线附近,预测锗单质的一种用途是_______ 。
②硅和锗单质分别与 反应生成的氢化物更稳定的是
反应生成的氢化物更稳定的是_______ (填“硅”或“锗”)。
(1)碱金属元素中,
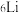 和
和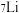 之间的关系是互为
之间的关系是互为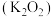 常作供氧剂,写出
常作供氧剂,写出 与
与 反应的化学方程式:
反应的化学方程式:(2)门捷列夫预言的“类硅”,后被发现,并命名为锗(Ge),周期表中排在硅的下一行。加上之前发现的碳(C)、铅(Pb)、锡(Sn),这一主族的元素趋于完善。
①锗在元素周期表中的位置是
②硅和锗单质分别与
 反应生成的氢化物更稳定的是
反应生成的氢化物更稳定的是
您最近一年使用:0次