运用元素周期律和元素周期表,可以系统研究元素的性质。回答下列问题:
(1)碱金属元素中,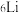 和
和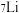 之间的关系是互为
之间的关系是互为_______ 。金属钾的氧化物有多种,其中过氧化钾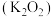 常作供氧剂,写出
常作供氧剂,写出 与
与 反应的化学方程式:
反应的化学方程式:_______ 。
(2)门捷列夫预言的“类硅”,后被发现,并命名为锗(Ge),周期表中排在硅的下一行。加上之前发现的碳(C)、铅(Pb)、锡(Sn),这一主族的元素趋于完善。
①锗在元素周期表中的位置是_______ ,根据锗在周期表中处于金属和非金属分界线附近,预测锗单质的一种用途是_______ 。
②硅和锗单质分别与 反应生成的氢化物更稳定的是
反应生成的氢化物更稳定的是_______ (填“硅”或“锗”)。
(1)碱金属元素中,
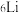 和
和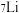 之间的关系是互为
之间的关系是互为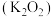 常作供氧剂,写出
常作供氧剂,写出 与
与 反应的化学方程式:
反应的化学方程式:(2)门捷列夫预言的“类硅”,后被发现,并命名为锗(Ge),周期表中排在硅的下一行。加上之前发现的碳(C)、铅(Pb)、锡(Sn),这一主族的元素趋于完善。
①锗在元素周期表中的位置是
②硅和锗单质分别与
 反应生成的氢化物更稳定的是
反应生成的氢化物更稳定的是
更新时间:2022-05-13 19:17:14
|
相似题推荐
【推荐1】根据物质结构有关性质和特点,回答下列问题:
(1)钴位于元素周期表的___________ 。
(2)基态铝原子核外电子云轮廓图的形状有(填名称)___________ 。
(3)2020年新冠肺炎疫情席卷全球,酒精(CH3CH2OH)成为家庭必备品,乙醇分子中碳原子轨道的杂化类型是___________ 。
(4)[Fe(H2NCONH2)]6(NO3)3的名称是三硝酸六尿素合铁(III),是一种重要的配合物。该化合物中,所含非金属元素C的最高价氧化物的电子式为___________ ;Fe3+比Fe2+更稳定的原因___________ 。
(5)Co(NH3)5BrSO4可形成两种钴的配合物,结构分别为[Co(NH3)5Br]SO4和[Co(SO4)(NH3)5]Br。已知Co3+的配位数为6,为确定钴的配合物的结构,现对两种配合物进行如下实验:在第一种配合物溶液中加入硝酸银溶液产生白色沉淀,在第二种配合物溶液中加入硝酸银溶液产生淡黄色沉淀。则第二种配合物的配体为___________ 。
(6)高温超导材料镧钡铜氧化物中含有Cu3+。基态时Cu3+的电子排布式为___________ ;
(1)钴位于元素周期表的
(2)基态铝原子核外电子云轮廓图的形状有(填名称)
(3)2020年新冠肺炎疫情席卷全球,酒精(CH3CH2OH)成为家庭必备品,乙醇分子中碳原子轨道的杂化类型是
(4)[Fe(H2NCONH2)]6(NO3)3的名称是三硝酸六尿素合铁(III),是一种重要的配合物。该化合物中,所含非金属元素C的最高价氧化物的电子式为
(5)Co(NH3)5BrSO4可形成两种钴的配合物,结构分别为[Co(NH3)5Br]SO4和[Co(SO4)(NH3)5]Br。已知Co3+的配位数为6,为确定钴的配合物的结构,现对两种配合物进行如下实验:在第一种配合物溶液中加入硝酸银溶液产生白色沉淀,在第二种配合物溶液中加入硝酸银溶液产生淡黄色沉淀。则第二种配合物的配体为
(6)高温超导材料镧钡铜氧化物中含有Cu3+。基态时Cu3+的电子排布式为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】请完成下列空白:
铁元素位于元素周期表的第___________ 周期第___________ 族,属于___________ 区。
| 表示方法 |  |  |
| 原子(或离子)结构示意图 | ||
| 电子排布式 | ||
| 价电子轨道表示式 |
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】我国科学家成功合成了含N 的五氮阴离子盐,这是全氮含能材料研究领域中里程碑式的突破。
的五氮阴离子盐,这是全氮含能材料研究领域中里程碑式的突破。
(1)N在元素周期表中的位置是___________ 。
(2)N 中,N原子之间的相互作用是
中,N原子之间的相互作用是___________ (填“离子键”或“共价键”)。
(3)非金属性O强于N,用原子结构解释原因:___________ ,得电子能力O大于N。
(4)磷(P)与氮位于同一主族,下列推断正确的是___________ (填序号)。
①磷元素的最低负化合价为−3价
②热稳定性:PH3>NH3
③磷的最高价氧化物对应的水化物属于酸
 的五氮阴离子盐,这是全氮含能材料研究领域中里程碑式的突破。
的五氮阴离子盐,这是全氮含能材料研究领域中里程碑式的突破。(1)N在元素周期表中的位置是
(2)N
 中,N原子之间的相互作用是
中,N原子之间的相互作用是(3)非金属性O强于N,用原子结构解释原因:
(4)磷(P)与氮位于同一主族,下列推断正确的是
①磷元素的最低负化合价为−3价
②热稳定性:PH3>NH3
③磷的最高价氧化物对应的水化物属于酸
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】元素在周期表中的位置,反映了元素的原子结构和元素的性质。下图是元素周期表的一部分。请用元素符号或化学式填空:

(1)所示元素中
①非金属性最强的元素是:_________
②金属性最强的元素是:___________
③原子半径最小的是:___________
④最高价含氧酸酸性最强的是______________
⑤经常用作半导体材料的元素是:___________ (只写一种)
⑥阴影部分属于元素周期表中的_________ 族,该族元素的最高正价均为_________
(2)根据元素周期律,推导:
①酸性强弱: H3AsO4_________ H3PO4(用“>”或“<”表示,下同);
②稳定性:H2S__________ HCl
③沸点:HF_____ HCl
④还原性:I-_______ Br-
⑤在O、F、S、Cl四种元素中,非金属性最接近的是:__________
A.O和F B.F和S C.S和Cl D.O和Cl
(3)根据同主族元素性质的相似性和递变性进行预测:
①关于Se的预测正确的是:________
A.常温下Se单质是气体
B. Se最高价氧化物的水化物能和NaOH发生反应
C. 氢化物的化学式为H2Se
D. 常见的氧化物只有SeO3
②已知Cl2在水溶液中能和SO2反应,Cl2+2H2O+SO2==H2SO4+2HCl,写出Br2在水溶液中和SO2反应的离子反应方程式___________________________________

(1)所示元素中
①非金属性最强的元素是:
②金属性最强的元素是:
③原子半径最小的是:
④最高价含氧酸酸性最强的是
⑤经常用作半导体材料的元素是:
⑥阴影部分属于元素周期表中的
(2)根据元素周期律,推导:
①酸性强弱: H3AsO4
②稳定性:H2S
③沸点:HF
④还原性:I-
⑤在O、F、S、Cl四种元素中,非金属性最接近的是:
A.O和F B.F和S C.S和Cl D.O和Cl
(3)根据同主族元素性质的相似性和递变性进行预测:
①关于Se的预测正确的是:
A.常温下Se单质是气体
B. Se最高价氧化物的水化物能和NaOH发生反应
C. 氢化物的化学式为H2Se
D. 常见的氧化物只有SeO3
②已知Cl2在水溶液中能和SO2反应,Cl2+2H2O+SO2==H2SO4+2HCl,写出Br2在水溶液中和SO2反应的离子反应方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】下表是周期表中的一部分,根据A~J在周期表中的位置,用元素符号或化学式回答下列问题:
(1)表中元素,只有负价而无正价的是___________________ ,可用于制半导体材料的元素是___________________ (填元素符号)。
(2)最高价氧化物的水化物碱性最强的是___________________ ,酸性最强的是___________________ ,呈两性的是___________________ (填化学式)。
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 1 | A | |||||||
| 2 | D | E | G | |||||
| 3 | B | C | J | F | H | I |
(1)表中元素,只有负价而无正价的是
(2)最高价氧化物的水化物碱性最强的是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】如图是元素周期表的一部分,表中的①~⑩中元素,填空回答:
用元素符号 或化学式 回答下列问题:
(1)在这些元素中,化学性质最不活泼的原子的原子结构示意图为______________ 。
(2)氧化性最强的单质是_____________ 。
(3)这些元素中的最高价氧化物对应的水化物中,酸性最强的是_____________ ,碱性最强的是_____________ ,呈两性的氢氧化物是_____________ 。
(4)写出①②③⑦对应的氢化物的稳定性由强到弱的是_____________ ,
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ③ | ④ | ||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
用
(1)在这些元素中,化学性质最不活泼的原子的原子结构示意图为
(2)氧化性最强的单质是
(3)这些元素中的最高价氧化物对应的水化物中,酸性最强的是
(4)写出①②③⑦对应的氢化物的稳定性由强到弱的是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】已知溴原子的原子结构示意图为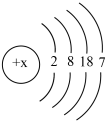
(1)溴元素在元素周期表中位置是___________ 。
(2)溴元素的最低化合价为___________ ,溴元素的最高价氧化物的水化物的化学式为___________ 。
(3)溴元素的非金属性比氯元素的非金属性___________ (选填“强”或“弱”)。
(4)向 溶液中滴加少量溴水,反应的离子方程式为
溶液中滴加少量溴水,反应的离子方程式为___________ 。继续加入少量苯,充分振荡,静置后观察到实验现象为___________ 。

(1)溴元素在元素周期表中位置是
(2)溴元素的最低化合价为
(3)溴元素的非金属性比氯元素的非金属性
(4)向
 溶液中滴加少量溴水,反应的离子方程式为
溶液中滴加少量溴水,反应的离子方程式为
您最近一年使用:0次
【推荐1】从下列各组物质中,找出合适的序号填在对应的空格内:
①NO2和N2O4 ②12C和14C ③金刚石和石墨 ④异戊烷(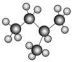 )和新戊烷(
)和新戊烷(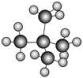 ) ⑤
) ⑤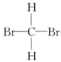 和
和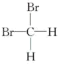 ⑥甲烷和丙烷。
⑥甲烷和丙烷。
(1)互为同位素的是____ (填序号,下同)。
(2)互为同分异构体的是____ 。
(3)互为同系物的是____ 。
(4)为同一种物质的是____ 。
①NO2和N2O4 ②12C和14C ③金刚石和石墨 ④异戊烷(
 )和新戊烷(
)和新戊烷( ) ⑤
) ⑤ 和
和 ⑥甲烷和丙烷。
⑥甲烷和丙烷。(1)互为同位素的是
(2)互为同分异构体的是
(3)互为同系物的是
(4)为同一种物质的是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】从下列各组物质中,找出合适的序号填在对应的空格内:
①甲烷和丙烷②12C和14C③金刚石和石墨④H和D⑤异戊烷( )和新戊烷(
)和新戊烷(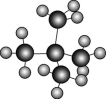 )⑥
)⑥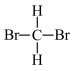 和
和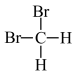 ⑦正丁烷和异丁烷⑧
⑦正丁烷和异丁烷⑧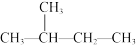 和
和
(1)互为同位素的是_______ (填序号,下同)。
(2)互为同分异构体的是_______ 。
(3)互为同系物的是_______ 。
(4)为同一种物质的是_______ 。
(5)互为同素异形体的是_______
①甲烷和丙烷②12C和14C③金刚石和石墨④H和D⑤异戊烷(
 )和新戊烷(
)和新戊烷( )⑥
)⑥ 和
和 ⑦正丁烷和异丁烷⑧
⑦正丁烷和异丁烷⑧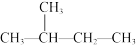 和
和
(1)互为同位素的是
(2)互为同分异构体的是
(3)互为同系物的是
(4)为同一种物质的是
(5)互为同素异形体的是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】 的衰变方程式为
的衰变方程式为 ,其中
,其中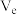 是反中微子,它的电荷为零,静止质量可以为零。
是反中微子,它的电荷为零,静止质量可以为零。
(1)下列关于 的叙述中,错误的是
的叙述中,错误的是___________ (填字母)。
A.质子数是27 B.电子数是27 C.质量数是27 D.中子数是60
(2)在上述衰变方程式中,衰变产物 的质量数A为
的质量数A为___________ ,核电荷数Z为___________ 。
(3)元素的化学性质主要取决于___________ (填字母)。
A.最外层电子数 B.核内中子数 C.核内质子数 D.质量数
(4)不同种元素的本质区别是___________ (填字母)。
A.质子数不同 B.中子数不同 C.电子数不同 D.质量数不同
 的衰变方程式为
的衰变方程式为 ,其中
,其中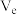 是反中微子,它的电荷为零,静止质量可以为零。
是反中微子,它的电荷为零,静止质量可以为零。(1)下列关于
 的叙述中,错误的是
的叙述中,错误的是A.质子数是27 B.电子数是27 C.质量数是27 D.中子数是60
(2)在上述衰变方程式中,衰变产物
 的质量数A为
的质量数A为(3)元素的化学性质主要取决于
A.最外层电子数 B.核内中子数 C.核内质子数 D.质量数
(4)不同种元素的本质区别是
A.质子数不同 B.中子数不同 C.电子数不同 D.质量数不同
您最近一年使用:0次

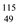 In的中子数与电子数的差值为
In的中子数与电子数的差值为

