请完成下列空白:
铁元素位于元素周期表的第___________ 周期第___________ 族,属于___________ 区。
| 表示方法 |  |  |
| 原子(或离子)结构示意图 | ||
| 电子排布式 | ||
| 价电子轨道表示式 |
更新时间:2021/12/03 09:07:47
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】化学元素周期表(Periodictableofelements)是根据元素原子核电荷数从小至大排序的化学元素列表。如表是元素周期表的一部分,根据表中给出的10种元素(其中X、Y、Z分别表示某种化学元素),按要求作答。
(1)Z元素符号是___________ 。
(2)表中元素化学性质最稳定的是___________ (填元素符号)。
(3)地壳中含量最多的元素在元素周期表中的位置是___________ 。
(4)写出Na的原子结构示意图___________ 。
(5)主要用来制作高纯半导体、耐高温材料、光导纤维通信材料的元素名称是___________ 。
(6)卤族元素之一,属周期系VIIA族,在元素周期表中位于第二周期的元素是___________ 。
(7)O2与S单质相比,更难与H2化合的是___________ 。
(8)写出N元素的气态氢化物的化学式___________ ,该物质与水反应的化学方程式:___________ 。
(9)Cl2与水反应的生成物中具有漂白作用的是___________ (填化学式),写出Cl2与NaOH溶液反应的离子方程式:___________ 。
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | X | N | O | F | Y | |||
| 3 | Na | Z | Al | Si | S | Cl |
(2)表中元素化学性质最稳定的是
(3)地壳中含量最多的元素在元素周期表中的位置是
(4)写出Na的原子结构示意图
(5)主要用来制作高纯半导体、耐高温材料、光导纤维通信材料的元素名称是
(6)卤族元素之一,属周期系VIIA族,在元素周期表中位于第二周期的元素是
(7)O2与S单质相比,更难与H2化合的是
(8)写出N元素的气态氢化物的化学式
(9)Cl2与水反应的生成物中具有漂白作用的是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】用化学用语表示:
(1)根据下列几种粒子的结构示意图,回答问题:
A B
B C
C D
D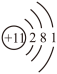 E
E F
F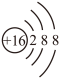
①写出C微粒的符号__________ ;
②只能失电子的粒子是_____________________ ;(填编号,下同)
③某元素R形成的氧化物为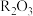 ,则R的离子结构示意图可能是
,则R的离子结构示意图可能是_____________________ 。
(2)写出下列反应的化学方程式:
①在空气中,漂白粉漂白原理________________________________ ;
②工业上的“氯碱工业”________________________________ 。
(1)根据下列几种粒子的结构示意图,回答问题:
A
 B
B C
C D
D E
E F
F
①写出C微粒的符号
②只能失电子的粒子是
③某元素R形成的氧化物为
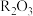 ,则R的离子结构示意图可能是
,则R的离子结构示意图可能是(2)写出下列反应的化学方程式:
①在空气中,漂白粉漂白原理
②工业上的“氯碱工业”
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】填空
(1)砷原子的最外层电子排布式是4s24p3,在元素周期表中,砷元素位于第_____ 周期_____ 族;最高价氧化物的化学式为_____ ,砷酸钠的化学式是_____ 。
(2)已知下列元素在周期表中的位置,写出它们的价电子排布式和元素符号:
①第4周期ⅣB族_____ ;
②第5周期ⅦA族_____ 。
(1)砷原子的最外层电子排布式是4s24p3,在元素周期表中,砷元素位于第
(2)已知下列元素在周期表中的位置,写出它们的价电子排布式和元素符号:
①第4周期ⅣB族
②第5周期ⅦA族
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】已知 的3d轨道上有6个电子,试回答:
的3d轨道上有6个电子,试回答:
(1)M元素原子的核外电子排布式为_______ 。
(2)M元素在元素周期表中的位置为_______ 。
(3)M的基态原子共有_______ 种不同能级的电子,该原子最外层电子数为_______ ,价层电子数为_______ 。
(4)某元素原子的基态电子排布式为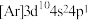 ,该元素处于元素周期表的第
,该元素处于元素周期表的第_______ 周期第_______ 族。试推测该元素处于元素周期表的_______ 区,该元素原子的价电子排布图为_______ 。
(5)与M元素相对比,铬(Cr)元素的原子核外电子排布有其特点,请写出Cr基态原子核外电子排布式_______ 。
 的3d轨道上有6个电子,试回答:
的3d轨道上有6个电子,试回答:(1)M元素原子的核外电子排布式为
(2)M元素在元素周期表中的位置为
(3)M的基态原子共有
(4)某元素原子的基态电子排布式为
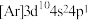 ,该元素处于元素周期表的第
,该元素处于元素周期表的第(5)与M元素相对比,铬(Cr)元素的原子核外电子排布有其特点,请写出Cr基态原子核外电子排布式
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】回答下列问题:
(1)基态Mn原子核外有___________ 种运动状态不同的电子。
(2)基态镁原子核外M层电子的自旋状态___________ (填“相同”或“相反”)。
(3)基态Ge原子有___________ 个未成对电子。
(4)镍元素基态原子的电子排布式为___________ 。
(5)氮原子价层电子的轨道表达式(电子排布图)为___________ 。
(6)基态 与
与 离子中未成对的电子数之比为
离子中未成对的电子数之比为___________ 。
(7)基态K原子中,核外电子占据的最高能层的符号是___________ 。
(8)Se的基态原子中电子占据的原子轨道总数为___________ 。
(1)基态Mn原子核外有
(2)基态镁原子核外M层电子的自旋状态
(3)基态Ge原子有
(4)镍元素基态原子的电子排布式为
(5)氮原子价层电子的轨道表达式(电子排布图)为
(6)基态
 与
与 离子中未成对的电子数之比为
离子中未成对的电子数之比为(7)基态K原子中,核外电子占据的最高能层的符号是
(8)Se的基态原子中电子占据的原子轨道总数为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】下表是元素周期表的一部分,表中所列字母分别代表一种元素。试回答下列问题:___________ 区。
②基态e离子的核外电子排布式是___________ 。
③基态g原子核外能量不同的电子有___________ 种。
④元素1的基态原子的核外电子共占据___________ 个原子轨道。
(2)将c、d、e、f四种元素按电负性由小到大的顺序排列___________ (用元素符号表示)。
(3)元素a和c可以构成多种化合物,苯就是其中的一种。以下有关苯分子中化学键的描述正确的是___________
(4)下列有关分子的空间结构,描述正确的是___________
(5)据报道,大气中存在一种潜在的温室气体 (结构如图),虽然其数量有限,但它是已知气体中吸热最高的。关于
(结构如图),虽然其数量有限,但它是已知气体中吸热最高的。关于 的说法正确的是___________
的说法正确的是___________
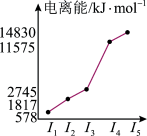
(6)表中所列的某主族元素的电离能情况如图所示,则该元素是___________ (填元素符号)。
①玻璃纤维是合成纤维的一种,属于高分子材料。___________
②二氧化硫具有氧化性,可用于漂白纸浆。___________
③CaO能与 反应,可作工业废气的脱硫剂。
反应,可作工业废气的脱硫剂。___________
④制 时,用水或NaOH溶液吸收尾气。
时,用水或NaOH溶液吸收尾气。___________
(8)o、p两元素的部分电离能数据列于下表:
比较两元素的 、
、 可知,气态
可知,气态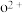 再失去一个电子比气态
再失去一个电子比气态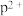 再失去一个电子难,其原因是
再失去一个电子难,其原因是___________
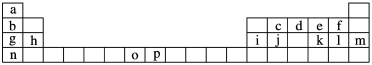
②基态e离子的核外电子排布式是
③基态g原子核外能量不同的电子有
④元素1的基态原子的核外电子共占据
(2)将c、d、e、f四种元素按电负性由小到大的顺序排列
(3)元素a和c可以构成多种化合物,苯就是其中的一种。以下有关苯分子中化学键的描述正确的是___________
A.每个碳原子的一个 杂化轨道参与形成大π键 杂化轨道参与形成大π键 |
| B.每个碳原子的未参加杂化的2p轨道形成大π键 |
C.碳原子的3个 杂化轨道与其他碳原子形成2个σ键和1个π键 杂化轨道与其他碳原子形成2个σ键和1个π键 |
| D.碳原子的未参加杂化的2p轨道与其他碳原子的2p轨道成键 |
(4)下列有关分子的空间结构,描述正确的是___________
A. 分子中N原子处在3个H原子所组成的三角形的中心 分子中N原子处在3个H原子所组成的三角形的中心 |
B. 分子中C原子处在4个Cl原子所组成的四面体的中心 分子中C原子处在4个Cl原子所组成的四面体的中心 |
C. 分子中O原子处在2个H原子所连成的直线的中央 分子中O原子处在2个H原子所连成的直线的中央 |
D. 分子中P原子处在3个Cl原子所组成的三角形的中心 分子中P原子处在3个Cl原子所组成的三角形的中心 |
(5)据报道,大气中存在一种潜在的温室气体
 (结构如图),虽然其数量有限,但它是已知气体中吸热最高的。关于
(结构如图),虽然其数量有限,但它是已知气体中吸热最高的。关于 的说法正确的是___________
的说法正确的是___________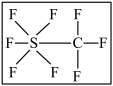
| A.分子中有σ键也有π键 |
B. 是s-pσ键 是s-pσ键 |
| C.分子中不是所有原子都满足8电子稳定结构 |
D.0.1mol 分子中电子数为8mol 分子中电子数为8mol |
(6)表中所列的某主族元素的电离能情况如图所示,则该元素是
①玻璃纤维是合成纤维的一种,属于高分子材料。
②二氧化硫具有氧化性,可用于漂白纸浆。
③CaO能与
 反应,可作工业废气的脱硫剂。
反应,可作工业废气的脱硫剂。④制
 时,用水或NaOH溶液吸收尾气。
时,用水或NaOH溶液吸收尾气。(8)o、p两元素的部分电离能数据列于下表:
| 元素 | o | p |
 | 717 | 759 |
 | 1509 | 1561 |
 | 3248 | 2957 |
 、
、 可知,气态
可知,气态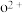 再失去一个电子比气态
再失去一个电子比气态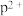 再失去一个电子难,其原因是
再失去一个电子难,其原因是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】近期我国科研工作者研究的金属—氮—碳优异电催化 还原催化剂取得新进展。回答下列问题:
还原催化剂取得新进展。回答下列问题:
(1) 可用于考古,其中子数为
可用于考古,其中子数为___________ ,该基态原子价层电子轨道表示式为___________ 。
(2)研究发现钴—氮—碳优异电催化 还原催化剂活性最高,金属钴的核外电子排布式为
还原催化剂活性最高,金属钴的核外电子排布式为___________ ;基态 未成对电子数为
未成对电子数为___________ 。
(3)基态N原子中,电子占据的最高能层符号为___________ ,该能层具有的原子轨道数为___________ ,电子数为___________ 。
 还原催化剂取得新进展。回答下列问题:
还原催化剂取得新进展。回答下列问题:(1)
 可用于考古,其中子数为
可用于考古,其中子数为(2)研究发现钴—氮—碳优异电催化
 还原催化剂活性最高,金属钴的核外电子排布式为
还原催化剂活性最高,金属钴的核外电子排布式为 未成对电子数为
未成对电子数为(3)基态N原子中,电子占据的最高能层符号为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】原子序数依次增大的四种元素A、B、C、D分别处于第一至第四周期.自然界存在多种A的化合物,B原子核外电子有6种不同的运动状态,B与C可形成正四面体形的分子,D的基态原子的最外能层只有一个电子,其他能层均已充满电子.请回答下列问题:
⑴这四种元素中电负性最大的元素的基态原子的价电子排布图为______ .
⑵由A与B两种元素形成的化合物中,其中B原子采用sp杂化的最简单化合物分子中,含有的δ键、π键数目之比为______ .
⑶D元素的常见离子的水溶液显色的原因是______ ,此离子中存在的化学键有______ (a.离子键 b.共价键c.配位键d.氢键e.范德华力f.金属键
⑴这四种元素中电负性最大的元素的基态原子的价电子排布图为
⑵由A与B两种元素形成的化合物中,其中B原子采用sp杂化的最简单化合物分子中,含有的δ键、π键数目之比为
⑶D元素的常见离子的水溶液显色的原因是

您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】根据原子核外电子排布规则,回答下列问题:
(1)基态N原子中,核外电子占据的最高能级的符号是___________ ,占据该能级电子的电子云轮廓图形状为___________ 。
(2)写出基态24Cr原子的核外电子排布式:___________ 。
(3)写出基态N原子的轨道表示式:___________ 。
(1)基态N原子中,核外电子占据的最高能级的符号是
(2)写出基态24Cr原子的核外电子排布式:
(3)写出基态N原子的轨道表示式:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】(1)第四周期中,未成对电子数最多的元素是________ ,(填名称)它位于第________ 族;核外电子排布式是__________________ 。它有________ 种运动状态不同的电子,其价电子排布图为:______________ 。
(2)已知NH5为离子化合物,写出其电子式:________ 。
(3)某同学根据掌握的知识分析Mg的核外电子排布为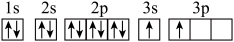 。该同学所画的电子排布图违背了
。该同学所画的电子排布图违背了________ 。
(4)在基态14C原子中,核外存在________ 对自旋相反的电子。
(2)已知NH5为离子化合物,写出其电子式:
(3)某同学根据掌握的知识分析Mg的核外电子排布为
 。该同学所画的电子排布图违背了
。该同学所画的电子排布图违背了(4)在基态14C原子中,核外存在
您最近一年使用:0次

 的原子结构示意图
的原子结构示意图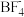 中心原子B的杂化方式为
中心原子B的杂化方式为 分子空间构型为
分子空间构型为

