X、Y、Z是三种短周期主族元素,已知其最高价氧化物对应的水化物的酸性由强到弱的顺序为HXO4>H2YO4>H3ZO4,下列说法正确的是
| A.单质与氢气反应的剧烈程度:X<Y<Z |
| B.原子半径:X<Y<Z |
| C.对应单质的氧化性:X<Y<Z |
| D.HX是同主族元素的气态氢化物中最稳定的 |
更新时间:2022-04-04 07:31:33
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】M、W、X、Y、Z是同周期主族元素,X原子的最外层电子数是W原子次外层电子数的3倍。它们形成的化合物可用作新型电池的电极材料,结构如图所示,化合物中除M+外其它原子均满足8电子稳定结构。下列说法正确的是
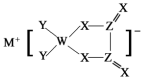

| A.原子半径:M>Z>W>X>Y |
| B.W的最高价氧化物对应的水化物是强酸 |
| C.简单气态氢化物稳定性:X<Y |
| D.上述五种元素中Z的电负性最大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】元素周期律多为大致规律,同时存在不少特例,下列说法正确的是
| A.主族元素对应单质氧化性越强,非金属性越强,没有特例 |
| B.同周期元素基态原子的第一电离能从左往右逐渐增大,没有特例 |
| C.同主族元素的最高化合价数值均等于相应基态原子最外层电子数,没有特例 |
| D.同主族元素原子半径从上往下逐渐增大,没有特例 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】下列结论正确的是( )
①粒子半径:S2->Cl>S ②氢化物稳定性:HF>HCl>H2S ③离子还原性:S2->Cl->Br->I- ④单质氧化性:Cl2>S ⑤酸性:H2SO4>HClO4 ⑥分散系中分散质粒子的直径:Fe(OH)3悬浊液>Fe(OH)3胶体>FeCl3溶液
①粒子半径:S2->Cl>S ②氢化物稳定性:HF>HCl>H2S ③离子还原性:S2->Cl->Br->I- ④单质氧化性:Cl2>S ⑤酸性:H2SO4>HClO4 ⑥分散系中分散质粒子的直径:Fe(OH)3悬浊液>Fe(OH)3胶体>FeCl3溶液
| A.①⑤ | B.③⑥ | C.②④⑥ | D.①③④ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列有关氢化物的叙述中正确的是:
| A.稳定性:H2S>HF | B.HCl的电子式为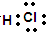 |
| C.H2O的摩尔质量为18 | D.在卤化氢中HI最稳定 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】从单质氟到碘,下列情况中不能反映出它们的氧化性强弱不同的是( )
| A.单质与卤化物之间的置换情况 |
| B.与氢气反应的情况 |
| C.与硝酸银反应生成卤化银的颜色情况 |
| D.与水反应的情况 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】有五种短周期元素X、Y、Z、M、W的原子序数依次增大,其最高正化合价或最低负化合价与原子序数的关系如下图,下列说法不正确 的是
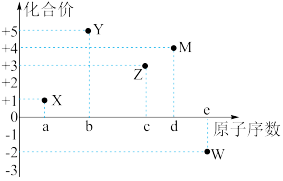

| A.元素X可能是锂 |
B.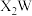 中各原子均达到8电子稳定结构 中各原子均达到8电子稳定结构 |
C.原子半径: |
D.元素气态氢化物的稳定性: |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列关于元素周期表和周期律的说法正确的是
| A.现行元素周期表有七个周期,18个族 |
| B.熔点:Li>K,沸点:I2>Br2 |
| C.盐酸的酸性比氢硫酸酸性强,可推测非金属性:Cl>S |
| D.At与I属于同主族元素,可推测AgAt为难溶于水的白色固体 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】现有X、Y、Z、W四种短周期元素,X、Y位于同主族,Z、W位于同主族且Z的核电荷数是W的2倍,Y、Z位于同周期,X与Z、W都不在同一周期。下列说法不正确的是
| A.简单离子半径:Z>W>Y |
| B.气态氢化物的稳定性:Z<W |
| C.Z的氢化物能与其最高价氧化物对应的水化物反应 |
| D.在X2和W2构成的燃料电池中,W2作负极 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列排列顺序正确的是
| A.微粒半径:Na+>K+>Cl->S2- | B.熔沸点:Li>Na>K>Rb |
| C.碱性:LiOH>NaOH>KOH>RbOH | D.稳定性:HI>HBr>HCl>HF |
您最近一年使用:0次

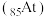 也是卤族元素,试推测砹和砹的化合物最
也是卤族元素,试推测砹和砹的化合物最





