木炭与浓硫酸反应可表示为:C+2H2SO4(浓)═CO2↑+2SO2↑+2H2O。
(1)该反应的反应物和生成物中,属于酸性氧化物的是_______ 。
(2)木炭作_______ (填“氧化剂”或“还原剂”),硫酸_______ (填“被氧化”或“被还原”)。
(3)若消耗了1molH2SO4,则生成_______ molSO2。
(4)用双线桥标出电子转移的方向和数目_______ 。
(1)该反应的反应物和生成物中,属于酸性氧化物的是
(2)木炭作
(3)若消耗了1molH2SO4,则生成
(4)用双线桥标出电子转移的方向和数目
更新时间:2022-04-04 10:39:49
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】我国古代四大发明之一的黑火药是由硫黄粉、硝酸钾和木炭粉按一定比例混合而成的,爆炸时的反应为:S+2KNO3+3C=K2S+N2↑+3CO2↑。
(1)在该反应中,还原剂是____ (填化学式),KNO3发生了____ 反应(填“氧化”或“还原”)。
(2)烟花爆竹的成分中含有黑火药。点燃后,瞬间产生大量气体,同时释放大量热,在有限的空间里,气体受热迅速膨胀引起爆炸。反应中每消耗0.1molS,释放的气体体积为_____ L(换算成标准状况)。
(3)除了黑火药,烟花爆竹中常加入一些金属元素,燃烧时会产生五彩缤纷的火焰。下表为一些金属元素的焰色:
若燃放烟花的火焰呈现紫色,则烟花中可能含有____ 元素,该元素的离子结构示意图为_____ 。
(1)在该反应中,还原剂是
(2)烟花爆竹的成分中含有黑火药。点燃后,瞬间产生大量气体,同时释放大量热,在有限的空间里,气体受热迅速膨胀引起爆炸。反应中每消耗0.1molS,释放的气体体积为
(3)除了黑火药,烟花爆竹中常加入一些金属元素,燃烧时会产生五彩缤纷的火焰。下表为一些金属元素的焰色:
| 金属元素 | 钠 | 钾 | 钙 | 锶 | 钡 | 铜 |
| 火焰颜色 | 黄 | 紫 | 砖红 | 洋红 | 黄绿 | 绿色 |
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】用双线桥法标出下列方程式中电子转移的方向和数目,并指出氧化剂和还原剂
(1)MnO2 + 4HCl(浓) = MnCl2 + 2H2O + Cl2↑____ ,氧化剂:_____ 还原剂:_____
(2)Zn + Cu SO4 = Zn SO4 + Cu____ , 氧化剂_____ 还原剂______
(1)MnO2 + 4HCl(浓) = MnCl2 + 2H2O + Cl2↑
(2)Zn + Cu SO4 = Zn SO4 + Cu
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】Ⅰ 化学与人类社会可持续发展密切相关,能源、环境、材料以及日常生活等都离不开化学。请根据题意回答以下问题:
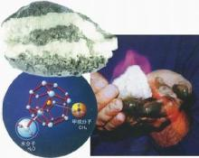
(1)海底埋藏着大量可燃烧的“冰”,“可燃冰”外观像冰,主要成分为甲烷水合物,并含有少量CO2等。可燃冰属于_______ (填“纯净物”或“混合物”);在较低的温度和压力下,用甲烷为原料可制成金刚石薄膜,该变化属于_______ (填“物理变化”或“化学变化”)。
(2)铝制品表面因有一层氧化铝薄膜而经久耐用,若用铝制容器长期盛装含强碱性的食物该容器表面会发生破损,相关反应的离子方程式为____________ 。
(3)粗盐中含可溶性CaCl2、MgCl2及一些硫酸盐,除去这些杂质的试剂可选用①Na2CO3、②NaOH、③BaCl2、④HCl,用序号表示加入的先后顺序是________ 。
II 新型纳米材料氧缺位铁酸盐(MFe2Ox,3<x<4,M=Mn、Zn、Ni,且均为+2价,下同)是由铁酸盐MFe2O4经过高温反应得到的。
(4)ZnFe2O4中Fe元素的化合价为________ 。
(5)含氧铁盐K2FeO4的重要应用之一是生成Fe(OH)3胶体吸附净水。实验室可用饱和FeCl3溶液模拟该胶体的制备,请写出化学反应方程式_________ 。
(6)在酸性条件下,某反应体系中共存在下列6种粒子: 、Fe2+、H+、H2O、Cu2O、Cu2+,请完成该反应的离子方程式并用双线桥表示电子的转移
、Fe2+、H+、H2O、Cu2O、Cu2+,请完成该反应的离子方程式并用双线桥表示电子的转移____ 。

(1)海底埋藏着大量可燃烧的“冰”,“可燃冰”外观像冰,主要成分为甲烷水合物,并含有少量CO2等。可燃冰属于
(2)铝制品表面因有一层氧化铝薄膜而经久耐用,若用铝制容器长期盛装含强碱性的食物该容器表面会发生破损,相关反应的离子方程式为
(3)粗盐中含可溶性CaCl2、MgCl2及一些硫酸盐,除去这些杂质的试剂可选用①Na2CO3、②NaOH、③BaCl2、④HCl,用序号表示加入的先后顺序是
II 新型纳米材料氧缺位铁酸盐(MFe2Ox,3<x<4,M=Mn、Zn、Ni,且均为+2价,下同)是由铁酸盐MFe2O4经过高温反应得到的。
(4)ZnFe2O4中Fe元素的化合价为
(5)含氧铁盐K2FeO4的重要应用之一是生成Fe(OH)3胶体吸附净水。实验室可用饱和FeCl3溶液模拟该胶体的制备,请写出化学反应方程式
(6)在酸性条件下,某反应体系中共存在下列6种粒子:
 、Fe2+、H+、H2O、Cu2O、Cu2+,请完成该反应的离子方程式并用双线桥表示电子的转移
、Fe2+、H+、H2O、Cu2O、Cu2+,请完成该反应的离子方程式并用双线桥表示电子的转移
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】用双线桥法表示出化合价的升降、电子转移数目,指出氧化反应和还原反应及氧化剂和还原剂.
(1)2KClO3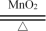 2KCl+3O2↑
2KCl+3O2↑
__________________________________
(2)4P+ 5O2 2P2O5
2P2O5
__________________________________
(1)2KClO3
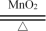 2KCl+3O2↑
2KCl+3O2↑(2)4P+ 5O2
 2P2O5
2P2O5
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】氧化还原反应是一类重要的反应,在工农业生产、日常生活中都有广泛的用途。
I、三氟化氮(NF3,氟元素显−1价)是一种无色、无味的气体,在潮湿的空气中与水蒸气能发生氧化还原反应,其反应产物有HF、NO和HNO3。请根据要求回答下列问题:
(1)NF3中N的化合价为___________ 。
(2)反应过程中,被氧化与被还原的元素原子个数之比为___________ 。
(3)写出该反应的化学方程式:___________ ,NO是该反应的___________ (填“氧化剂”“还原剂”“氧化产物“还原产物”)。
(4)三氟化氮可由反应4NH3+3F2=NF3+3NH4F得到,说明氧化性NF3___________ F2(填“>”“<”或“=”)。
Ⅱ、高铁酸钠(Na2FeO4)是一种新型绿色消毒剂,其一种制备原理如下,请配平该方程式
(5)___________ClO-+___________Fe3++___________OH-=___________ +___________Cl-+___________H2O
+___________Cl-+___________H2O___________ 。
Ⅲ、Cu可与稀硝酸反应:3Cu+8HNO3(稀) =3Cu(NO3)2+2NO↑+4H2O
(6)请用双线桥表示反应中的电子转移的方向和数目___________ 。
(7)该反应中,硝酸体现的性质为___________ ,每生成1分子NO转移电子的数目为___________ 。
I、三氟化氮(NF3,氟元素显−1价)是一种无色、无味的气体,在潮湿的空气中与水蒸气能发生氧化还原反应,其反应产物有HF、NO和HNO3。请根据要求回答下列问题:
(1)NF3中N的化合价为
(2)反应过程中,被氧化与被还原的元素原子个数之比为
(3)写出该反应的化学方程式:
(4)三氟化氮可由反应4NH3+3F2=NF3+3NH4F得到,说明氧化性NF3
Ⅱ、高铁酸钠(Na2FeO4)是一种新型绿色消毒剂,其一种制备原理如下,请配平该方程式
(5)___________ClO-+___________Fe3++___________OH-=___________
 +___________Cl-+___________H2O
+___________Cl-+___________H2OⅢ、Cu可与稀硝酸反应:3Cu+8HNO3(稀) =3Cu(NO3)2+2NO↑+4H2O
(6)请用双线桥表示反应中的电子转移的方向和数目
(7)该反应中,硝酸体现的性质为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】高铁酸盐是一种新型、高效、多功能绿色水处理剂,工业上可用湿法制备高铁酸钾:2Fe(OH)3+3ClO-+4OH-=2FeO +3Cl-+5H2O。
+3Cl-+5H2O。
(1)高铁酸根FeO 中铁元素化合价为
中铁元素化合价为_____ ,在该反应中氧化剂是_____ ,被氧化的元素是_____ 。
(2)请用双线桥表示反应中电子转移情况:2Fe(OH)3+3ClO-+4OH−=2FeO +3Cl-+5H2O
+3Cl-+5H2O_____ 。
(3)根据化合价,推测FeO 能和
能和_____ 反应(填标号)。
(4)工业盐中含有NaNO2,误食会中毒,其原因是NaNO2把人体内的Fe2+转化成Fe3+,使Fe2+失去与O2结合的能力,说明NaNO2具有_____ (填“氧化性”或“还原性”)。
(5)下列反应中属于氧化还原反应,但是水既不作氧化剂又不作还原剂的是_____ (填标号)。
(6)化工厂常用浓氨水检验管道是否漏气,其原理为3Cl2+8NH3=6NH4Cl+N2,被氧化的NH3与被还原的Cl2的个数之比为_____ 。
 +3Cl-+5H2O。
+3Cl-+5H2O。(1)高铁酸根FeO
 中铁元素化合价为
中铁元素化合价为(2)请用双线桥表示反应中电子转移情况:2Fe(OH)3+3ClO-+4OH−=2FeO
 +3Cl-+5H2O
+3Cl-+5H2O(3)根据化合价,推测FeO
 能和
能和| A.KMnO4 | B.SO2 | C.H2S | D.O2 |
(5)下列反应中属于氧化还原反应,但是水既不作氧化剂又不作还原剂的是
| A.Na2O+H2O=2NaOH | B.3NO2+H2O=2HNO3+NO |
| C.CaH2+2H2O=Ca(OH)2+2H2↑ | D.3Fe+4H2O(g) Fe3O4+4H2 Fe3O4+4H2 |
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】按要求填空:
(1)①石墨 ②盐酸 ③胆矾 ④KOH固体 ⑤Fe ⑥氨水 ⑦乙醇 ⑧冰醋酸 ⑨干冰 ⑩熔融BaSO4
能导电的是________________________ ,电解质是_______________________ ,非电解质是________________________ ;
(2)KIO3 + 5KI + 3H2SO4 == 3K2SO4 + 3I2 + 3H2O的反应中氧化产物和还原产物的物质的量之比是__________________ ;
(3)铁是应用最广的金属,铁的卤化物、氧化物以及高价铁的含氧酸盐为重要的化合物。高铁酸钾(K2FeO4)是一种强氧化剂,可作为水处理剂和高容量电池材料。FeCl3和KClO在强碱条件下反应制取K2FeO4,其反应的离子方程式为____________________________________
(1)①石墨 ②盐酸 ③胆矾 ④KOH固体 ⑤Fe ⑥氨水 ⑦乙醇 ⑧冰醋酸 ⑨干冰 ⑩熔融BaSO4
能导电的是
(2)KIO3 + 5KI + 3H2SO4 == 3K2SO4 + 3I2 + 3H2O的反应中氧化产物和还原产物的物质的量之比是
(3)铁是应用最广的金属,铁的卤化物、氧化物以及高价铁的含氧酸盐为重要的化合物。高铁酸钾(K2FeO4)是一种强氧化剂,可作为水处理剂和高容量电池材料。FeCl3和KClO在强碱条件下反应制取K2FeO4,其反应的离子方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】把19.2g的Cu放入600mL 2mol·L-1稀硝酸中,发生如下反应3Cu+8HNO3(稀)=3Cu (NO3)2+2NO↑+4H2O,充分反应,Cu完全溶解。
(1)写出Cu与稀硝酸反应的离子方程式:_______________ 。
(2)还原剂是_________ ,被还原的元素是________ ,还原产物是_____ ,氧化剂与还原剂的物质的量比为_______ 。
(3)转移的电子的数目为_________ (用含NA的式子表示),被还原的HNO3为______ mol,反应后溶液中c(H+)为_______ (体积变化忽略不计)
(1)写出Cu与稀硝酸反应的离子方程式:
(2)还原剂是
(3)转移的电子的数目为
您最近一年使用:0次

 4NO+6H2O
4NO+6H2O

