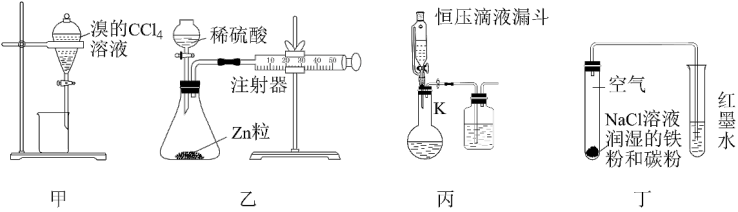
下列各组实验装置、所用试剂、实验现象及结论都正确的是
| A | B | C | D |
 | 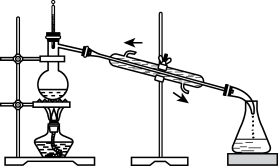 | 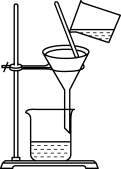 |  |
| 分离苯萃取碘水后已分层的有机层和水层 | 从三氯甲烷和四氯甲烷混合物中蒸馏出三氯甲烷 | 趁热过滤提纯苯甲酸 | 萃取时,将所需试剂加入分液漏斗,塞上玻璃塞,按如图所示方式用力振荡 |
| A.A | B.B | C.C | D.D |
更新时间:2022-04-21 11:37:16
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列说法正确的是
| A.提纯苯甲酸可采用蒸馏的方法 |
| B.分离正戊烷(沸点36℃)和正己烷(沸点69℃)可采用萃取的方法 |
| C.某有机物的相对分子质量为58,则其分子式一定为C3H6O |
| D.某烃完全燃烧生成CO2和H2O的物质的量之比为2:3,则其实验式为CH3 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】从古至今,化学与人类的生产生活紧密相关,下列说法正确的是
| A.“雨过天晴云破处”所描述的瓷器青色来自氧化铁 |
| B.“水银乃至阴之毒物,因火锻丹砂而出,加硫磺升而为银朱”,该过程应用了蒸馏的方法 |
| C.补铁保健品中的铁元素常常表现氧化性,与具有还原性的维生素C同服效果更佳 |
| D.将废铁屑加入FeCl2溶液中,可用于除去工业废气中的Cl2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
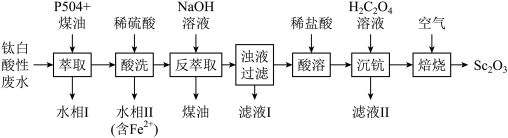
【推荐1】氧化钪( )广泛应用于航天、激光和导弹等尖端科学领域。利用钛白酸性废水(含
)广泛应用于航天、激光和导弹等尖端科学领域。利用钛白酸性废水(含 、
、 、
、 等)制备氧化钪的工艺具有较高的经济价值,其工艺流程如图所示:
等)制备氧化钪的工艺具有较高的经济价值,其工艺流程如图所示:
已知; 、
、 均能与P504(用HR表示)发生络合反应,且机理均为
均能与P504(用HR表示)发生络合反应,且机理均为 。
。
下列说法错误的是
 )广泛应用于航天、激光和导弹等尖端科学领域。利用钛白酸性废水(含
)广泛应用于航天、激光和导弹等尖端科学领域。利用钛白酸性废水(含 、
、 、
、 等)制备氧化钪的工艺具有较高的经济价值,其工艺流程如图所示:
等)制备氧化钪的工艺具有较高的经济价值,其工艺流程如图所示:
已知;
 、
、 均能与P504(用HR表示)发生络合反应,且机理均为
均能与P504(用HR表示)发生络合反应,且机理均为 。
。下列说法错误的是
| A.“萃取”时,有机相应从分液漏斗下口放出 |
B.与P504的络合能力: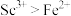 |
| C.“浊液过滤”时用到的玻璃仪器有漏斗、玻璃棒和烧杯 |
| D.该工业流程中Sc元素的化合价未发生变化 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】为提纯下列物质,除杂药品和分离方法都正确的是
| 被提纯的物质(杂质) | 除杂药品 | 分离方法 | |
| A | 乙醇(乙酸) | NaOH溶液 | 分液 |
| B | KBr溶液(KI) | 氯水、 | 萃取、分液 |
| C | 乙烷(乙烯) | 氢气 | 洗气 |
| D |  | 饱和 溶液 溶液 | 洗气 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】垃圾分类具有社会、经济、生态等几方面的效益,为研究废旧电池的再利用,实验室利用旧电池的铜帽(主要成分为Zn和Cu)回收Cu并制备ZnO的部分实验流程如图所示。下列说法错误的是
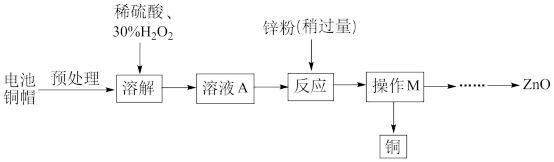

| A.“溶解”过程中,加入H2O2的作用是氧化Cu而使Cu溶解 |
| B.加入锌粉过量的目的是使铜离子完全转化为铜单质 |
| C.操作M中用到的玻璃仪器有铁架台、烧杯、漏斗和玻璃棒 |
| D.通过加适量碱、过滤、洗涤、干燥、加热等操作,可得到ZnO |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列由废铜屑(杂质不溶于水也不参与反应)制取CuSO4·5H2O的过程不能达到实验目的的是


| A.除去废铜屑表面的油污 | B.溶解废铜屑 |
| C.过滤得CuSO4(aq) | D.蒸发结晶得CuSO4·5H2O |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列说法不正确的是
| A.受酸腐蚀致伤,先用大量水冲洗,再用稀氨水、肥皂水或饱和碳酸氢钠溶液洗,最后再用水洗 |
| B.饱和FeSO4溶液中加入适量(NH4)2SO4晶体,经过滤、洗涤,即可得纯净的硫酸亚铁铵晶体 |
| C.市售食醋总酸含量大约5%,浓度接近1mol·L-1,稀释10倍再进行滴定,可减小误差 |
| D.实验室完成焰色反应时,若无铂丝,可用铁丝代替,但不可用铜丝或玻璃棒 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列实验方案中,能达到相应实验目的的是
| 选项 | 方案 | 目的 |
| A | 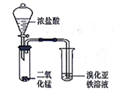 | 验证氧化性::Cl2>Br2 |
| B | 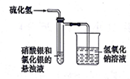 | 验证溶解度:AgCl>Ag2S |
| C | 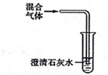 | 检验SO2、CO2混合气体中有CO2 |
| D | 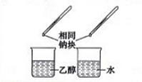 | 比较乙醇中羟基氢原子和水分子中氢原子的活泼性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】用相同的铝片、6 mol·L-1稀盐酸、3 mol·L-1稀硫酸、6 mol·L-1氢氧化钠溶液、试管等分别进行下表实验:
对上述实验的相关说法不正确 的是
| 实验方案 | 实验现象 | 实验原理(化学方程式) |
| (1)铝片与足量盐酸反应 | 铝片开始无现象,一段时间后逐渐溶解,并有大量气泡产生 | Al2O3+6HCl=2AlCl3+3H2O 2Al+6HCl=2AlCl3+3H2↑ |
| (2)铝片与足量硫酸反应 | 铝片开始无现象,一段时间后反应缓慢,铝片表面有少量气泡产生 | Al2O3+3H2SO4=2Al2(SO4)3+3H2O 2Al+3H2SO4=2Al2(SO4)3+3H2↑ |
| (3)铝片与足量氢氧化钠溶液反应 | 铝片开始无现象,一段时间后铝片逐渐溶解,并有大量气泡产生 | Al2O3+2NaOH=2NaAlO2+H2O 2Al+2NaOH+2H2O=2NaAlO2+3H2↑ |
| A.对比(1)、(2)、(3)中Al2O3参与的反应可得出:Al2O3既有碱性氧化物的某些性质,又有酸性氧化物的某些性质 |
| B.对比(1)、(2)、(3)中气体产生现象和酸碱的挥发性可得出:实验(3)最适宜于实验室制备H2 |
| C.对比实验(1)、(2)中后来产生气泡的现象,可得出:c(H+)越大,相同时间内产生气泡越多 |
D.对比实验(1)、(2)中后来产生气泡的现象,可得出: 对Al与H+的反应可能有阻碍作用 对Al与H+的反应可能有阻碍作用 |
您最近一年使用:0次