溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如下:
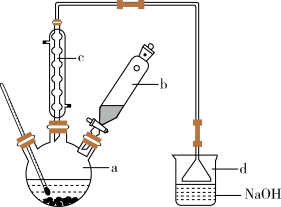
I.合成步骤:在a中加入15 mL无水苯和少量铁屑。在b中小心加入5.0 mL液溴。打开活塞,向a中滴入液溴,发生反应。
请回答下列问题:
(1)仪器c的名称为_______ ,实验室制取溴苯的化学方程式为_______ 。
(2)反应过程中,仪器a外壁温度升高,为提高原料利用率可利用温度计控制温度,适宜的温度范围为_______(填标号)。
(3)装置d的作用除了能防倒吸外,还有_______ 。
(4)本实验中,仪器a的容积最适合的是_______(填标号)。
II.待反应完成后,取出a装置中的混合物,设计如下流程分离、提纯溴苯:
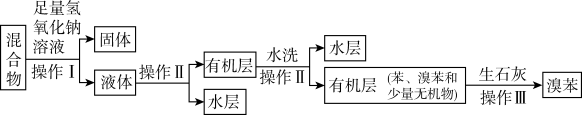
(5)流程中“固体”的化学式为_______ ,操作I的名称是。_______ ,。操作II所需主要玻璃仪器有_______ 。
(6)设计实验检验水洗是否达到目的:_______ 。
(7)若经过操作III后得纯溴苯11. 30 g。则溴苯的产率是_______ (计算结果保留2位有效数字)。
| 苯 | 溴 | 溴苯 | |
| 密度/g·cm-3 | 0.88 | 3.20 | 1.50 |
| 沸点/°C | 80 | 59 | 156 |
| 水中溶解度 | 微溶 | 微溶 | 微溶 |

I.合成步骤:在a中加入15 mL无水苯和少量铁屑。在b中小心加入5.0 mL液溴。打开活塞,向a中滴入液溴,发生反应。
请回答下列问题:
(1)仪器c的名称为
(2)反应过程中,仪器a外壁温度升高,为提高原料利用率可利用温度计控制温度,适宜的温度范围为_______(填标号)。
| A.>156°C | B.59°C - 80°C | C.<59°C | D.80°C- 156°C |
(4)本实验中,仪器a的容积最适合的是_______(填标号)。
| A.25 mL | B.50 mL | C.250 mL | D.500 mL |
II.待反应完成后,取出a装置中的混合物,设计如下流程分离、提纯溴苯:

(5)流程中“固体”的化学式为
(6)设计实验检验水洗是否达到目的:
(7)若经过操作III后得纯溴苯11. 30 g。则溴苯的产率是
更新时间:2022-04-22 10:29:10
|
相似题推荐
解答题-实验探究题
|
较难
(0.4)
【推荐1】实验室常用下图所示装置制取少量溴苯,并验证其中的一种产物。

请完成下列问题:
(1)在烧瓶a中装的试剂是________ 、________ 、________ 。
(2)导管c的下口能否浸没于液面下____________ ,理由是____________ 。
(3)反应过程中在导管c的下口附近可以观察到的现象是有_______ 出现,这是由于反应生成的_______ 遇水蒸气而形成的。
(4)反应完毕后,向锥形瓶d中滴加硝酸银溶液有________ 生成,反应的离子方程式是________

请完成下列问题:
(1)在烧瓶a中装的试剂是
(2)导管c的下口能否浸没于液面下
(3)反应过程中在导管c的下口附近可以观察到的现象是有
(4)反应完毕后,向锥形瓶d中滴加硝酸银溶液有
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐2】按下列合成步骤回答问题:
(1)在a中加入15mL无水苯和少量铁屑.在b中小心加入4.0mL液态溴.向a中滴入几滴溴,有白雾产生,继续滴加至液溴滴完.装置c的作用是_________ ,三颈烧瓶中反应的化学方程式为_____________________ ;
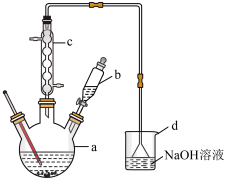
(2)液溴滴完后,经过下列步骤分离提纯:
①向a中加入10mL水,然后过滤除去未反应的铁屑;
②滤液依次用10mL水、8mL10%的NaOH溶液、10mL水洗涤.NaOH溶液洗涤的作用是__________ ;
③向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤.加入氯化钙的目的是_________ ;
(3)经以上分离操作后,粗溴苯中还含有的主要杂质为____________ ,要进一步提纯,下列操作中必须的是_________________ ;(填入正确选项前的字母)
A.结晶 B.过滤 C.蒸馏 D.萃取
(4)在该实验中,a的容积最适合的是____________ 。(填入正确选项前的字母)
A.25mL B.50mL C.250mL D.500mL
(1)在a中加入15mL无水苯和少量铁屑.在b中小心加入4.0mL液态溴.向a中滴入几滴溴,有白雾产生,继续滴加至液溴滴完.装置c的作用是

(2)液溴滴完后,经过下列步骤分离提纯:
①向a中加入10mL水,然后过滤除去未反应的铁屑;
②滤液依次用10mL水、8mL10%的NaOH溶液、10mL水洗涤.NaOH溶液洗涤的作用是
③向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤.加入氯化钙的目的是
(3)经以上分离操作后,粗溴苯中还含有的主要杂质为
A.结晶 B.过滤 C.蒸馏 D.萃取
(4)在该实验中,a的容积最适合的是
A.25mL B.50mL C.250mL D.500mL
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐3】溴苯是重要的有机合成中间体,下图为溴苯的制备实验装置:
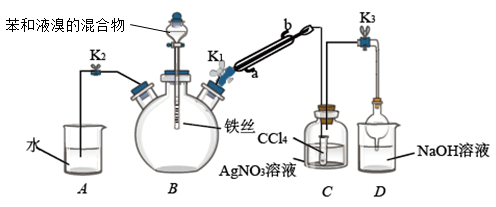
实验步骤:
I.检查气密性后,关闭K2,打开K1、K3和分液漏斗活塞,将苯和溴的混合物缓慢滴加到三颈烧瓶中,液体微沸,红色气体充满烧瓶,C装置小试管中无色液体逐渐变为橙红色,瓶内液面上方出现白雾。
II.关闭K1,打开K2,A中液体倒吸入B中。
II.拆除装置,将B中液体倒入盛有冷水的大烧杯中,分液,分别用NaOH溶液和水洗涤有机物,再加入MgSO4固体,过滤,最后将所得有机物进行蒸馏。
(1)K1、K3连接处均使用了乳胶管,其中不合理的是_______ (填“K1”或“K3”),理由是_______ 。
(2)可以证明溴和苯的反应是取代而不是加成的实验现象是_______ 。
(3)步骤I的目的是_______ 。
(4)用NaOH洗涤有机物时发生反应的离子方程式为_______ 。
(5)步骤II中的蒸馏操作可用如下的减压蒸馏装置(加热装置和夹持装置已略)。
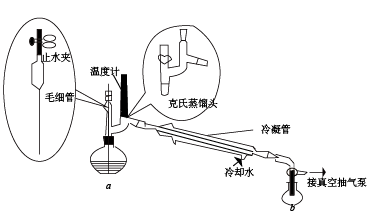
①实验前,烧瓶中无需加入碎瓷片,实验过程中打开毛细管上端的止水夹时,a中的现象是_______ ;毛细管的作用是_______ 。
②使用克氏蒸馏头的优点是_______ 。

实验步骤:
I.检查气密性后,关闭K2,打开K1、K3和分液漏斗活塞,将苯和溴的混合物缓慢滴加到三颈烧瓶中,液体微沸,红色气体充满烧瓶,C装置小试管中无色液体逐渐变为橙红色,瓶内液面上方出现白雾。
II.关闭K1,打开K2,A中液体倒吸入B中。
II.拆除装置,将B中液体倒入盛有冷水的大烧杯中,分液,分别用NaOH溶液和水洗涤有机物,再加入MgSO4固体,过滤,最后将所得有机物进行蒸馏。
(1)K1、K3连接处均使用了乳胶管,其中不合理的是
(2)可以证明溴和苯的反应是取代而不是加成的实验现象是
(3)步骤I的目的是
(4)用NaOH洗涤有机物时发生反应的离子方程式为
(5)步骤II中的蒸馏操作可用如下的减压蒸馏装置(加热装置和夹持装置已略)。

①实验前,烧瓶中无需加入碎瓷片,实验过程中打开毛细管上端的止水夹时,a中的现象是
②使用克氏蒸馏头的优点是
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
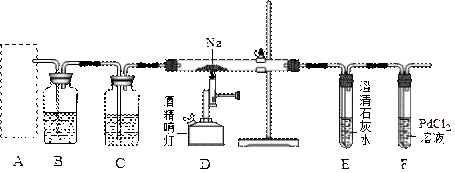
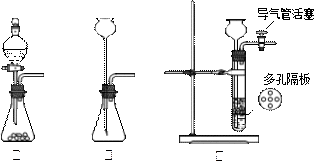
【推荐1】某兴趣小组的学生根据活泼金属Mg与CO2发生反应,推测活泼金属钠也能与CO2发生反应,因此兴趣小组用下列装置进行“钠与二氧化碳反应”的实验探究(尾气处理装置已略去)。已知:常温下,CO能使一些化合物中的金属离子还原
例如:PdCl2 + CO + H2O=Pd↓+ CO2+2HCl 。反应生成黑色的金属钯,此反应也可用来检测微量CO的存在。
请回答下列问题:
(1)通常实验室制取CO2气体的离子方程式是_______________________________ ,为了使制气装置能“随开随用,随关随停”,上图A处应选用的装置是_____ (填写 “Ⅰ”、“Ⅱ”或“Ⅲ”)。若要制取干燥、纯净的CO2气体,装置B中应盛放的试剂是____________ 溶液,装置C中应盛放的试剂是______________ 。
(2)观察实验装置图可知Na与CO2反应的条件是_____________ 。检查装置的气密性完好并装入药品后,在点燃酒精喷灯前,必须进行的操作是____________________ 。待装置______ (填写字母)中出现____________________ 现象时,再点燃酒精喷灯,这步操作的目的是______________________________________ 。
(3)假设CO2气体为足量,在实验过程中分别产生以下①、②两种不同情况,请分析并回答问题:
①若装置F中溶液无明显变化,装置D中生成两种固体物质,取少量固体生成物与盐酸反应后,有能使澄清石灰水变浑浊的气体放出,则钠与二氧化碳反应的化学方程式是_______________________ 。
②若装置F中有黑色沉淀生成,装置D中只生成一种固体物质,取少量该固体与盐酸反应后,也有能使澄清石灰水变浑浊的气体放出,则钠与二氧化碳反应的化学方程式是__________________________ 。
(4)请用文字简要说明你判断②中D装置生成固体的成分是钠的正盐或酸式盐的理由。_________________________________ 。

例如:PdCl2 + CO + H2O=Pd↓+ CO2+2HCl 。反应生成黑色的金属钯,此反应也可用来检测微量CO的存在。


请回答下列问题:
(1)通常实验室制取CO2气体的离子方程式是
(2)观察实验装置图可知Na与CO2反应的条件是
(3)假设CO2气体为足量,在实验过程中分别产生以下①、②两种不同情况,请分析并回答问题:
①若装置F中溶液无明显变化,装置D中生成两种固体物质,取少量固体生成物与盐酸反应后,有能使澄清石灰水变浑浊的气体放出,则钠与二氧化碳反应的化学方程式是
②若装置F中有黑色沉淀生成,装置D中只生成一种固体物质,取少量该固体与盐酸反应后,也有能使澄清石灰水变浑浊的气体放出,则钠与二氧化碳反应的化学方程式是
(4)请用文字简要说明你判断②中D装置生成固体的成分是钠的正盐或酸式盐的理由。
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐2】苯乙酮(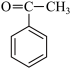 )广泛用于皂用香精中,可由苯和乙酸酐(
)广泛用于皂用香精中,可由苯和乙酸酐(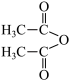 )制备。
)制备。
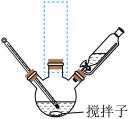
已知:
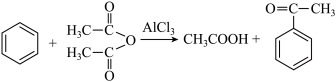
步骤I 向三颈烧瓶中加入39 g苯和44.5 g无水氯化铝,在搅拌下滴加25.5 g乙酸酐,在70~80℃下加热45min,发生反应如下:
步骤II 冷却后将反应物倒入100g冰水中,有白色胶状沉淀Al(OH)3生成,采用合适的方法处理,水层用苯萃取,合并苯层溶液,再依次用30 mL 5% NaOH溶液和30 mL水洗涤,分离出的苯层用无水硫酸镁干燥。
步骤III 常压蒸馏回收苯,再收集产品苯乙酮。
请回答下列问题:
(1)AlCl3在反应中作用_________ ;步骤I中的加热方式为_________ 。
(2)根据上述实验药品的用量,三颈烧瓶的最适宜规格为_________ (填标号)。
(3)图示实验装置虚线框内缺少一种仪器,该仪器的作用为_________ 。
(4)步骤II中用NaOH溶液洗涤的目的是_________ 。
(5)步骤III中将苯乙酮中的苯分离除去所需的最低温度为_________ 。
(6)实验中收集到24.0 mL苯乙酮,则苯乙酮的产率为_________ (保留三位有效数字)。
(7)已知: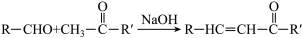 。苯乙酮(
。苯乙酮( )和苯甲醛(
)和苯甲醛(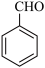 )在NaOH催化下可以合成查尔酮,查尔酮的结构简式为
)在NaOH催化下可以合成查尔酮,查尔酮的结构简式为_________ 。
 )广泛用于皂用香精中,可由苯和乙酸酐(
)广泛用于皂用香精中,可由苯和乙酸酐( )制备。
)制备。
已知:
| 名称 | 相对分子质量 | 熔点/℃ | 沸点/℃ | 密度/(g·mL-1 ) | 溶解性 |
| 苯 | 78 | 5.5 | 80.1 | 0.88 | 不溶于水,易溶于有机溶剂 |
| 苯乙酮 | 120 | 19.6 | 203 | 1.03 | 微溶于水,易溶于有机溶剂 |
| 乙酸酐 | 102 | -73 | 139 | 1.08 | 有吸湿性,易溶于有机溶剂 |
| 乙酸 | 60 | 16.6 | 118 | 1.05 | 易溶于水,易溶于有机溶剂 |

步骤II 冷却后将反应物倒入100g冰水中,有白色胶状沉淀Al(OH)3生成,采用合适的方法处理,水层用苯萃取,合并苯层溶液,再依次用30 mL 5% NaOH溶液和30 mL水洗涤,分离出的苯层用无水硫酸镁干燥。
步骤III 常压蒸馏回收苯,再收集产品苯乙酮。
请回答下列问题:
(1)AlCl3在反应中作用
(2)根据上述实验药品的用量,三颈烧瓶的最适宜规格为_________ (填标号)。
| A.100 mL | B.250 mL | C.500 mL | D.1000 mL |
(4)步骤II中用NaOH溶液洗涤的目的是
(5)步骤III中将苯乙酮中的苯分离除去所需的最低温度为
(6)实验中收集到24.0 mL苯乙酮,则苯乙酮的产率为
(7)已知:
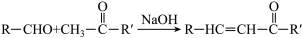 。苯乙酮(
。苯乙酮( )和苯甲醛(
)和苯甲醛( )在NaOH催化下可以合成查尔酮,查尔酮的结构简式为
)在NaOH催化下可以合成查尔酮,查尔酮的结构简式为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐3】单晶硅是信息产业中重要的基础材料。通常用炭在高温下还原二氧化硅制得粗硅(含铁、铝、硼、磷等杂质),粗硅与氯气反应生成四氯化硅(反应温度450~500℃),四氯化硅经提纯后用氢气还原可得高纯硅。以下是实验室制备四氯化硅的装置示意图。
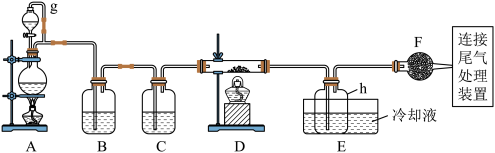
相关信息:①四氯化硅遇水极易水解;② 沸点为57.7℃,熔点为-70.0℃。请回答:
沸点为57.7℃,熔点为-70.0℃。请回答:
(1)写出装置A中发生反应的离子方程式______ 。
(2)装置C中的试剂是______ ;装置F的作用是______ ;装置E中的h瓶需要冷却的理由是______ 。
(3)装置E中h瓶收集到的粗产物可通过精馏(类似多次蒸馏)得到高纯度四氯化硅,精馏后的残留物中含有铁元素,为了分析残留物中铁元素的含量,先将残留物预处理,使铁元素还原成Fe2+,再用KMnO4标准溶液在酸性条件下进行氧化还原滴定。
①反应的离子方程式:______ 。
②滴定前是否要滴加指示剂?______ (填“是”或“否”),请说明理由______ 。
③滴定前检验Fe3+是否被完全还原的实验操作是______ 。

相关信息:①四氯化硅遇水极易水解;②
 沸点为57.7℃,熔点为-70.0℃。请回答:
沸点为57.7℃,熔点为-70.0℃。请回答:(1)写出装置A中发生反应的离子方程式
(2)装置C中的试剂是
(3)装置E中h瓶收集到的粗产物可通过精馏(类似多次蒸馏)得到高纯度四氯化硅,精馏后的残留物中含有铁元素,为了分析残留物中铁元素的含量,先将残留物预处理,使铁元素还原成Fe2+,再用KMnO4标准溶液在酸性条件下进行氧化还原滴定。
①反应的离子方程式:
②滴定前是否要滴加指示剂?
③滴定前检验Fe3+是否被完全还原的实验操作是
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
【推荐1】油脂厂油脂氢化的催化剂(主要含金属 、
、 、
、 及其氧化物,还有少量其他不溶性物质。)废弃后可采用如图工艺流程回收其中的镍制备硫酸镍晶体(
及其氧化物,还有少量其他不溶性物质。)废弃后可采用如图工艺流程回收其中的镍制备硫酸镍晶体(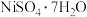 ):
):

溶液中金属离子开始沉淀和完全沉淀的 如表所示:
如表所示:
回答下列问题:
(1)“碱浸”中 的两个作用分别是
的两个作用分别是___________ 。为回收金属,用稀硫酸将“滤液①”调为中性,生成沉淀。写出该反应的离子方程式___________ 。
(2)“转化”中的离子方程式___________ 。
(3)利用上述表格数据,计算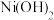


___________ 。如果“转化”后的溶液中 浓度为
浓度为 ,则“调
,则“调 ”应控制的
”应控制的 范围是
范围是___________ 。
(4)硫酸镍在强碱溶液中用 氧化,可沉淀出能用作镍镉电池正极材料的
氧化,可沉淀出能用作镍镉电池正极材料的 。写出该反应的离子方程式
。写出该反应的离子方程式___________ 。写出镍镉电池(碱性)正极的电极方程式___________
 、
、 、
、 及其氧化物,还有少量其他不溶性物质。)废弃后可采用如图工艺流程回收其中的镍制备硫酸镍晶体(
及其氧化物,还有少量其他不溶性物质。)废弃后可采用如图工艺流程回收其中的镍制备硫酸镍晶体(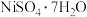 ):
):
溶液中金属离子开始沉淀和完全沉淀的
 如表所示:
如表所示:| 金属离子 |  |  |  |  |
开始沉淀时(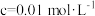 )的 )的 | 7.2 | 3.7 | 2.2 | 7.5 |
沉淀完全时( )的 )的 | 8.7 | 4.7 | 3.2 | 9.0 |
(1)“碱浸”中
 的两个作用分别是
的两个作用分别是(2)“转化”中的离子方程式
(3)利用上述表格数据,计算
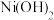


 浓度为
浓度为 ,则“调
,则“调 ”应控制的
”应控制的 范围是
范围是(4)硫酸镍在强碱溶液中用
 氧化,可沉淀出能用作镍镉电池正极材料的
氧化,可沉淀出能用作镍镉电池正极材料的 。写出该反应的离子方程式
。写出该反应的离子方程式
您最近一年使用:0次
【推荐2】铋主要用于制造合金,铋合金具有凝固时不收缩的特性,用于铸造印刷铅字和高精度铸型。湿法提铋新工艺以氧化铋渣(主要成分为Bi2O3,含有PbO、Ag2O、CuO)为原料提取Bi的工艺流程如下:
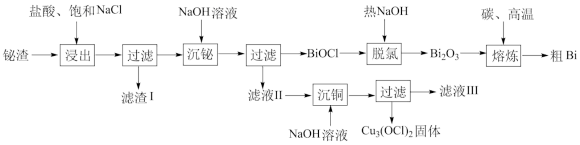
已知:Ⅰ.BiCl3可水解生成不溶于水的BiOCl
Ⅱ.25℃时,Ksp[Cu(OH)2]=1.2×10-20;Ksp(PbCl2)=1.17×10-5。
回答下列问题:
(1)“浸出”时,若c(HCl)=1mol/L时,铋的浸出率和Cl-浓度的关系如图所示,其中NaCl的作用是___________ ;若升高温度,反应相同的时间,铋的浸出率先升高后降低,则浸出率下降的主要原因可能是HCl挥发和___________ 。

(2)“滤渣Ⅰ”的成分为___________ (填化学式)。
(3)“脱氯”的化学方程式为___________ 。
(4)“沉铜”时向“滤液Ⅱ”中加入NaOH溶液,可促进Cu2+水解生成Cu3(OCl)2沉淀,请写出“沉铜”的离子方程式___________ 。若“滤液Ⅱ”中c(Cu2+)为0.01mol·L-1,常温下加入等体积的NaOH溶液使pH恰好为6时,出现Cu(OH)2沉淀,此时Cu2+的去除率为___________ (忽略溶液体积变化)。
(5)可循环利用的物质是___________ 。
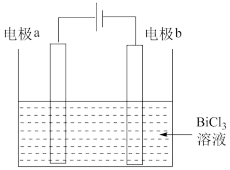
(6)粗铋可通过电解法进行精炼,其原理如图所示,其中电极a的材料是___________ ,电极b上发生的电极反应为___________ 。

已知:Ⅰ.BiCl3可水解生成不溶于水的BiOCl
Ⅱ.25℃时,Ksp[Cu(OH)2]=1.2×10-20;Ksp(PbCl2)=1.17×10-5。
回答下列问题:
(1)“浸出”时,若c(HCl)=1mol/L时,铋的浸出率和Cl-浓度的关系如图所示,其中NaCl的作用是

(2)“滤渣Ⅰ”的成分为
(3)“脱氯”的化学方程式为
(4)“沉铜”时向“滤液Ⅱ”中加入NaOH溶液,可促进Cu2+水解生成Cu3(OCl)2沉淀,请写出“沉铜”的离子方程式
(5)可循环利用的物质是
(6)粗铋可通过电解法进行精炼,其原理如图所示,其中电极a的材料是

您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐3】用金属钴板(含少量Fe、Ni)制备应用广泛的氯化钴的工艺流程如下:
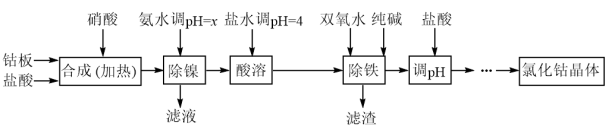
注:钴与盐酸反应极慢,需加入催化剂硝酸才可能进行实际生产。
有关钴、镍和铁化合物的性质见下表:
(1)“除镍”步骤中,NH3·H2O用量对反应收率的影响见表中数据:从表中数据可知,当PH调节至x=_______ 时,除镍效果最好。
(2)“除镍”步骤必须控制在一定的时间内完成,否则沉淀中将有部分Co(OH)2转化为Co(OH)3,此反应的化学方程式为________________ 。
(3)“除铁”步骤中加入双氧水发生反应的离子方程式是________________________ 。
(4)“除铁”步骤中加入的纯碱作用是________________________________ 。
(5)在“调pH”步骤中,加盐酸的作用是______________________________ 。
(6)已知25℃时,Ksp[Fe(OH)3]=4.0×10-38,则该温度下反应Fe3++3H2O Fe(OH)3+3H+的平衡常数为
Fe(OH)3+3H+的平衡常数为_____________________ 。

注:钴与盐酸反应极慢,需加入催化剂硝酸才可能进行实际生产。
有关钴、镍和铁化合物的性质见下表:
| 化学式 | 沉淀完全时的pH | 钴镍性质 |
| Co(OH)2 | 9.4 | Co+2HCl=CoCl2+H2↑ Co2++2NH3·H2O=Co(OH)2↓+2NH4+ Co2++2H2O  Co(OH)2+2H+ Co(OH)2+2H+Ni+2HCl=NiCl2+H2↑ Ni2++6NH3·H2O=[Ni(NH3)6]2++6H2O |
| Fe(OH)2 | 9.6 | |
| Fe (OH)3 | 3.7 |
| 加NH3·H2O调pH | 收率/% | Ni2+含量/% |
| 9 | 98.1 | 0.08 |
| 9.5 | 98 | 0.05 |
| 10 | 97.6 | 0.005 |
| 10.3 | 94 | 0.005 |
(3)“除铁”步骤中加入双氧水发生反应的离子方程式是
(4)“除铁”步骤中加入的纯碱作用是
(5)在“调pH”步骤中,加盐酸的作用是
(6)已知25℃时,Ksp[Fe(OH)3]=4.0×10-38,则该温度下反应Fe3++3H2O
 Fe(OH)3+3H+的平衡常数为
Fe(OH)3+3H+的平衡常数为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐1】[Co(NH3)6]Cl3是科研、化工上常用的化学试剂,水溶液中存在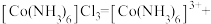 3C1-,在强碱热溶液中可以生成NH3.下面是[Co(NH3)6]Cl3的制备及生成物组成的测定实验,回答下列问题:
3C1-,在强碱热溶液中可以生成NH3.下面是[Co(NH3)6]Cl3的制备及生成物组成的测定实验,回答下列问题:
I、[Co(NH3)6]Cl3的制备
如图所示,在三颈烧瓶中将6.0g CoCl2·6H2O晶体溶解在氯化铵溶液中,并加入适量的活性炭作催化剂,通入氨气并逐滴滴加5% H2O2溶液。加热到40℃并搅拌,会有橙黄色晶体([Co(NH3)6]Cl3)析出。

(1)仪器X的名称为_______ ,放入的化学试剂为_______ 。
(2)装置中制备氨气时不宜选取 NH4NO3与NaOH反应,原因是_______ (答1条即可)。
(3)写出生成[Co(NH3)6]Cl3的化学方程式:_______ 。
(4)充分反应后,某学生实验得到[Co(NH3)6]Cl3的实际质量为3.72 g,比理论值少_______ g。
Ⅱ.三氯化六氨合钴(II)组成的测定
(5)氨的测定。准确称取0.2g[Co(NH3)6]Cl3在热强碱下反应生成氨气,产生的氨气被H3BO3溶液完全吸收,滴加5~6滴甲基红溴甲酚氯指示剂,再用标准的盐酸滴定吸收了氨气的H3BO3溶液即可得出氨的含量(已知:NH3+H3BO3=NH3·H3BO3;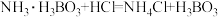 )。下列操作(其他步骤操作均正确)会造成氨的测定值偏高的是
)。下列操作(其他步骤操作均正确)会造成氨的测定值偏高的是_______ (填字母代号)。
a.滴定结束时仰视读数
b.锥形瓶清洗后未干燥
c.滴定前滴定管中含有气泡,滴定结束无气泡
d.未使用标准盐酸溶液润洗滴定管
(6)氯的测定。用标准AgNO3溶液迪过沉淀滴定法测定门的量。适宜选取_______ 作指示剂。滴定终点现象为_______ 已知Ksp(AgBr) =4.9×10-13.,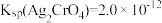 ,
,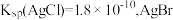 为黄色沉淀,
为黄色沉淀, 为砖红色沉淀)。
为砖红色沉淀)。
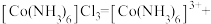 3C1-,在强碱热溶液中可以生成NH3.下面是[Co(NH3)6]Cl3的制备及生成物组成的测定实验,回答下列问题:
3C1-,在强碱热溶液中可以生成NH3.下面是[Co(NH3)6]Cl3的制备及生成物组成的测定实验,回答下列问题:I、[Co(NH3)6]Cl3的制备
如图所示,在三颈烧瓶中将6.0g CoCl2·6H2O晶体溶解在氯化铵溶液中,并加入适量的活性炭作催化剂,通入氨气并逐滴滴加5% H2O2溶液。加热到40℃并搅拌,会有橙黄色晶体([Co(NH3)6]Cl3)析出。

(1)仪器X的名称为
(2)装置中制备氨气时不宜选取 NH4NO3与NaOH反应,原因是
(3)写出生成[Co(NH3)6]Cl3的化学方程式:
(4)充分反应后,某学生实验得到[Co(NH3)6]Cl3的实际质量为3.72 g,比理论值少
Ⅱ.三氯化六氨合钴(II)组成的测定
(5)氨的测定。准确称取0.2g[Co(NH3)6]Cl3在热强碱下反应生成氨气,产生的氨气被H3BO3溶液完全吸收,滴加5~6滴甲基红溴甲酚氯指示剂,再用标准的盐酸滴定吸收了氨气的H3BO3溶液即可得出氨的含量(已知:NH3+H3BO3=NH3·H3BO3;
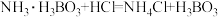 )。下列操作(其他步骤操作均正确)会造成氨的测定值偏高的是
)。下列操作(其他步骤操作均正确)会造成氨的测定值偏高的是a.滴定结束时仰视读数
b.锥形瓶清洗后未干燥
c.滴定前滴定管中含有气泡,滴定结束无气泡
d.未使用标准盐酸溶液润洗滴定管
(6)氯的测定。用标准AgNO3溶液迪过沉淀滴定法测定门的量。适宜选取
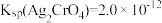 ,
,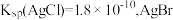 为黄色沉淀,
为黄色沉淀, 为砖红色沉淀)。
为砖红色沉淀)。
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐2】牙膏是常见的日用化学品。磨擦剂是牙膏的主体原料,在牙膏中最重要的作用就是去除牙垢,减轻牙结石。
I.完成下列问题。
(1)下表列出了牙膏中常见的摩擦剂,请写出它们所属的物质类别(填“酸”“碱”“盐”或“氧化物”)。
(2)根据用途推测 在水中的溶解性:
在水中的溶解性:_______ (填“易溶”或“难溶”)。
(3)牙膏中的摩擦剂氢氧化镁可以用菱镁矿(主要成分为 、
、 、
、 、
、 )来制备,按要求回答下列问题。
)来制备,按要求回答下列问题。_______ (填字母)。
A.菱镁矿 B. C.
C. D.
D. E.硫酸钙 F.氨
E.硫酸钙 F.氨
②方案中可循环利用的物质有_______ (填化学式)。
II.某牙膏摩擦剂的成分为 ,为测定其中
,为测定其中 的含量的操作如下(设该牙膏中的其他成分不与盐酸或者氢氧化钠反应):
的含量的操作如下(设该牙膏中的其他成分不与盐酸或者氢氧化钠反应):
①配制 稀盐酸和
稀盐酸和 NaOH溶液;
NaOH溶液;
②称取0.60g该牙膏,溶于水并稀释至20.00mL;
③用 NaOH溶液中和过量的稀盐酸,记录所消耗氢氧化钠溶液的体积;
NaOH溶液中和过量的稀盐酸,记录所消耗氢氧化钠溶液的体积;
④加入25.00mL 稀盐酸;
稀盐酸;
(4)正确的操作顺序为①_______ (填标号)。
(5)该测定实验共进行了4次,实验室现有50mL、100mL、250mL、500mL4种规格的容量瓶,则配制盐酸应选用的容量瓶规格为_______ 。
(6)某同学4次测定所消耗NaOH溶液的体积如下:
则该牙膏中碳酸钙的质量分数约为_______ (保留三位有效数字)%。
I.完成下列问题。
(1)下表列出了牙膏中常见的摩擦剂,请写出它们所属的物质类别(填“酸”“碱”“盐”或“氧化物”)。
| 摩擦剂成分 | 氢氧化镁 | 碳酸钙 | 二氧化硅 |
| 物质类别 | ① | ② |
 在水中的溶解性:
在水中的溶解性:(3)牙膏中的摩擦剂氢氧化镁可以用菱镁矿(主要成分为
 、
、 、
、 、
、 )来制备,按要求回答下列问题。
)来制备,按要求回答下列问题。
A.菱镁矿 B.
 C.
C. D.
D. E.硫酸钙 F.氨
E.硫酸钙 F.氨②方案中可循环利用的物质有
II.某牙膏摩擦剂的成分为
 ,为测定其中
,为测定其中 的含量的操作如下(设该牙膏中的其他成分不与盐酸或者氢氧化钠反应):
的含量的操作如下(设该牙膏中的其他成分不与盐酸或者氢氧化钠反应):①配制
 稀盐酸和
稀盐酸和 NaOH溶液;
NaOH溶液;②称取0.60g该牙膏,溶于水并稀释至20.00mL;
③用
 NaOH溶液中和过量的稀盐酸,记录所消耗氢氧化钠溶液的体积;
NaOH溶液中和过量的稀盐酸,记录所消耗氢氧化钠溶液的体积;④加入25.00mL
 稀盐酸;
稀盐酸;(4)正确的操作顺序为①
(5)该测定实验共进行了4次,实验室现有50mL、100mL、250mL、500mL4种规格的容量瓶,则配制盐酸应选用的容量瓶规格为
(6)某同学4次测定所消耗NaOH溶液的体积如下:
| 实验标号 | 1 | 2 | 3 | 4 |
| V(NaOH)/mL | 10.10 | 9.90 | 10.20 | 9.80 |
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐3】纯碱是一种重要的化工原料,具有广泛的用途。实验室利用氯化钠和碳酸氢铵制备纯碱并测定产品中碳酸氢钠的含量,具体步骤如下:
步骤i.精制氯化钠
取饱和粗盐水并加热,向其中加入饱和 溶液调节pH至11,有大量胶状沉淀析出;继续加热至沸,趁热过滤,滤液用盐酸调节pH至7。
溶液调节pH至11,有大量胶状沉淀析出;继续加热至沸,趁热过滤,滤液用盐酸调节pH至7。
步骤ⅱ.制备纯碱
在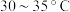 水浴条件下,向上述滤液中加入碳酸氢铵粉末,搅拌至反应完全;冷却后过滤得到碳酸氢钠晶体;用碳酸氢钠饱和过的酒精水溶液洗涤晶体;加热使其分解得到产品。
水浴条件下,向上述滤液中加入碳酸氢铵粉末,搅拌至反应完全;冷却后过滤得到碳酸氢钠晶体;用碳酸氢钠饱和过的酒精水溶液洗涤晶体;加热使其分解得到产品。
步骤ⅲ.产品中碳酸氢钠含量的测定
称取a g产品加水溶解,滴加指示剂M,用 盐酸逐滴滴定,并不断振荡,到达终点时消耗盐酸
盐酸逐滴滴定,并不断振荡,到达终点时消耗盐酸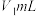 ;滴加指示剂N,继续用上述盐酸滴定,到达终点时消耗盐酸总体积
;滴加指示剂N,继续用上述盐酸滴定,到达终点时消耗盐酸总体积 。
。
已知:相关物质的溶解度如下
说明:“—”表示该物质在相应温度下已开始分解。
回答下列问题:
(1)步骤ⅰ中,胶状沉淀的成分为 ,生成该沉淀的离子方程式为
,生成该沉淀的离子方程式为________________ ;
(2)步骤ⅰ中,沉淀析出后需继续加热煮沸一段时间,其目的为________________ ;
(3)步骤ⅱ中,选择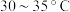 水浴的原因为
水浴的原因为________________ ;
(4)步骤ⅱ中,用碳酸氢钠饱和过的酒精水溶液洗涤晶体可除去的杂质为________________ ;
(5)步骤ⅲ中,用到的玻璃仪器除胶头滴管外还需要下列仪器中的________ (填仪器名称);________ ;滴定过程中,盐酸需要逐滴加入并不断振荡的原因为________________ ;选择指示剂N时,滴定终点溶液颜色变化为________________ ;
(7)产品中碳酸氢钠的质量分数为________ (用含字母的代数式表示)。
步骤i.精制氯化钠
取饱和粗盐水并加热,向其中加入饱和
 溶液调节pH至11,有大量胶状沉淀析出;继续加热至沸,趁热过滤,滤液用盐酸调节pH至7。
溶液调节pH至11,有大量胶状沉淀析出;继续加热至沸,趁热过滤,滤液用盐酸调节pH至7。步骤ⅱ.制备纯碱
在
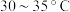 水浴条件下,向上述滤液中加入碳酸氢铵粉末,搅拌至反应完全;冷却后过滤得到碳酸氢钠晶体;用碳酸氢钠饱和过的酒精水溶液洗涤晶体;加热使其分解得到产品。
水浴条件下,向上述滤液中加入碳酸氢铵粉末,搅拌至反应完全;冷却后过滤得到碳酸氢钠晶体;用碳酸氢钠饱和过的酒精水溶液洗涤晶体;加热使其分解得到产品。步骤ⅲ.产品中碳酸氢钠含量的测定
称取a g产品加水溶解,滴加指示剂M,用
 盐酸逐滴滴定,并不断振荡,到达终点时消耗盐酸
盐酸逐滴滴定,并不断振荡,到达终点时消耗盐酸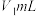 ;滴加指示剂N,继续用上述盐酸滴定,到达终点时消耗盐酸总体积
;滴加指示剂N,继续用上述盐酸滴定,到达终点时消耗盐酸总体积 。
。已知:相关物质的溶解度如下
温度 | 10 | 20 | 30 | 40 | 50 | 60 | 70 |
| 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 37.8 |
| 15.8 | 21.0 | 27.0 | — | — | — | — |
| 8.15 | 9.6 | 11.1 | 12.7 | 14.5 | 16.4 | — |
| 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.2 | 60.2 |
回答下列问题:
(1)步骤ⅰ中,胶状沉淀的成分为
 ,生成该沉淀的离子方程式为
,生成该沉淀的离子方程式为(2)步骤ⅰ中,沉淀析出后需继续加热煮沸一段时间,其目的为
(3)步骤ⅱ中,选择
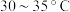 水浴的原因为
水浴的原因为(4)步骤ⅱ中,用碳酸氢钠饱和过的酒精水溶液洗涤晶体可除去的杂质为
(5)步骤ⅲ中,用到的玻璃仪器除胶头滴管外还需要下列仪器中的
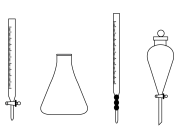
(7)产品中碳酸氢钠的质量分数为
您最近一年使用:0次







