纯碱在生产、生活中有广泛应用。工业上,用纯碱溶液从海水中提取溴,氯气置换海水中溴之后,富集、提取溴的主要原理是:
反应1:3Br2+3Na2CO3=NaBrO3+5NaBr+3CO2↑;
反应2:NaBrO3+5NaBr+3H2SO4=3Na2SO4+3Br2+3H2O;
反应3:实验室里用纯碱溶液吸收尾气中的氯气生成三种盐。
下列说法正确的是
反应1:3Br2+3Na2CO3=NaBrO3+5NaBr+3CO2↑;
反应2:NaBrO3+5NaBr+3H2SO4=3Na2SO4+3Br2+3H2O;
反应3:实验室里用纯碱溶液吸收尾气中的氯气生成三种盐。
下列说法正确的是
| A.反应1中氧化剂、还原剂的质量之比为1:5 |
| B.标准状况下,22.4L溴单质含2mol溴原子 |
| C.反应3中的三种盐是NaClO、NaClO3和NaHCO3 |
| D.反应1中Br2的作用类似于反应3中的Cl2 |
2022·湖南娄底·模拟预测 查看更多[5]
湖南省娄底市2022届高考仿真模拟考试化学试题(已下线)专题04 氧化还原反应-三年(2020-2022)高考真题分项汇编(已下线)专题04 氧化还原反应-2022年高考真题模拟题分项汇编湖南省岳阳市临湘市2021-2022学年高一下学期期末教学质量检测化学试题(已下线)微专题19 海水资源的综合利用(提取溴和碘)-备战2023年高考化学一轮复习考点微专题
更新时间:2022-04-23 17:35:53
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】设NA为阿伏加德罗常数的值,下列判断正确的是
| A.60g乙酸与足量乙醇发生酯化反应,充分反应后断裂的C-O键数目为NA |
| B.2.3g金属钠与足量乙醇反应,产生11.2L氢气 |
| C.高温下,5.6gFe与足量硫单质反应,转移的电子数为0.2NA |
| D.标准状况下,2.24LCl2与2.24LCH4混合后光照反应,得到0.1NA个CH3Cl |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】用NA表示阿伏加德罗常数的值,下列叙述正确的是
| A.标准状况下,2.24LH2O中含有的原子数为0.3NA |
| B.16g由O2和O3组成的混合物中含有的氧原子数为2NA |
| C.78gNa2O2粉末中含有2NA个阴离子 |
| D.100mL0.1mol/L的H2SO4溶液中含有的硫原子数为0.01NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】NA表示阿伏加德罗常数,下列叙述不正确的是
| A.标准状况下,22.4 L CO2和He的混合气体中含有的分子数为NA |
| B.常温常压下,2.8g N2和CO的混合气中原子数为0.2 NA |
| C.3.4g的OH-中含有的电子数为2 NA |
| D.1 mol/L的Na2CO3溶液中含有的钠离子数为2 NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】二氧化氯(ClO2 )是一种安全的绿色消毒剂,实验室可用下列方法制备:
①电解NH4Cl的盐酸溶液制得NCl3(N元素为-3价)溶液;
②将NCl3溶液与NaClO2溶液混合制得ClO2。
下列说法正确的是
①电解NH4Cl的盐酸溶液制得NCl3(N元素为-3价)溶液;
②将NCl3溶液与NaClO2溶液混合制得ClO2。
下列说法正确的是
| A.①中在电解池的阴极得到NCl3 |
| B.组成①中的电解池除需要有电源、导线和大烧杯等,还必须有两个不同材质的电极 |
| C.②中反应的氧化剂与还原剂的物质的量之比是6:1 |
| D.②中反应后的溶液中主要存在的阳离子是Na+ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】水体中过量氨氮(以NH3表示)含量过高会导致水体富营养化。用次氯酸钠除去氨氮的一种原理如图所示。下列说法正确的是

| A.过程①②③均属于氧化还原反应 |
B.该过程的总反应为: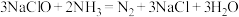 |
| C.过程②中氧化剂与还原剂的个数之比是2:3 |
| D.在较高温度下,氨氮去除率会更好 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】解释下列事实的方程式不正确 的是
| A.将二氧化硫通入硝酸钡溶液中,产生白色沉淀:SO2+Ba2++H2O=BaSO3↓+2H+ |
B.将碳酸氢钠溶液与氯化钙溶液混合,产生白色沉淀:2HCO +Ca2+=CaCO3↓+H2O+CO2↑ +Ca2+=CaCO3↓+H2O+CO2↑ |
C.将氯化铜溶液加热,溶液由蓝色变为绿色:[Cu(H2O)4]2+(aq)+4Cl—(aq) [CuCl4]2—(aq)+4H2O(l) △H>0 [CuCl4]2—(aq)+4H2O(l) △H>0 |
| D.用氢氧化钠溶液吸收氯气:Cl2+2OH—=Cl—+ClO—+H2O |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】某同学用下列装置进行实验,有关说法错误的是
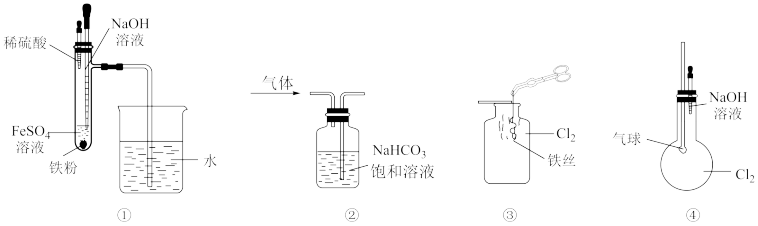

A.利用装置①可以较长时间看到 白色沉淀 白色沉淀 |
B.装置②可以除去 中的HCl气体 中的HCl气体 |
| C.装置③中生成棕黄色的烟,加少量水溶解,得到棕黄色溶液 |
D.装置④中若气球明显膨胀,证明 与NaOH溶液反应 与NaOH溶液反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】工业上把Cl2通入冷NaOH溶液中制得漂白液(主要成分NaClO)。某化学小组在一定温度下将氯气缓缓通入NaOH溶液,模拟实验得到ClO-、ClO3-等离子其物质的量(mol)与反应时间t(min)的关系曲线.下列说法错误的是
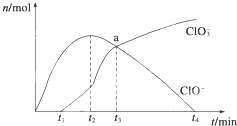

| A.参加反应所需NaOH与氯气的物质的量之比一定为2:1 |
| B.a点时溶液中n(NaCl):n(NaClO3):n(NaClO)=6:1:1 |
| C.t2~t4,ClO-离子的物质的量下降的原因可能是3ClO-=2Cl-+ClO3- |
| D.使用漂白液时,为了增强漂白效果,可以向漂白液中加入浓盐酸 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】我国海洋资源十分丰富。下列各组物质可以通过物理法直接从海水中提取的是
| A.氯气、碘 | B.粗盐、淡水 | C.烧碱、氢气 | D.钠、镁、铝 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】解释下列事实的化学方程式或离子方程式正确的是
A.用石英和焦炭制取粗硅:SiO2+C Si+CO2 Si+CO2 |
| B.氢氟酸雕刻玻璃发生的离子反应:4H++4F-+SiO2=SiF4↑+2H2O |
C.海水提碘时,反萃取反应的化学方程式为: |
| D.单质铝溶于烧碱溶液中:2Al+8NaOH+6H2O=2Na[Al(OH)4]+2H2↑ |
您最近一年使用:0次

 )是重要的化学试剂,其与氧气的反应如下:
)是重要的化学试剂,其与氧气的反应如下: 。下列说法正确的是
。下列说法正确的是
 ,转移电子数是
,转移电子数是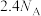
 是氧化产物
是氧化产物


