将32.64g铜与140mL一定浓度的硝酸反应,铜完全溶解产生的NO和NO2混合气体在标准状况下的体积为11.2L。请回答:
(1)NO的体积为_____ L,NO2的体积为______ L。
(2)参加反应的硝酸的物质的量是_______ mol。
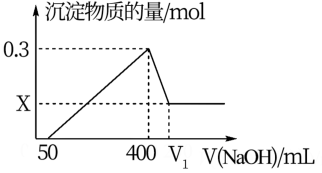
(3)待产生的气体全部释放后,向溶液加入VmL a mol/L的NaOH溶液,恰好使溶液中的Cu2+全部转化成沉淀,则原硝酸溶液的浓度为___________ mol/L。(结果不需化简)
(4)欲使铜与硝酸反应生成的气体在NaOH溶液中全部转化为NaNO3,至少需要30%的双氧水________ g。
(1)NO的体积为
(2)参加反应的硝酸的物质的量是
(3)待产生的气体全部释放后,向溶液加入VmL a mol/L的NaOH溶液,恰好使溶液中的Cu2+全部转化成沉淀,则原硝酸溶液的浓度为
(4)欲使铜与硝酸反应生成的气体在NaOH溶液中全部转化为NaNO3,至少需要30%的双氧水
13-14高一上·湖南长沙·开学考试 查看更多[11]
(已下线)2012-2013湖南省浏阳一中高一上学期入学考试化学试卷2016-2017学年辽宁省庄河市高级中学高一4月月考化学试卷河南省新野县第一高级中学2018届高三上学期第一次月考化学试题河北省定州中学2018届高三上学期第二次月考化学试题1(已下线)2019高考备考一轮复习精品资料 第四章 常见的非金属及其化合物 第4讲 氮及其化合物【教学案】(已下线)专题06 非金属及其化合物-备战2021届高考化学二轮复习题型专练陕西省韩城市西庄中学2021-2022学年高三上学期9月月考化学试题(已下线)3.2.2 铵盐和硝酸-【帮课堂】2022-2023学年高一化学同步精品讲义(沪科版2020必修第一册)第四章 非金属及其化合物 第23讲 硝酸 含氮化合物的转化关系(已下线)专题03 硫酸和硝酸专讲(专题过关)-2022-2023学年高一化学下学期期中期末考点大串讲(人教版2019必修第二册)(已下线)第6讲 硝酸 含氮化合物之间的转化
更新时间:2016-12-09 04:13:28
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】将22.4g铜与92mL一定浓度的硝酸反应,铜完全溶解,产生的NO和NO2混合气体在标准状况下的体积为6.72L。
(1)求NO、NO2的体积分别是多少?
(2)若要将产生的NO、NO2气体用水完全吸收,则需O2的体积(标准状况)是多少?
(1)求NO、NO2的体积分别是多少?
(2)若要将产生的NO、NO2气体用水完全吸收,则需O2的体积(标准状况)是多少?
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】用20.00 mL NaClO溶液恰好能氧化一定质量的Ba(HC2O4)2·6H2O固体,氧化产物为CO2。同样质量的Ba(HC2O4)2·6H2O固体又恰好能被25.00 mL 0.150 mol·L-1的Ba(OH)2溶液中和(假设反应后体积不变)。(计算结果保留到小数点后三位)
(1)中和后的溶液中Ba2+的浓度为_________ 。
(2)列式计算求NaClO溶液的浓度:_________ 。
(1)中和后的溶液中Ba2+的浓度为
(2)列式计算求NaClO溶液的浓度:
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】有硫酸与硝酸的混合液,取出其中10mL,加入足量的BaCl2溶液,将生成的沉淀过滤洗涤,干燥称得质量为4.66g。另取这种溶液10mL与2mol·L-1的NaOH溶液25mL恰好中和。则:
(1)混合液中c(H2SO4)=__ mol·L-1,c(HNO3)=__ mol·L-1
(2)另取10mL的混合液(混合液中的硝酸视为稀硝酸)与0.96g铜粉共热时,产生气体的体积为__ L(标准状况)。
(1)混合液中c(H2SO4)=
(2)另取10mL的混合液(混合液中的硝酸视为稀硝酸)与0.96g铜粉共热时,产生气体的体积为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】16.8gFe跟一定量浓 HNO3 反应,Fe 全部溶解,共收集NO、NO2的总体积为 11.2 L(标准状况),所得溶液中 H+的物质的量为0.02mol,请回答:
(1)反应中被还原的硝酸为_______ mol。
(2)生成的 NO 与 NO2 的物质的量之比为______ 。
(3)写出该反应的离子方程式:______ 。
(1)反应中被还原的硝酸为
(2)生成的 NO 与 NO2 的物质的量之比为
(3)写出该反应的离子方程式:
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】将32.64g铜与140mL一定浓度的硝酸反应,铜完全溶解产生的NO和NO2混合气体在标准状况下的体积为11.2L。
(1)NO的体积为_______ ;
(2)NO2的体积为______ 。
(1)NO的体积为
(2)NO2的体积为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】某研究性学习小组拟通过铜银合金与浓硝酸的反应,测定该合金的组成。考虑到NO2的聚合,该小组同学查阅到下列资料:
17℃、1.01×105Pa,2NO2(g) N2O4(g) 的平衡常数K=13.3,该条件下密闭容器中N2O4和NO2的混合气体达到平衡时c(NO2)="0.0300" mol·L-1。
N2O4(g) 的平衡常数K=13.3,该条件下密闭容器中N2O4和NO2的混合气体达到平衡时c(NO2)="0.0300" mol·L-1。
⑴此时平衡混合气体中c(N2O4)= (保留两位有效数字,下同)。
⑵17℃、1.01×105Pa时,将12.44g合金放入足量浓硝酸中,待合金完全溶解后,收集到NO2和N2O4的混合气体5.00L。
①根据平衡体系中NO2和N2O4的物质的量浓度,计算5.00L气体中NO2、N2O4的物质的量分别为 、 。
②计算合金中银的质量分数。
17℃、1.01×105Pa,2NO2(g)
 N2O4(g) 的平衡常数K=13.3,该条件下密闭容器中N2O4和NO2的混合气体达到平衡时c(NO2)="0.0300" mol·L-1。
N2O4(g) 的平衡常数K=13.3,该条件下密闭容器中N2O4和NO2的混合气体达到平衡时c(NO2)="0.0300" mol·L-1。⑴此时平衡混合气体中c(N2O4)= (保留两位有效数字,下同)。
⑵17℃、1.01×105Pa时,将12.44g合金放入足量浓硝酸中,待合金完全溶解后,收集到NO2和N2O4的混合气体5.00L。
①根据平衡体系中NO2和N2O4的物质的量浓度,计算5.00L气体中NO2、N2O4的物质的量分别为 、 。
②计算合金中银的质量分数。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】把2.0 mol/L Fe2(SO4)3溶液和2.0 mol/L H2SO4等体积混合(假设混合后溶液的体积等于混合前溶液的体积之和)。计算:(写出计算过程)
(1)混合液中Fe3+的物质的量浓度;
(2)混合液中H+、SO42—的物质的量浓度;
(3)向溶液中加入足量铁粉,经足够长时间后,铁粉有剩余, 求此时溶液中FeSO4的物质的量浓度。
(已知加入铁粉时先发生Fe+ Fe2(SO4)3="3Fe" SO4 反应,后发生Fe+ H2SO4="Fe" SO4+ H2)
(4)假设混和后的溶液为2L,加入一定量Fe粉后放出H2在标准状况下的体积为16.8L,求最终溶液中H+物质的量浓度。
(1)混合液中Fe3+的物质的量浓度;
(2)混合液中H+、SO42—的物质的量浓度;
(3)向溶液中加入足量铁粉,经足够长时间后,铁粉有剩余, 求此时溶液中FeSO4的物质的量浓度。
(已知加入铁粉时先发生Fe+ Fe2(SO4)3="3Fe" SO4 反应,后发生Fe+ H2SO4="Fe" SO4+ H2)
(4)假设混和后的溶液为2L,加入一定量Fe粉后放出H2在标准状况下的体积为16.8L,求最终溶液中H+物质的量浓度。
您最近一年使用:0次

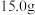 合金溶于
合金溶于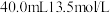 的浓硝酸中,待合金完全溶解后,收集到
的浓硝酸中,待合金完全溶解后,收集到 的
的 、
、 混合气体(标准状况),并测得溶液中的
混合气体(标准状况),并测得溶液中的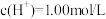 。假设反应后溶液的体积仍为
。假设反应后溶液的体积仍为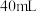 ,试计算:
,试计算:

