中国科学技术大学俞书宏教授团队和高敏锐教授课题组通过室温过饱和溶液共沉积法,实现了无定形NiFeMo氧化物纳米材料的宏量制备,该方法简便快捷,反应几分钟即可一次性生产多达515克的产物,制备的无定形NiFeMo氧化物在碱性条件下展示出优异的OER催化活性,明显优于结晶型NiFeMo氧化物。根据所学知识回答下列问题:
(1)区别结晶型NiFeMo氧化物和无定形NiFeMo氧化物最可靠的科学方法为_______ ,结晶型NiFeMo氧化物能自发呈现多面体外形,这种性质称为晶体的_______ 。
(2)配合物Ni(CO)4常温下为液态,易溶于CCl4,苯等有机溶剂,是获得高纯度纳米镍的原料,Ni(CO)4的配位原子是_______ 。
(3)下列状态的铁中,电离最外层的一个电子所需能量最大的是_______(填编号)。
(4)FeCl3中的化学键具有明显的共价性,蒸气状态下以双聚分子存在的FeCl3的结构式为_______ ,其中Fe的配位数为_______ 。
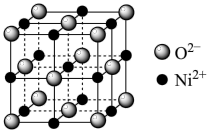
(5)立方NiO(氧化镍)晶体的结构如图所示,其晶胞边长为a pm,列式表示NiO晶体的密度为_______ g/cm3(不必计算出结果,阿伏加德罗常数的值为NA)。
(1)区别结晶型NiFeMo氧化物和无定形NiFeMo氧化物最可靠的科学方法为
(2)配合物Ni(CO)4常温下为液态,易溶于CCl4,苯等有机溶剂,是获得高纯度纳米镍的原料,Ni(CO)4的配位原子是
(3)下列状态的铁中,电离最外层的一个电子所需能量最大的是_______(填编号)。
A. | B.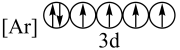 |
C.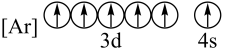 | D.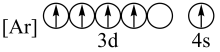 |
(5)立方NiO(氧化镍)晶体的结构如图所示,其晶胞边长为a pm,列式表示NiO晶体的密度为

更新时间:2022-04-22 14:53:06
|
相似题推荐
解答题-结构与性质
|
较难
(0.4)
【推荐1】短周期元素a、b、c、d的原子序数依次增大,c和d位于同主族且原子序数相差8;基态a原子核外有3个能级上容纳电子且每个能级上电子数相等,c原子s能级电子总数与p能级电子数相等,基态e原子的M层上有2个未成对电子且无空轨道。
(1)在a、b、c中,第一电离能由大到小排序为_______ (用元素符号表示);基态e原子的价层电子排布式为_____________ 。
(2)配合物e(ac)4在常温下呈液态,易溶于四氯化碳、苯等有机溶剂。固态e(ac)4的晶体类型是________ 。已知(dab)2分子中含非极性键,分子中每个原子最外层都达到8个电子稳定结构,1mol(dab)2分子含σ键的数目为_________ 。
(3)写出一种与dab-互为等电子体的分子__________ (填化学式)。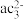 的中心原子杂化类型为
的中心原子杂化类型为______ ; 的空间构型为
的空间构型为___________ 。
(4)ec晶胞结构如图所示,其晶胞参数为a pm,列式计算该晶胞的密度为_________ g·cm-3(不必计算出结果,阿伏加德罗常数的值为NA),晶胞中c粒子的配位数为_____________ 。
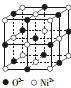
(5)人工合成的ec晶胞存在缺陷,即阳离子有+3、+2价两种。某人工合成的晶体样品组成为e0.96c,则该晶体中+3价、+2价两种离子的个数之比为__________ 。
(1)在a、b、c中,第一电离能由大到小排序为
(2)配合物e(ac)4在常温下呈液态,易溶于四氯化碳、苯等有机溶剂。固态e(ac)4的晶体类型是
(3)写出一种与dab-互为等电子体的分子
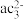 的中心原子杂化类型为
的中心原子杂化类型为 的空间构型为
的空间构型为(4)ec晶胞结构如图所示,其晶胞参数为a pm,列式计算该晶胞的密度为

(5)人工合成的ec晶胞存在缺陷,即阳离子有+3、+2价两种。某人工合成的晶体样品组成为e0.96c,则该晶体中+3价、+2价两种离子的个数之比为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐2】氮和磷元素的单质和化合物在农药生产及工业制造业等领域用途非常广泛,请根据提示回答下列问题:
(1)科学家合成了一种阳离子为“N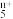 ”、其结构是对称的,5个N排成“V”形,每个N原子都达到8电子稳定结构,且含有2个氮氮三键;此后又合成了一种含有“N
”、其结构是对称的,5个N排成“V”形,每个N原子都达到8电子稳定结构,且含有2个氮氮三键;此后又合成了一种含有“N ”化学式分“N8”的离子晶体,其电子式为
”化学式分“N8”的离子晶体,其电子式为__________________ ,其中的阴离子的空间构型为_________ 。
(2)2001年德国专家从硫酸钱中检出一种组成为N4H4(SO4)2的物质,经测定,该物质易溶于水,在水中以SO 和N4H
和N4H 两种离子的形式存在。N4H44+根系易吸收,但它遇到碱时会生成类似白磷的N4分子,不能被植物吸收。1个N4H
两种离子的形式存在。N4H44+根系易吸收,但它遇到碱时会生成类似白磷的N4分子,不能被植物吸收。1个N4H 中含有
中含有______ 个σ键。
(3)氨(NH3)和膦(PH3)是两种三角锥形气态氢化物,其键角分别为107°和93.6°,试分析PH3的键角小于NH3的原因__________ 。
(4)P4S3可用于制造火柴,其分子结构如图l所示。_______ 。
②每个P4S3分子中含孤电子对的数月为_______ 。
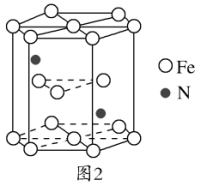
(5)某种磁性氮化铁的晶胞结构如图2所示,该化合物的化学式为______ 。若晶胞底边长为anm,高为cnm,则这种磁性氮化铁的晶体密度为_______ g/㎝3(用含ac和NA的式子表示)______ ;化合物中,稀土元素最常见的化合价是+3,但也有少数的稀土元素可以显示+4价,观察下面四种稀土元素的电离能数据,判断最有可能显示+4价的稀土元素是_____________ 。
几种稀土元素的电离能(单位:kJ/mol)
(1)科学家合成了一种阳离子为“N
 ”、其结构是对称的,5个N排成“V”形,每个N原子都达到8电子稳定结构,且含有2个氮氮三键;此后又合成了一种含有“N
”、其结构是对称的,5个N排成“V”形,每个N原子都达到8电子稳定结构,且含有2个氮氮三键;此后又合成了一种含有“N ”化学式分“N8”的离子晶体,其电子式为
”化学式分“N8”的离子晶体,其电子式为(2)2001年德国专家从硫酸钱中检出一种组成为N4H4(SO4)2的物质,经测定,该物质易溶于水,在水中以SO
 和N4H
和N4H 两种离子的形式存在。N4H44+根系易吸收,但它遇到碱时会生成类似白磷的N4分子,不能被植物吸收。1个N4H
两种离子的形式存在。N4H44+根系易吸收,但它遇到碱时会生成类似白磷的N4分子,不能被植物吸收。1个N4H 中含有
中含有(3)氨(NH3)和膦(PH3)是两种三角锥形气态氢化物,其键角分别为107°和93.6°,试分析PH3的键角小于NH3的原因
(4)P4S3可用于制造火柴,其分子结构如图l所示。

②每个P4S3分子中含孤电子对的数月为
(5)某种磁性氮化铁的晶胞结构如图2所示,该化合物的化学式为
几种稀土元素的电离能(单位:kJ/mol)
| 元素 | I1 | I2 | I3 | I4 |
| Se(钪) | 633 | 1235 | 2389 | 7019 |
| Y(铱) | 616 | 1181 | 1980 | 5963 |
| La(镧) | 538 | 1067 | 1850 | 4819 |
| Ce(铈) | 527 | 1047 | 1949 | 3547 |
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐3】回答下列问题:
(1)已知五种气体的溶解度如下表(气体的压强为 ,温度为
,温度为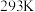 )。
)。
①比较电负性大小:S_______ P(填“>”“<”或“=”),硫化氢溶解度大于磷化氢可能原因是_______ 。
②已知不同杂化方式的碳原子的电负性会有差异,请从以上信息排出电负性的正确顺序:
_______ 
_______  ,乙烷、乙烯、乙炔中最易与金属钠反应的物质是
,乙烷、乙烯、乙炔中最易与金属钠反应的物质是_______ 。
(2)镍原子形成的微粒,电子排布式分别为① 、②
、② 、③
、③ 、④
、④ 、⑤
、⑤ ,有关这些微粒的叙述,下列叙述正确的是_______。
,有关这些微粒的叙述,下列叙述正确的是_______。
(3)铜及其化合物具有广泛的应用。请回答:
① 元素位于周期表
元素位于周期表_______ 区。
②下列说法不正确的是_______ 。
A.基态铜原子的核外电子有29种不间的空间运动状态
B.铜催化烯烃硝化反应时会产生 的键角比
的键角比 大
大
C. 中非金属元素电负性:
中非金属元素电负性:
D.配位键的强度: 大于
大于
③高温下固体中 比
比 稳定,常温下水溶液中
稳定,常温下水溶液中 离子比
离子比 离子稳定(水溶液中
离子稳定(水溶液中 易发生歧化反应生成
易发生歧化反应生成 ),原因是
),原因是_______ 。[已知:金属阳离子在水溶液中易与水分子发生络合形成水合离子,对应的热效应称为水合能, 的水合能为
的水合能为 的水合能为
的水合能为 的第二电离能为
的第二电离能为 。]
。]
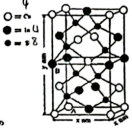
④ 与S形成的某化合物晶体的晶胞如图,该化合物的化学式为
与S形成的某化合物晶体的晶胞如图,该化合物的化学式为_______ 。该晶胞形状为长方体,长为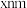 ,宽为
,宽为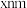 ,高为
,高为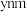 ,阿伏加德罗常数为
,阿伏加德罗常数为 。该晶体的密度为
。该晶体的密度为_______  。
。
(1)已知五种气体的溶解度如下表(气体的压强为
 ,温度为
,温度为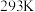 )。
)。| 气体 | 乙烷 | 乙烯 | 乙炔 | 硫化氢 | 磷化氢 |
溶解度 | 0.0062 | 0.0149 | 0.117 | 0.36 | 0.036 |
②已知不同杂化方式的碳原子的电负性会有差异,请从以上信息排出电负性的正确顺序:


 ,乙烷、乙烯、乙炔中最易与金属钠反应的物质是
,乙烷、乙烯、乙炔中最易与金属钠反应的物质是(2)镍原子形成的微粒,电子排布式分别为①
 、②
、② 、③
、③ 、④
、④ 、⑤
、⑤ ,有关这些微粒的叙述,下列叙述正确的是_______。
,有关这些微粒的叙述,下列叙述正确的是_______。A.微粒半径: | B.由光谱仪一定可以捕捉到发射光谱的是:②③④ |
C.电离一个电子所需最低能量: | D.得电子能力: |
①
 元素位于周期表
元素位于周期表②下列说法不正确的是
A.基态铜原子的核外电子有29种不间的空间运动状态
B.铜催化烯烃硝化反应时会产生
 的键角比
的键角比 大
大C.
 中非金属元素电负性:
中非金属元素电负性:
D.配位键的强度:
 大于
大于
③高温下固体中
 比
比 稳定,常温下水溶液中
稳定,常温下水溶液中 离子比
离子比 离子稳定(水溶液中
离子稳定(水溶液中 易发生歧化反应生成
易发生歧化反应生成 ),原因是
),原因是 的水合能为
的水合能为 的水合能为
的水合能为 的第二电离能为
的第二电离能为 。]
。]④
 与S形成的某化合物晶体的晶胞如图,该化合物的化学式为
与S形成的某化合物晶体的晶胞如图,该化合物的化学式为 ,宽为
,宽为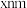 ,高为
,高为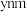 ,阿伏加德罗常数为
,阿伏加德罗常数为 。该晶体的密度为
。该晶体的密度为 。
。
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】碳元素在无机物和有机物中均充当了重要的角色,请回答下列问题:
(1)基态碳原子的价层电子排布图(轨道表达式)为__ ,其电子占据的能量最高的原子轨道的形状为__ ;C、N、O三种元素第一电离能最大的是__ 。
(2)有机物 中碳原子的轨道杂化类型为
中碳原子的轨道杂化类型为__ ,分子中两种碳碳单键长的大小关系为①__ ②(填“>”、“<”或“=”)。
(3) 和
和 均可以形成氢键,则沸点较高的是
均可以形成氢键,则沸点较高的是__ ,原因是__ 。
(4)石墨的结构及晶胞如图一所示,则石墨的密度为__ g·cm-3(用含a、d、NA的表达式表示)。A的原子坐标为( 、
、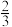 、0),则B的原子坐标为
、0),则B的原子坐标为__ 。

(5)石墨能与熔融的金属K作用,形成一种青铜色的化合物CxK,如图二所示,则x=__ 。
(1)基态碳原子的价层电子排布图(轨道表达式)为
(2)有机物
 中碳原子的轨道杂化类型为
中碳原子的轨道杂化类型为(3)
 和
和 均可以形成氢键,则沸点较高的是
均可以形成氢键,则沸点较高的是(4)石墨的结构及晶胞如图一所示,则石墨的密度为
 、
、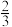 、0),则B的原子坐标为
、0),则B的原子坐标为
(5)石墨能与熔融的金属K作用,形成一种青铜色的化合物CxK,如图二所示,则x=
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐2】物质的组成与结构决定了物质的性质与变化,回答下列问题:
(1)基态氮原子核外未成对电子数为_______ 。
(2)在元素周期表中,N、O、F位于同周期且相邻,第一电离能最大的元素和最小的元素组成一种只含极性键的化合物M,中心原子的杂化类型是_______ 。
(3) 能与多种金属离子形成配合物,例如,工业冶炼金的原理:
能与多种金属离子形成配合物,例如,工业冶炼金的原理: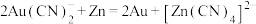 。
。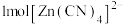 中含
中含_______ molσ键。
(4)钛酸钙晶胞结构如图所示。1个钛离子与_______ 个氧离子等距离且最近,连接这些氧离子构成正八面体,钛离子位于该正八面体的体心。
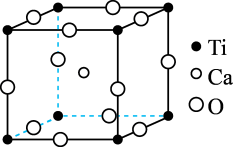
(5)在元素周期中,钡位于第六周期IIA族。钛酸钡、钛酸钙的熔点分别为1610℃、1975℃,其熔点差异的主要原因是_______ 。
(1)基态氮原子核外未成对电子数为
(2)在元素周期表中,N、O、F位于同周期且相邻,第一电离能最大的元素和最小的元素组成一种只含极性键的化合物M,中心原子的杂化类型是
(3)
 能与多种金属离子形成配合物,例如,工业冶炼金的原理:
能与多种金属离子形成配合物,例如,工业冶炼金的原理: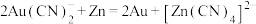 。
。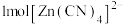 中含
中含(4)钛酸钙晶胞结构如图所示。1个钛离子与

(5)在元素周期中,钡位于第六周期IIA族。钛酸钡、钛酸钙的熔点分别为1610℃、1975℃,其熔点差异的主要原因是
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
【推荐3】短周期元素a、b、c、d的原子序数依次增大,c和d位于同主族且原子序数相差8;基态a原子核外有3个能级上容纳电子且每个能级上电子数相等,c原子s能级电子总数与p能级电子数相等,基态e原子的M层上有2个未成对电子且无空轨道。
(1)在a、b、c中,第一电离能由大到小排序为_______ (用元素符号表示);基态e原子的价层电子排布式为_____________ 。
(2)配合物e(ac)4在常温下呈液态,易溶于四氯化碳、苯等有机溶剂。固态e(ac)4的晶体类型是________ 。已知(dab)2分子中含非极性键,分子中每个原子最外层都达到8个电子稳定结构,1mol(dab)2分子含σ键的数目为_________ 。
(3)写出一种与dab-互为等电子体的分子__________ (填化学式)。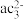 的中心原子杂化类型为
的中心原子杂化类型为______ ; 的空间构型为
的空间构型为___________ 。
(4)ec晶胞结构如图所示,其晶胞参数为a pm,列式计算该晶胞的密度为_________ g·cm-3(不必计算出结果,阿伏加德罗常数的值为NA),晶胞中c粒子的配位数为_____________ 。

(5)人工合成的ec晶胞存在缺陷,即阳离子有+3、+2价两种。某人工合成的晶体样品组成为e0.96c,则该晶体中+3价、+2价两种离子的个数之比为__________ 。
(1)在a、b、c中,第一电离能由大到小排序为
(2)配合物e(ac)4在常温下呈液态,易溶于四氯化碳、苯等有机溶剂。固态e(ac)4的晶体类型是
(3)写出一种与dab-互为等电子体的分子
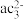 的中心原子杂化类型为
的中心原子杂化类型为 的空间构型为
的空间构型为(4)ec晶胞结构如图所示,其晶胞参数为a pm,列式计算该晶胞的密度为

(5)人工合成的ec晶胞存在缺陷,即阳离子有+3、+2价两种。某人工合成的晶体样品组成为e0.96c,则该晶体中+3价、+2价两种离子的个数之比为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】过渡金属在生产生活中的应用十分广泛。
Ⅰ.Cr元素形成的氯化铬酰(CrO2Cl2)有重要用途,在有机合成中可作氧化剂或氯化剂,能与许多有机物反应。
(1)CrO2Cl2常温下为深红色液体,能与CCl4、CS2等互溶,由以上实验事实可以判断CrO2Cl2分子是_____________ (填“极性”或“非极性”)分子,该分子的立体构型的名称为___________ 。
Ⅱ.Cu可形成多种配合物,根据下列信息回答问题:
(2)向盛有硫酸铜水溶液的试管里逐滴加入氨水,首先出现蓝色沉淀,继续滴加氨水,蓝色沉淀溶解,得到深蓝色的透明溶液,先后发生的离子方程式为Cu2++2NH3.H2O=Cu(OH)2↓+2NH4+,_______________ 。
(3)再向深蓝色透明溶液加入乙醇,析出深蓝色的晶体。深蓝色晶体的化学式为__________________________ ;析出晶体的原因是_______________________________________________________ 。若将Cu单质的粉末加入NH3的浓溶液中,通入O2,充分反应后溶液呈深蓝色,该反应的离子方程式是____________________ 。
(4)根据以上实验过程,判断NH3和H2O与Cu2+的配位能力:NH3____ H2O(填“大于”、“等于”或“小于”)。
Ⅲ.Ni(CO)6为正八面体结构,其中的镍原子位于正八面体的中心,配位体CO分子则在正八面体的六个顶点上。
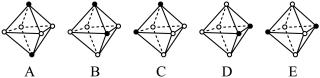
(5)若把其中两个CO配位体换成 NH3 得到新的配合物,则以下物质中互为同分异构体的是_________ 。(填字母编号,任填一组。图中黑点为NH3,圆圈为CO,Ni略去)
Ⅰ.Cr元素形成的氯化铬酰(CrO2Cl2)有重要用途,在有机合成中可作氧化剂或氯化剂,能与许多有机物反应。
(1)CrO2Cl2常温下为深红色液体,能与CCl4、CS2等互溶,由以上实验事实可以判断CrO2Cl2分子是
Ⅱ.Cu可形成多种配合物,根据下列信息回答问题:
(2)向盛有硫酸铜水溶液的试管里逐滴加入氨水,首先出现蓝色沉淀,继续滴加氨水,蓝色沉淀溶解,得到深蓝色的透明溶液,先后发生的离子方程式为Cu2++2NH3.H2O=Cu(OH)2↓+2NH4+,
(3)再向深蓝色透明溶液加入乙醇,析出深蓝色的晶体。深蓝色晶体的化学式为
(4)根据以上实验过程,判断NH3和H2O与Cu2+的配位能力:NH3
Ⅲ.Ni(CO)6为正八面体结构,其中的镍原子位于正八面体的中心,配位体CO分子则在正八面体的六个顶点上。

(5)若把其中两个CO配位体换成 NH3 得到新的配合物,则以下物质中互为同分异构体的是
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐2】第四周期的Cr、Fe、Co、Ni、Cu、Zn等许多金属能形成配合物。
(1)Cr的核外电子排布式为_________________ 。
(2)胆矾CuSO4·5H2O可写成[Cu(H2O)4]SO4·H2O,其结构示意图如下:

下列说法不正确的是___________ (填字母序号)。
A.在上述结构示意图中,所有氧原子都采用sp3杂化
B.在上述结构示意图中,存在配位键、共价键和离子键
C.胆矾是分子晶体,分子间存在氢键
D.胆矾中的水在不同温度下会分步失去
(3)往硫酸铜溶液中加入过量氨水,可生成配离子[Cu(NH3)4]2+。已知NF3与NH3的空间构型都是三角锥形,N与F的电负性大小为:N____ F(填“>”或“<”),但NF3不易与Cu2+形成配离子,其原因是______ 。写出与硫酸根离子互为等电子体的分子和离子____ 、____ (各填一种)。
(4)金属镍粉在CO气流中轻微加热;生成无色挥发性液态Ni(CO)4,呈正四面体构型。试推测四羰基镍的晶体类型是________ ,Ni(CO)4易溶于下列物质中的________ 。
A.水 B.四氯化碳 C.苯 D.硫酸镍溶液
(5)某镍铜合金的立方晶胞结构如图所示。
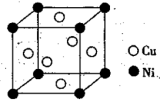
若合金的密度为d g·cm-3,晶胞参数a=_____ nm。(设NA代表阿伏加德罗常数的值)
(1)Cr的核外电子排布式为
(2)胆矾CuSO4·5H2O可写成[Cu(H2O)4]SO4·H2O,其结构示意图如下:

下列说法不正确的是
A.在上述结构示意图中,所有氧原子都采用sp3杂化
B.在上述结构示意图中,存在配位键、共价键和离子键
C.胆矾是分子晶体,分子间存在氢键
D.胆矾中的水在不同温度下会分步失去
(3)往硫酸铜溶液中加入过量氨水,可生成配离子[Cu(NH3)4]2+。已知NF3与NH3的空间构型都是三角锥形,N与F的电负性大小为:N
(4)金属镍粉在CO气流中轻微加热;生成无色挥发性液态Ni(CO)4,呈正四面体构型。试推测四羰基镍的晶体类型是
A.水 B.四氯化碳 C.苯 D.硫酸镍溶液
(5)某镍铜合金的立方晶胞结构如图所示。

若合金的密度为d g·cm-3,晶胞参数a=
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐3】 (硫酸四氨合铜晶体)是一种重要化工产品,一种制备流程如图所示。
(硫酸四氨合铜晶体)是一种重要化工产品,一种制备流程如图所示。

回答下列问题:
(1)基态 原子的价层电子排布图为
原子的价层电子排布图为___________ 。
(2) 的键角
的键角___________ (填“大于”“小于”或“等于”) 的键角。
的键角。
(3)已知: 、
、 的结构式如图所示,
的结构式如图所示, (硫酸)、
(硫酸)、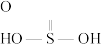 (亚硫酸)。
(亚硫酸)。
①浓硫酸浓度一般为 ,由稀硫酸较难得到无水硫酸,其主要原因是
,由稀硫酸较难得到无水硫酸,其主要原因是______________________ 。
②含氧酸中 键极性越强,酸性越强。
键极性越强,酸性越强。 的酸性比
的酸性比 的强,其原因是
的强,其原因是______________________ 。
(4) 是非极性分子,
是非极性分子, 是极性溶剂,但是
是极性溶剂,但是 能溶于水,其主要原因是
能溶于水,其主要原因是______________________ 。在 ,溶液中加入乙醇析出晶体,由此推知分子极性:
,溶液中加入乙醇析出晶体,由此推知分子极性:
_______ 水(填“大于”或“小于”)。
(5)浓硫酸中 价S具有强氧化性,而稀硫酸中S稳定,不表现强氧化性,其主要原因是
价S具有强氧化性,而稀硫酸中S稳定,不表现强氧化性,其主要原因是______________________ (从结构稳定性角度分析)。
(6)铜单质晶胞如图所示。与铜最近且等距离的铜原子有______ 个。铜晶胞中原子空间利用率为___________ 。

提示:顶点铜原子与面心铜原子紧邻,原子空间利用率等于原子总体积与晶胞体积之比。
 (硫酸四氨合铜晶体)是一种重要化工产品,一种制备流程如图所示。
(硫酸四氨合铜晶体)是一种重要化工产品,一种制备流程如图所示。
回答下列问题:
(1)基态
 原子的价层电子排布图为
原子的价层电子排布图为(2)
 的键角
的键角 的键角。
的键角。(3)已知:
 、
、 的结构式如图所示,
的结构式如图所示, (硫酸)、
(硫酸)、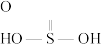 (亚硫酸)。
(亚硫酸)。①浓硫酸浓度一般为
 ,由稀硫酸较难得到无水硫酸,其主要原因是
,由稀硫酸较难得到无水硫酸,其主要原因是②含氧酸中
 键极性越强,酸性越强。
键极性越强,酸性越强。 的酸性比
的酸性比 的强,其原因是
的强,其原因是(4)
 是非极性分子,
是非极性分子, 是极性溶剂,但是
是极性溶剂,但是 能溶于水,其主要原因是
能溶于水,其主要原因是 ,溶液中加入乙醇析出晶体,由此推知分子极性:
,溶液中加入乙醇析出晶体,由此推知分子极性:
(5)浓硫酸中
 价S具有强氧化性,而稀硫酸中S稳定,不表现强氧化性,其主要原因是
价S具有强氧化性,而稀硫酸中S稳定,不表现强氧化性,其主要原因是(6)铜单质晶胞如图所示。与铜最近且等距离的铜原子有

提示:顶点铜原子与面心铜原子紧邻,原子空间利用率等于原子总体积与晶胞体积之比。
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
【推荐1】C、N和Si能形成多种高硬度材料,如 。
。
(1) 和
和 中硬度较高的是
中硬度较高的是_______ ,理由是_______ 。
(2)C和N能形成一种类石墨结构材料,其合成过程如下图。该类石塑结构材料化合物的化学式为_______ 。

(3)C和N还能形成一种五、元环状有机物咪唑(im),其结构为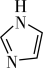 。化合物
。化合物 的结构示意图如下:
的结构示意图如下:

①基态Co原子的价层电子轨道表达式(价层电子排布图)为_______ 。
②N与Co之间的共价键类型是配位键,判断的理由是_______ 。
③阴离子 中心原子
中心原子 的价层电子对数为
的价层电子对数为_______ 。阳离子 和
和 之间除了阴阳离子间的静电作用力,还存在氢键作用,画出该氢键的表示式
之间除了阴阳离子间的静电作用力,还存在氢键作用,画出该氢键的表示式_______ 。例如水中氢键的表示式为: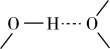
(4)晶胞内部各微粒的相对位置可以用原子坐标参数表示。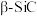 为立方晶系晶体,其晶胞中原子的坐标为
为立方晶系晶体,其晶胞中原子的坐标为
C: ;……
;……
Si: 。
。
① 立方晶胞中含有
立方晶胞中含有_______ 个Si原子、_______ 个C原子;
②已知晶胞参数为a,Si原子半径为 ,C原子半径为
,C原子半径为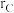 ,该晶胞中原子的体积占晶胞体积的百分率为
,该晶胞中原子的体积占晶胞体积的百分率为_______ (列出计算式即可)。
 。
。(1)
 和
和 中硬度较高的是
中硬度较高的是(2)C和N能形成一种类石墨结构材料,其合成过程如下图。该类石塑结构材料化合物的化学式为

(3)C和N还能形成一种五、元环状有机物咪唑(im),其结构为
 。化合物
。化合物 的结构示意图如下:
的结构示意图如下:
①基态Co原子的价层电子轨道表达式(价层电子排布图)为
②N与Co之间的共价键类型是配位键,判断的理由是
③阴离子
 中心原子
中心原子 的价层电子对数为
的价层电子对数为 和
和 之间除了阴阳离子间的静电作用力,还存在氢键作用,画出该氢键的表示式
之间除了阴阳离子间的静电作用力,还存在氢键作用,画出该氢键的表示式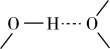
(4)晶胞内部各微粒的相对位置可以用原子坐标参数表示。
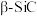 为立方晶系晶体,其晶胞中原子的坐标为
为立方晶系晶体,其晶胞中原子的坐标为
C:
 ;……
;……Si:
 。
。①
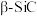 立方晶胞中含有
立方晶胞中含有②已知晶胞参数为a,Si原子半径为
 ,C原子半径为
,C原子半径为 ,该晶胞中原子的体积占晶胞体积的百分率为
,该晶胞中原子的体积占晶胞体积的百分率为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐2】氟硼铍酸钾是一种非线性光学晶体,我国是率先掌握通过非线性光学晶体变频来获得深紫外激光技术的国家。回答下列问题。
(1)多个处于激发态1s22s13s1的铍原子,在回到基态的过程中,最多可发出___ 种不同波长的光。
(2)Be和B的第一电离能(11)如上表所示。I1(Be)>I1(B)的原因是___ 。
(3)H3BO3在水溶液中存在解离反应:H3BO3+H2O⇌H++B(OH) ,B(OH)
,B(OH) 中存在配位键,其中B原子的杂化类型是
中存在配位键,其中B原子的杂化类型是____ ,从原子结构分析B(OH) 中能形成配位键的原因是
中能形成配位键的原因是___ 。
(4)氟硼酸钾是制备氟硼铍酸钾的原料之一、氟硼酸钾在高温下分解为KF和BF3,二者的沸点分别为1500℃、-101℃。KF的沸点远高于BF3的原因是___ 。
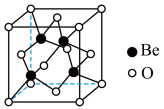
(5)BeO晶体也是制备氟硼铍酸钾晶体的原料,其晶胞结构如图所示。BeO晶胞中,O的堆积方式为______ ;设O与Be的最近距离为apm,用N、表示阿伏加德罗常数的值,则BeO晶体的密度为_____ g·cm-3。

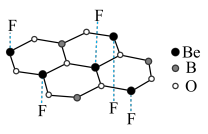
(6)氟硼铍酸钾晶体为层片状结构,如图为其中一层的局部示意图。平面六元环以B-O键和Be-O键交织相连,形成平面网状结构,每个Be都连接一个F,且F分别指向平面的上方或下方,K+分布在层间。则氟硼铍酸钾晶体的化学式为_______ 。
(1)多个处于激发态1s22s13s1的铍原子,在回到基态的过程中,最多可发出
| I1/( kJ∙mol-1) | |
| Be | 900 |
| B | 801 |
(3)H3BO3在水溶液中存在解离反应:H3BO3+H2O⇌H++B(OH)
 ,B(OH)
,B(OH) 中存在配位键,其中B原子的杂化类型是
中存在配位键,其中B原子的杂化类型是 中能形成配位键的原因是
中能形成配位键的原因是(4)氟硼酸钾是制备氟硼铍酸钾的原料之一、氟硼酸钾在高温下分解为KF和BF3,二者的沸点分别为1500℃、-101℃。KF的沸点远高于BF3的原因是
(5)BeO晶体也是制备氟硼铍酸钾晶体的原料,其晶胞结构如图所示。BeO晶胞中,O的堆积方式为

(6)氟硼铍酸钾晶体为层片状结构,如图为其中一层的局部示意图。平面六元环以B-O键和Be-O键交织相连,形成平面网状结构,每个Be都连接一个F,且F分别指向平面的上方或下方,K+分布在层间。则氟硼铍酸钾晶体的化学式为


您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐3】钛被称为继铁、铝之后的第三金属,制备金属钛的一种流程如下:

回答下列问题:
(1)基态钛原子的价电子排布图为______________________ ,其原子核外共有______ 种运动状态不相同的电子。已知TiCl4在通常情况下是无色液体,熔点为-37℃,沸点为136℃,可知TiCl4为__________________ 晶体。
(2)根据价层电子互斥理论,价层电子对之间的斥力大小有如下顺序:l—l>>l—b>b—b(1为孤对电子对,b为成键电子对),则关于H2O中的H—O—H键角可得出的结论是__________________________ 。
A.180°
B.接近120°,但小于120°
C.接近120°,但大于120°
D.接近109°28′,但小于109°28′
(3)钙钛矿晶体的结构如图所示。钛离子位于立方晶胞的角顶,被_______ 个氧离子包围成配位八面体;钙离子位于立方晶胞的体心,被_______ 个氧离子包围。钙钛矿晶体的化学式为_________ 。若该晶胞的边长为a pm,则钙钛矿晶体的密度为_________________ g·cm-3(只要求列算式,不必计算出数值)。


回答下列问题:
(1)基态钛原子的价电子排布图为
(2)根据价层电子互斥理论,价层电子对之间的斥力大小有如下顺序:l—l>>l—b>b—b(1为孤对电子对,b为成键电子对),则关于H2O中的H—O—H键角可得出的结论是
A.180°
B.接近120°,但小于120°
C.接近120°,但大于120°
D.接近109°28′,但小于109°28′
(3)钙钛矿晶体的结构如图所示。钛离子位于立方晶胞的角顶,被

您最近一年使用:0次



