NH3是重要的化工原料,可用于某些配合物的制备,如NiSO4溶于氨水可以形成[Ni(NH3)6]SO4。下列有关[Ni(NH3)6]SO4的说法正确的是
| A.配体为NH3,其空间结构为平面三角形 |
| B.1mol [Ni(NH3)6]2+中σ键的数目为18mol |
| C.[Ni(NH3)6]2+中H-N-H的键角大于NH3中的键角 |
| D.由于[Ni(NH3)6]SO4是配合物,故向其中滴加BaCl2溶液不会产生沉淀 |
更新时间:2022-04-28 21:38:06
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列叙述中正确的是
A.丙炔( )分子中含有3个 )分子中含有3个 键,2个 键,2个 键 键 |
B.丙炔( )分子中碳原子均是sp杂化 )分子中碳原子均是sp杂化 |
C.甲烷分子中的 键电子云关于镜面对称 键电子云关于镜面对称 |
D.环己烷(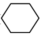 )的二氯代物只有4种(不考虑对映异构) )的二氯代物只有4种(不考虑对映异构) |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】治疗新冠肺炎药物瑞德西韦的主要成分结构如图。下列说法错误的是


A.分子中存在 键、 键、 键 键 |
B.分子中的 键的键能小于 键的键能小于 键的键能 键的键能 |
C.分子中N、O、P原子的第一电离能由大到小的关系为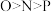 |
| D.分子中含有手性碳原子 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐3】NA为阿伏加德罗常数的值,下列说法正确的是
| A.4.4gC2H4O中含有σ键数目最多为0.7NA |
| B.1.7gH2O2中含有氧原子数为0.2NA |
| C.向1L0.1mol/LCH3COOH溶液通氨气至中性,铵根离子数为0.1NA |
| D.标准状况下,11.2LCl2通入水中,溶液中氯离子数为0.5NA |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】价层电子对互斥理论可以预测某些微粒的空间结构。下列说法正确的是
A. 和 和 的空间构型均为直线型 的空间构型均为直线型 | B. 和 和 的价层电子对互斥模型均为四面体 的价层电子对互斥模型均为四面体 |
C. 和 和 均为非极性分子 均为非极性分子 | D. 与 与 的键角相等 的键角相等 |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】A、B、C、D、E、F、G是前四周期的七种元素,其原子序数依次增大。A的基态原子中没有成对电子;B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同;D及其同主族元素的氢化物沸点变化趋势如图(D的氢化物沸点最高);F是地壳中含量最高的金属元素;G与F同主族。请回答下列问题:
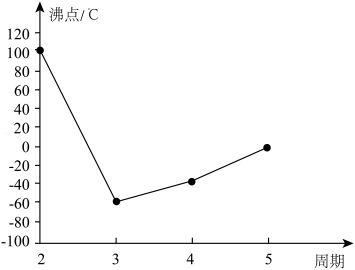
(1)写出F元素基态原子的核外电子排布式:____________ 。
(2)B、C、D三种元素电负性由大到小的顺序是____________ (用元素符号表示)。
(3)有关上述元素的下列说法,正确的是________ (填序号)。
①CA3沸点高于BA4,主要是因为前者相对分子质量较大
②配合物Ni(BD)4常温下为液态,易溶于CCl4、苯等有机溶剂,因此固态Ni(BD)4属于离子晶体
③C的氢化物的中心原子采取sp2杂化
④F单质的熔点高于E单质,是因为F单质的金属键较强
⑤比G的原子序数少1的元素第一电离能高于G
(4)CA3分子的立体构型为________ ,1 mol B2A4分子中含有________ 个σ键;

(1)写出F元素基态原子的核外电子排布式:
(2)B、C、D三种元素电负性由大到小的顺序是
(3)有关上述元素的下列说法,正确的是
①CA3沸点高于BA4,主要是因为前者相对分子质量较大
②配合物Ni(BD)4常温下为液态,易溶于CCl4、苯等有机溶剂,因此固态Ni(BD)4属于离子晶体
③C的氢化物的中心原子采取sp2杂化
④F单质的熔点高于E单质,是因为F单质的金属键较强
⑤比G的原子序数少1的元素第一电离能高于G
(4)CA3分子的立体构型为
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】 可用作杀虫剂,其制备步骤如下。
可用作杀虫剂,其制备步骤如下。
步骤1:向足量铜粉与一定量稀 的混合物中通入热空气,当铜粉不再溶解时,过滤得滤液。
的混合物中通入热空气,当铜粉不再溶解时,过滤得滤液。
步骤2:向步骤1所得滤液中边搅拌边滴加氨水,沉淀先增加后减少。当沉淀完全溶解时,停止滴加氨水。
步骤3:向步骤2所得溶液中加入95%乙醇,析出深蓝色 晶体。
晶体。
下列说法正确的是
 可用作杀虫剂,其制备步骤如下。
可用作杀虫剂,其制备步骤如下。步骤1:向足量铜粉与一定量稀
 的混合物中通入热空气,当铜粉不再溶解时,过滤得滤液。
的混合物中通入热空气,当铜粉不再溶解时,过滤得滤液。步骤2:向步骤1所得滤液中边搅拌边滴加氨水,沉淀先增加后减少。当沉淀完全溶解时,停止滴加氨水。
步骤3:向步骤2所得溶液中加入95%乙醇,析出深蓝色
 晶体。
晶体。下列说法正确的是
A.步骤1发生反应的离子方程式为 |
B.步骤2所得溶液中大量存在的离子有 、 、 、 、 、 、 |
C.步骤3加入95%乙醇的目的是降低 的溶解量 的溶解量 |
D. 中有12个配位键 中有12个配位键 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】Co3+的八面体配合物为CoClm•nNH3,若1mol此配合物与AgNO3作用生成1molAgCl沉淀,则m、n的值是
| A.m=1,n=5 | B.m=3,n=4 | C.m=4,n=3 | D.m=4,n=5 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐1】NA为阿伏加德罗常数的值。下列叙述错误的是
| A.1mol[Cu(NH3)4]2+中配位键的个数为4NA |
| B.46gCH3CH2OH中sp3杂化的原子数为2NA |
| C.0.5molSF6中S的价层电子对数为3NA |
| D.500mLpH=2的醋酸溶液中H+数目为0.005NA |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】不同空腔尺寸的葫芦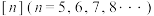 可以通过形成超分子从气体或溶液中识别不同分子并选择性吸附,对位取代的苯的衍生物恰好可以进入葫芦[6]脲(结构如图所示)的空腔。下列说法正确的是
可以通过形成超分子从气体或溶液中识别不同分子并选择性吸附,对位取代的苯的衍生物恰好可以进入葫芦[6]脲(结构如图所示)的空腔。下列说法正确的是
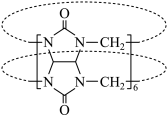
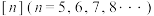 可以通过形成超分子从气体或溶液中识别不同分子并选择性吸附,对位取代的苯的衍生物恰好可以进入葫芦[6]脲(结构如图所示)的空腔。下列说法正确的是
可以通过形成超分子从气体或溶液中识别不同分子并选择性吸附,对位取代的苯的衍生物恰好可以进入葫芦[6]脲(结构如图所示)的空腔。下列说法正确的是
| A.葫芦脲可以吸附进入空腔的所有分子 |
| B.葫芦[6]脲是超分子且能发生丁达尔效应 |
| C.葫芦[6]脲形成的超分子中分子间存在范德华力、氢键 |
| D.可装入对甲基苯甲酸体现了超分子的“分子识别”功能 |
您最近半年使用:0次

 中,Cu为配位原子,NH3为配体
中,Cu为配位原子,NH3为配体 的价电子数为5;Z原子最外层电子数为次外层电子数的三倍;Q基态原子次外层有三个能级且各能级均排满电子,最外层有1个电子。下列说法不正确的是
的价电子数为5;Z原子最外层电子数为次外层电子数的三倍;Q基态原子次外层有三个能级且各能级均排满电子,最外层有1个电子。下列说法不正确的是

 与
与 之间可形成配位键
之间可形成配位键

