500℃时,在2L的密闭容器中,SO2和足量的O2在催化剂的条件下发生反应:2SO2+O2 2SO3。SO2和SO3的物质的量随时间变化的关系曲线如图所示。回答下列问题。
2SO3。SO2和SO3的物质的量随时间变化的关系曲线如图所示。回答下列问题。
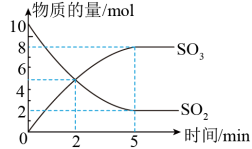
(1)在前5min内,以SO2的浓度变化表示的化学反应速率是____ mol/(L·min)。加快反应速率的措施有____ (至少提出两条)。
(2)该反应在____ (填2或5)min达到限度。
(3)反应达到平衡状态的依据是____ 。
A.单位时间内消耗1molSO2,同时生成1molSO3
B.SO2的浓度与SO3浓度相等
C.SO2的浓度与SO3浓度均不再变化
(4)用微观示意图的形式表示上述反应:____ 。

 2SO3。SO2和SO3的物质的量随时间变化的关系曲线如图所示。回答下列问题。
2SO3。SO2和SO3的物质的量随时间变化的关系曲线如图所示。回答下列问题。
(1)在前5min内,以SO2的浓度变化表示的化学反应速率是
(2)该反应在
(3)反应达到平衡状态的依据是
A.单位时间内消耗1molSO2,同时生成1molSO3
B.SO2的浓度与SO3浓度相等
C.SO2的浓度与SO3浓度均不再变化
(4)用微观示意图的形式表示上述反应:

更新时间:2022-05-06 08:16:32
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】恒温下在2L密闭容器中,X、Y、Z三种气态物质的物质的量随时间变化曲线如图。

(1)该反应的化学方程式为_____ 。
(2)从开始至5min,Y的平均反应速率为_____ ;X的转化率为_____ 。
(3)反应达平衡时体系的压强是开始时的_____ 倍。
(4)下列描述中能表明反应已达到平衡状态的是_____ 。(填序号)
①混合气体的压强不变
②混合气体的密度不变
③Z(g)的物质的量浓度不变
④混合气体的平均相对分子质量不变
⑤单位时间内生成2n mol Z,同时生成3n mol X
⑥容器内X、Y、Z三种气体的浓度之比为3:1:2
⑦某时刻v(X)=3v(Y)且不等于零
(5)在某一时刻采取下列措施能加快反应速率的是 。

(1)该反应的化学方程式为
(2)从开始至5min,Y的平均反应速率为
(3)反应达平衡时体系的压强是开始时的
(4)下列描述中能表明反应已达到平衡状态的是
①混合气体的压强不变
②混合气体的密度不变
③Z(g)的物质的量浓度不变
④混合气体的平均相对分子质量不变
⑤单位时间内生成2n mol Z,同时生成3n mol X
⑥容器内X、Y、Z三种气体的浓度之比为3:1:2
⑦某时刻v(X)=3v(Y)且不等于零
(5)在某一时刻采取下列措施能加快反应速率的是 。
| A.加催化剂 | B.降低温度 |
| C.体积不变,充入X | D.体积不变,从容器中分离出Y |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】能源是现代社会发展的支柱之一、
(1)化学反应中的能量变化,通常主要表现为热量的变化。下列反应中,属于放热反应的是___________ (填序号)。
a.Ba(OH)2·8H2O与NH4Cl混合搅拌
b.高温煅烧石灰石
c.铝与盐酸反应
(2)卫星发射可用肼(N2H4)作燃料,2 mol N2H4(气态)在O2(气态)中燃烧,生成N2(气态)和H2O(液态)放出1244 kJ的热量。则该反应的热化学方程式为:___________
(3)某温度时,在一个2 L的密闭容器中,X、Y、Z三种气体物质的物质的量随时间的变化曲线如图所示。根据图中数据,试填写下列空白:
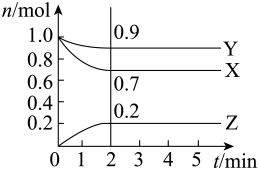
①该反应第___________ 分钟到达平衡状态。
②该反应的化学方程式为___________
③2 min时,Y的浓度为___________
④反应开始至2 min,气体X的平均反应速率为___________
(1)化学反应中的能量变化,通常主要表现为热量的变化。下列反应中,属于放热反应的是
a.Ba(OH)2·8H2O与NH4Cl混合搅拌
b.高温煅烧石灰石
c.铝与盐酸反应
(2)卫星发射可用肼(N2H4)作燃料,2 mol N2H4(气态)在O2(气态)中燃烧,生成N2(气态)和H2O(液态)放出1244 kJ的热量。则该反应的热化学方程式为:
(3)某温度时,在一个2 L的密闭容器中,X、Y、Z三种气体物质的物质的量随时间的变化曲线如图所示。根据图中数据,试填写下列空白:

①该反应第
②该反应的化学方程式为
③2 min时,Y的浓度为
④反应开始至2 min,气体X的平均反应速率为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】(1)写出葡萄糖的结构简式:_______ 。
(2)已知一定条件下,石墨可以转化为金刚石,其能量变化如图所示,则石墨和金刚石相比,较稳定的是_______ 。

(3)下列反应中,属于吸热反应的是_______ (填序号)。
①煅烧石灰石制生石灰 ②燃烧木炭取暖 ③炸药爆炸 ④酸与碱的中和反应 ⑤生石灰与水作用制熟石灰⑥Ba(OH)2·8H2O粉末和NH4Cl粉末反应 ⑦十水合碳酸钠(Na2CO3·10H2O)与硝酸铵的反应
(4)可逆反应 X(s)+3Y(g) 2Z(g) +Q(g)在不同条件下的反应速率如下,其中反应速率最快的是
2Z(g) +Q(g)在不同条件下的反应速率如下,其中反应速率最快的是_______ 。
A.v(X)=0 25 mol/(L·s) B. v(Y)=3.6 mol/(L·min)
C. v(Q)=0.1 mol/(L·s) D. v(Z)=0.3 mol/(L·s)
(2)已知一定条件下,石墨可以转化为金刚石,其能量变化如图所示,则石墨和金刚石相比,较稳定的是

(3)下列反应中,属于吸热反应的是
①煅烧石灰石制生石灰 ②燃烧木炭取暖 ③炸药爆炸 ④酸与碱的中和反应 ⑤生石灰与水作用制熟石灰⑥Ba(OH)2·8H2O粉末和NH4Cl粉末反应 ⑦十水合碳酸钠(Na2CO3·10H2O)与硝酸铵的反应
(4)可逆反应 X(s)+3Y(g)
 2Z(g) +Q(g)在不同条件下的反应速率如下,其中反应速率最快的是
2Z(g) +Q(g)在不同条件下的反应速率如下,其中反应速率最快的是A.v(X)=0 25 mol/(L·s) B. v(Y)=3.6 mol/(L·min)
C. v(Q)=0.1 mol/(L·s) D. v(Z)=0.3 mol/(L·s)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】如图,一定温度下,分别往容积均为 5L 的甲(恒压容器)、乙(恒容容器)中加入 0.5mol无色的N2O4气体,立即出现红棕色。当反应进行到 2s时,测得乙容器中N2O4的浓度为 0.09mol·L-1.经过 60s,乙容器中的反应达到平衡。(反应过程中两个容器的温度均保持恒定)

(1)容器中气体出现红棕色的原因(用化学方程式表示)是:_______ 。
(2)前 2s内乙容器中以N2O4的浓度变化表示的反应速率为_______ 。
(3)达到平衡时,甲容器中反应所需的时间_______ 60s(填“大于”、“小于”或“等于”,以下同);容器内N2O4的浓度甲_______ 乙;反应过程中吸收的能量甲_______ 乙。

(1)容器中气体出现红棕色的原因(用化学方程式表示)是:
(2)前 2s内乙容器中以N2O4的浓度变化表示的反应速率为
(3)达到平衡时,甲容器中反应所需的时间
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】2022年北京冬奥会的火炬“飞扬”是世界首款高压储氢火炬,它运用了液体火箭发动机的氢能技术。由氨气制取氢气是一种新工艺,氨气中氢含量高,是一种优良的小分子储氢载体,且安全、易储运,可通过下面两种方法由氨气制取氢气。
方法I:氨热分解法制氢气
(1)已知该反应为可逆反应,在一定温度下,利用催化剂将 分解为
分解为 和
和 的化学方程式为
的化学方程式为_______ 。
(2)该反应为吸热反应,说明反应物的总能量_______ 生成物的总能量(填“大于”“小于”或“等于”)。
(3)在一定温度和催化剂的条件下,向 容积固定的密闭容器中充入
容积固定的密闭容器中充入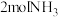 发生该反应,
发生该反应,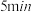 末测得容器中
末测得容器中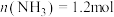 ,则在
,则在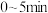 内,用
内,用 的浓度变化表示该反应的平均速率是:
的浓度变化表示该反应的平均速率是:
_______  。
。
(4)该反应达到化学平衡的标志是_______(填序号)。
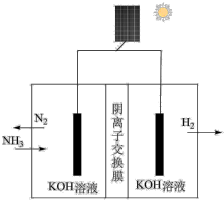
方法II:氨电解法制氢气
(5)利用电解原理,将氨转化为高纯氢气,其装置如图所示。装置中将太阳能转化为电能的电池,其主要材料是_______ 。装置中生成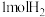 时,电路中通过
时,电路中通过_______  电子。为提高制取氢气的反应速率,可采取的方法是
电子。为提高制取氢气的反应速率,可采取的方法是_______ 。
方法I:氨热分解法制氢气
(1)已知该反应为可逆反应,在一定温度下,利用催化剂将
 分解为
分解为 和
和 的化学方程式为
的化学方程式为(2)该反应为吸热反应,说明反应物的总能量
(3)在一定温度和催化剂的条件下,向
 容积固定的密闭容器中充入
容积固定的密闭容器中充入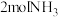 发生该反应,
发生该反应,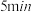 末测得容器中
末测得容器中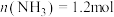 ,则在
,则在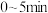 内,用
内,用 的浓度变化表示该反应的平均速率是:
的浓度变化表示该反应的平均速率是:
 。
。(4)该反应达到化学平衡的标志是_______(填序号)。
A. 的浓度为0 的浓度为0 | B. 的物质的量保持不变 的物质的量保持不变 |
| C.正反应速率与逆反应速率相等 | D. 的物质的量之比为 的物质的量之比为 |
方法II:氨电解法制氢气
(5)利用电解原理,将氨转化为高纯氢气,其装置如图所示。装置中将太阳能转化为电能的电池,其主要材料是
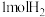 时,电路中通过
时,电路中通过 电子。为提高制取氢气的反应速率,可采取的方法是
电子。为提高制取氢气的反应速率,可采取的方法是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】回答下列问题:
(1)pH=3的醋酸和pH=ll的氢氧化钠溶液等体积混合后,混合溶液中c(Na+)____ c(CH3COO-)(填“>”或“<”)。
(2)将NaHCO3溶液跟A12(SO4)3溶液混合,相关反应的离子方程式是_________ 。
(3)—定温度下,在一个固定容积的密闭容器中,可逆反应A(g)+2B(g)⇌4C(g)△H>0,达到平衡时,c(A)=2mol•L-1,c(B)=7mol•L-1,c(C)=4mol•L-1。试确定B的起始浓度c(B)的取值范围是________________ 。若改变条件重新达到平衡后体系中C的质量分数增大,其采取的措施是________________ 。
(4)以丙烷为燃料制作新型燃料电池,电池的一极通入O2和CO2,另一极通入丙烷,电解质是熔融碳酸盐,电池负极的电极反应式为___________ ;放电时,CO32−移向电池的___ (填“正”或“负”)极。
(1)pH=3的醋酸和pH=ll的氢氧化钠溶液等体积混合后,混合溶液中c(Na+)
(2)将NaHCO3溶液跟A12(SO4)3溶液混合,相关反应的离子方程式是
(3)—定温度下,在一个固定容积的密闭容器中,可逆反应A(g)+2B(g)⇌4C(g)△H>0,达到平衡时,c(A)=2mol•L-1,c(B)=7mol•L-1,c(C)=4mol•L-1。试确定B的起始浓度c(B)的取值范围是
(4)以丙烷为燃料制作新型燃料电池,电池的一极通入O2和CO2,另一极通入丙烷,电解质是熔融碳酸盐,电池负极的电极反应式为
您最近一年使用:0次



