将FeCl3溶液滴加到KI-淀粉试纸上,试纸变蓝色,发生反应的离子方程式为:_______ 。
21-22高一·全国·课后作业 查看更多[3]
(已下线)9.2.1 反应的合理选择-2021-2022学年高一化学10分钟课前预习练(苏教版2019必修第二册)(已下线)1.2.2 离子反应和离子方程式(好题帮)-备战2023年高考化学一轮复习考点帮(新教材新高考)?(已下线)【定心卷】3.1.2 铁的重要化合物随堂练习-人教版2023-2024学年必修第一册
更新时间:2022-05-17 18:30:19
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】现有物质 ①铜 ②干冰 ③盐酸 ④液态醋酸 ⑤蔗糖 ⑥NaHSO4 固体 ⑦Ba(OH)2溶液 ⑧ 熔融的 NaCl ⑨BaSO4固体 ⑩稀硫酸
(1)能导电的是_______________ ;
(2)属于电解质的是___________________ ;
(3)向Ba(OH)2溶液中逐滴滴加NaHSO4溶液至 Ba2+恰好完全沉淀,发生反应的离子方程式为:_______ 。
(1)能导电的是
(2)属于电解质的是
(3)向Ba(OH)2溶液中逐滴滴加NaHSO4溶液至 Ba2+恰好完全沉淀,发生反应的离子方程式为:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】现有化学中常见的一些物质:①空气 ②氯气 ③氢氧化钠 ④熔融状态的硝酸钾 ⑤铁 ⑥葡萄糖 ⑦硫酸 ⑧氯化铁溶液⑨碳酸氢钠⑩氨气。在以上物质中:
(1)属于单质的是_______ ,属于混合物的是_______ ;
(2)属于电解质的是_______ ,属于非电解质的是_______ ;
(3)属于酸的是_______ ,属于碱的是_______ ,属于盐(包括盐溶液)的是_______ ;
(4)上述物质在该状态下能导电的是_______
(5)写出⑨在水中的电离方程式:_______
(6)写出下列离子方程式
i.③和⑧反应:_______
ii.用⑨治疗胃酸(主要成分为盐酸)过多:_______ 。
(1)属于单质的是
(2)属于电解质的是
(3)属于酸的是
(4)上述物质在该状态下能导电的是
(5)写出⑨在水中的电离方程式:
(6)写出下列离子方程式
i.③和⑧反应:
ii.用⑨治疗胃酸(主要成分为盐酸)过多:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】现有下列十种物质:①O2;②Fe;③CaO;④CO2;⑤H2SO4;⑥Ba(OH)2;⑦红褐色的氢氧化铁胶体;⑧硫酸钠溶液;⑨稀硝酸;⑩Cu2(OH)2CO3。
(1)按物质的树状分类法填写表格的空白处:
(2)上述十种物质中有两种物质之间可发生离子反应:H++OH-=H2O,该离子反应对应的化学反应方程式为_______ 。
(3)③与⑨发生反应的离子方程式为_______ 。
(4)②与⑨发生反应的化学方程式为3Fe+8HNO3(稀)=3Fe(NO3)2+2NO↑+4H2O,该反应的还原产物是_______ (填化学式),参加反应的氧化剂与还原剂的个数之比为_______ ,并用双线桥法表示该反应中电子转移的情况_________ 。
(5)写出的⑥的电离方程式:_______
(1)按物质的树状分类法填写表格的空白处:
分类标准 | 氧化物 | 电解质 | |||
属于该类的物质 | ② | ⑧⑨ | ⑦ |
(2)上述十种物质中有两种物质之间可发生离子反应:H++OH-=H2O,该离子反应对应的化学反应方程式为
(3)③与⑨发生反应的离子方程式为
(4)②与⑨发生反应的化学方程式为3Fe+8HNO3(稀)=3Fe(NO3)2+2NO↑+4H2O,该反应的还原产物是
(5)写出的⑥的电离方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
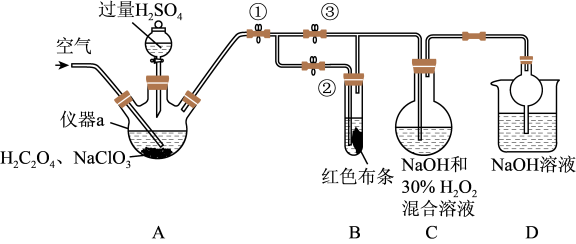
【推荐1】某小组在实验室探究 溶液与稀盐酸反应的实质。向0.2
溶液与稀盐酸反应的实质。向0.2
 溶液中滴加0.1
溶液中滴加0.1 盐酸,测定导电率的变化如图所示,回答下列问题:
盐酸,测定导电率的变化如图所示,回答下列问题:
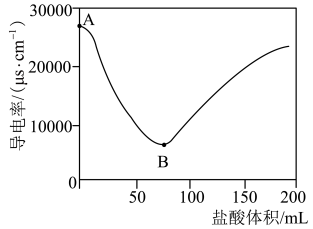
(1) 在水中以离子形式存在的实验证据是
在水中以离子形式存在的实验证据是___________ 。 的电离方程式为
的电离方程式为___________ 。
(2)A~B段反应的离子方程式为___________ 。
(3)B点恰好完全反应,此时溶液中存在的微粒有 、
、___________ 。
(4)下列化学反应的实质与 溶液与稀盐酸反应的实质相同的是
溶液与稀盐酸反应的实质相同的是___________ 。
A. 和
和 B.NaOH和
B.NaOH和 C.
C. 与
与
(5)与500mL该 溶液中
溶液中 含有相同原子数的HCl的质量为
含有相同原子数的HCl的质量为___________ 。
 溶液与稀盐酸反应的实质。向0.2
溶液与稀盐酸反应的实质。向0.2
 溶液中滴加0.1
溶液中滴加0.1 盐酸,测定导电率的变化如图所示,回答下列问题:
盐酸,测定导电率的变化如图所示,回答下列问题:
(1)
 在水中以离子形式存在的实验证据是
在水中以离子形式存在的实验证据是 的电离方程式为
的电离方程式为(2)A~B段反应的离子方程式为
(3)B点恰好完全反应,此时溶液中存在的微粒有
 、
、(4)下列化学反应的实质与
 溶液与稀盐酸反应的实质相同的是
溶液与稀盐酸反应的实质相同的是A.
 和
和 B.NaOH和
B.NaOH和 C.
C. 与
与
(5)与500mL该
 溶液中
溶液中 含有相同原子数的HCl的质量为
含有相同原子数的HCl的质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】废镍催化剂中主要有Ni,还有Al、Fe、SiO2及其它不溶于酸、碱的杂质。现用废镍催化剂制备NiSO4·7H2O晶体,其流程如图:
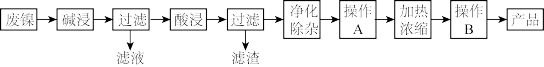
已知:Ksp[Fe(OH)3]=8.0×10-38,Ksp[Fe(OH)2]=8.0×10-16,Ksp[Al(OH)3]=3.2×10-34,Ksp[Ni(OH)2]=2.0×10-15,1g2=0.3,
回答下列问题
(1)“酸浸时发生的离子方程式为Fe+2H+=Fe2++H2↑、____ 。
(2)“净化除杂需要先加入H2O2溶液,发生反应的离子方程式为___ 。
(3)Ni2+在强碱性溶液中还可被NaClO氧化为NiOOH,该反应离子方程式为___ 。

已知:Ksp[Fe(OH)3]=8.0×10-38,Ksp[Fe(OH)2]=8.0×10-16,Ksp[Al(OH)3]=3.2×10-34,Ksp[Ni(OH)2]=2.0×10-15,1g2=0.3,
回答下列问题
(1)“酸浸时发生的离子方程式为Fe+2H+=Fe2++H2↑、
(2)“净化除杂需要先加入H2O2溶液,发生反应的离子方程式为
(3)Ni2+在强碱性溶液中还可被NaClO氧化为NiOOH,该反应离子方程式为
您最近一年使用:0次
【推荐3】(1)难溶物PbSO4溶于CH3COONH4溶液可制得易溶于水的(CH3COO)2Pb,发生的反应为PbSO4+2CH3COONH4=(CH3COO)2Pb+(NH4)2SO4,说明(CH3COO)2Pb是________ (填“强”或“弱”)电解质。
(2)已知次磷酸(H3PO2)与足量的氢氧化钠溶液反应生成NaH2PO2和H2O,则次磷酸是_____ 元酸(填“一”、“二”或“三”)。
(3)一个完整的氧化还原反应方程式可以拆开写成两个“半反应式”,一个是“氧化反应”式,一个是“还原反应”式。如2Fe3++Cu=2Fe2++Cu2+的拆写结果是:氧化反应为:Cu-2e−=Cu2+;还原反应为:2Fe3++2e−=2Fe2+。请据此将反应:Fe+2H+=Fe2++H2↑拆写成两个“半反应式”:氧化反应为____________________ ;还原反应为____________________ 。
(4)某同学写出以下三个化学方程式(未配平)
①NO+HNO3→N2O3+H2O
②NH3+NO→HNO2+H2O
③N2O4+H2O→HNO3+HNO2
其中你认为一定不可能实现的是________ (填序号)。
(2)已知次磷酸(H3PO2)与足量的氢氧化钠溶液反应生成NaH2PO2和H2O,则次磷酸是
(3)一个完整的氧化还原反应方程式可以拆开写成两个“半反应式”,一个是“氧化反应”式,一个是“还原反应”式。如2Fe3++Cu=2Fe2++Cu2+的拆写结果是:氧化反应为:Cu-2e−=Cu2+;还原反应为:2Fe3++2e−=2Fe2+。请据此将反应:Fe+2H+=Fe2++H2↑拆写成两个“半反应式”:氧化反应为
(4)某同学写出以下三个化学方程式(未配平)
①NO+HNO3→N2O3+H2O
②NH3+NO→HNO2+H2O
③N2O4+H2O→HNO3+HNO2
其中你认为一定不可能实现的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】工业燃烧煤、石油等化石燃料释放出大量氮氧化物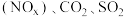 等气体,严重污染空气.对废气进行脱硝、脱碳和脱硫处理可实现绿色环保、废物利用。
等气体,严重污染空气.对废气进行脱硝、脱碳和脱硫处理可实现绿色环保、废物利用。
I.脱硝:
(1)催化剂存在下, 还原
还原 生成水蒸气和其他无毒物质的化学方程式为
生成水蒸气和其他无毒物质的化学方程式为_______ 。
II.脱碳:向 密闭容器中加入
密闭容器中加入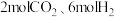 ,在恒温恒容的条件下发生反应
,在恒温恒容的条件下发生反应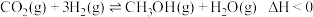 。
。
(2)下列叙述中,能说明此反应达到平衡状态的是_______(填字母)。
(3)该反应过程中的部分数据见下表:
① 时,反应是否达到平衡状态?
时,反应是否达到平衡状态?__________ (填“是”或“否),理由是____________ 。
②前 内的平均反应速率
内的平均反应速率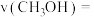
____________  ;平衡时
;平衡时 的浓度为
的浓度为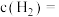
____________  ;平衡时
;平衡时 的转化率为
的转化率为________________ 。
③在其他条件不变的情况下,若 时向该密闭容器中通入
时向该密闭容器中通入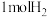 ,此时正反应速率将
,此时正反应速率将___________ (用“变快”,“变慢”或“不变”填空)。
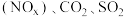 等气体,严重污染空气.对废气进行脱硝、脱碳和脱硫处理可实现绿色环保、废物利用。
等气体,严重污染空气.对废气进行脱硝、脱碳和脱硫处理可实现绿色环保、废物利用。I.脱硝:
(1)催化剂存在下,
 还原
还原 生成水蒸气和其他无毒物质的化学方程式为
生成水蒸气和其他无毒物质的化学方程式为II.脱碳:向
 密闭容器中加入
密闭容器中加入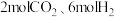 ,在恒温恒容的条件下发生反应
,在恒温恒容的条件下发生反应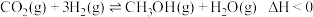 。
。(2)下列叙述中,能说明此反应达到平衡状态的是_______(填字母)。
A.单位时间内生成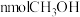 的同时生成 的同时生成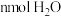 |
B. 和 和 的物质的量分数保持不变 的物质的量分数保持不变 |
C. 和 和 的浓度保持不变 的浓度保持不变 |
| D.混合气体的密度保持不变 |
反应时间/ | 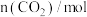 | 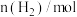 | 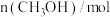 | 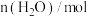 |
| 0 | 2 | 6 | 0 | 0 |
| 10 | 4.5 | |||
| 20 | 1 | |||
| 30 | 1 |
 时,反应是否达到平衡状态?
时,反应是否达到平衡状态?②前
 内的平均反应速率
内的平均反应速率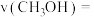
 ;平衡时
;平衡时 的浓度为
的浓度为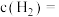
 ;平衡时
;平衡时 的转化率为
的转化率为③在其他条件不变的情况下,若
 时向该密闭容器中通入
时向该密闭容器中通入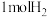 ,此时正反应速率将
,此时正反应速率将
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】“价——类”二维图是学习元素化合物知识的好方法,依据图中氮元素及其化合物的转化关系,回答问题:
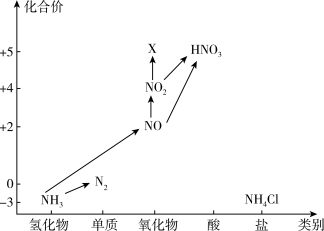
(1)图中,X的化学式为_______
(2)回答下列关于NH3的问题:
①实验室常用NH4Cl与Ca(OH)2制取氨气,该反应的化学方程式为_______ 。
②下列试剂能用于干燥NH3的是_______ (填字母)。
A.浓硫酸 B.碱石灰 C.CaO固体 D.P2O5固体
③氮分子的电子式为_______ ,硝酸铵具有的化学键类型是_______ 。。
④工业上可采用碱液吸收和氨还原处理含NOx尾气。其中用碱液吸收的化学方程式为:NO+NO2+2NaOH=2NaNO2+H2O,NO2+2NaOH=NaNO2+NaNO3+H2O。根据上述原理,下列气体中被过量NaOH溶液吸收后有气体剩余的是_______ 。
A.1molO2和4molNO2 B.1molO2和7molNO
C.1molNO和4molNO2 D.4molNO和4molNO2
(3)SCR和NSR技术可有效降低柴油发动机在空气过量条件下的NOx排放。SCR(选择性催化还原)工作原理:
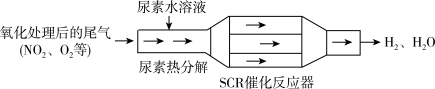
①已知尿素[CO(NH2)2]水溶液热分解为NH3和CO2,请写出SCR催化反应器中NH3还原NO2的化学方程式:_______ 。
②尿素溶液浓度影响NO2的转化,测定溶液中尿素(M=60g·mol−1)含量的方法如下:取ag尿素溶液,将所含氮完全转化为NH3,所得NH3用过量的v1mLc1mol·L−1H2SO4溶液吸收完全,剩余H2SO4用v2mLc2mol·L−1NaOH溶液恰好中和,则尿素溶液中溶质的质量分数是_______ 。

(1)图中,X的化学式为
(2)回答下列关于NH3的问题:
①实验室常用NH4Cl与Ca(OH)2制取氨气,该反应的化学方程式为
②下列试剂能用于干燥NH3的是
A.浓硫酸 B.碱石灰 C.CaO固体 D.P2O5固体
③氮分子的电子式为
④工业上可采用碱液吸收和氨还原处理含NOx尾气。其中用碱液吸收的化学方程式为:NO+NO2+2NaOH=2NaNO2+H2O,NO2+2NaOH=NaNO2+NaNO3+H2O。根据上述原理,下列气体中被过量NaOH溶液吸收后有气体剩余的是
A.1molO2和4molNO2 B.1molO2和7molNO
C.1molNO和4molNO2 D.4molNO和4molNO2
(3)SCR和NSR技术可有效降低柴油发动机在空气过量条件下的NOx排放。SCR(选择性催化还原)工作原理:

①已知尿素[CO(NH2)2]水溶液热分解为NH3和CO2,请写出SCR催化反应器中NH3还原NO2的化学方程式:
②尿素溶液浓度影响NO2的转化,测定溶液中尿素(M=60g·mol−1)含量的方法如下:取ag尿素溶液,将所含氮完全转化为NH3,所得NH3用过量的v1mLc1mol·L−1H2SO4溶液吸收完全,剩余H2SO4用v2mLc2mol·L−1NaOH溶液恰好中和,则尿素溶液中溶质的质量分数是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】铁是应用最广泛的金属,铁的卤化物、氧化物以及高价铁的含氧酸盐均为重要化合物。
(1)现有一含有FeCl2和FeCl3的混合物样品,采用实验方法测得n(Fe):n(Cl)=1:2.1,则该样品中FeCl3的物质的量分数为________ 。在实验室中, 可用铁粉和
可用铁粉和________ 反应制备,FeCl3可用铁粉和________ 反应制备。
(2) FeCl3与氢碘酸反应时可生成棕色物质,该反应的离子方程式为________________ 。
(3)高铁酸钾(K2FeO4)是一种强氧化剂,可作为水处理剂和高容量电池材料。FeCl3与KClO在强碱性条件下反应可制取K2FeO4,其反应的离子方程式为________________ 。
(1)现有一含有FeCl2和FeCl3的混合物样品,采用实验方法测得n(Fe):n(Cl)=1:2.1,则该样品中FeCl3的物质的量分数为
 可用铁粉和
可用铁粉和(2) FeCl3与氢碘酸反应时可生成棕色物质,该反应的离子方程式为
(3)高铁酸钾(K2FeO4)是一种强氧化剂,可作为水处理剂和高容量电池材料。FeCl3与KClO在强碱性条件下反应可制取K2FeO4,其反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】纳米磁性流体材料广泛应用于减震、医疗器械、声音调节等高科技领域。下图是制备纳米Fe3O4磁流体的两种流程:
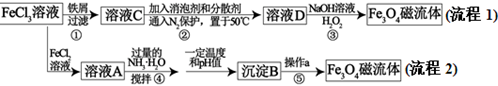
(1)分析流程图中的两种流程,其中_________ (填“流程1”、“流程2”)所有反应不涉及氧化还原反应。步骤①反应的离子方程式为____________ 。
(2)步骤②保持50℃的做法是_________ 。
(3)步骤③中加入的H2O2电子式是_______ ,步骤③制备Fe3O4磁流体的化学方程式为________ 。
(4)流程2中FeCl3和FeCl2制备Fe3O4磁流体,理论上FeCl3和FeCl2物质的量之比为_________ 。已知沉淀B为四氧化三铁,步骤⑤中操作a具体的步骤是_____________ 。
(5)利用K2Cr2O7可测定Fe3O4磁流体中的Fe2+含量。若Fe3O4磁流体与K2Cr2O7充分反应消耗了0.01 mol·L-1的K2Cr2O7标准溶液100 mL,则磁流体中含有Fe2+的物质的量为_____ mol。若配制的K2Cr2O7标准溶液装在__________ (填“酸式滴定管”或“碱式滴定管”)时,滴定前平视刻度线,滴定后仰视刻度线,则测定结果是Fe3O4磁流体中的Fe2+含量_____ (填“偏大”、“偏小”或“不变”)。

(1)分析流程图中的两种流程,其中
(2)步骤②保持50℃的做法是
(3)步骤③中加入的H2O2电子式是
(4)流程2中FeCl3和FeCl2制备Fe3O4磁流体,理论上FeCl3和FeCl2物质的量之比为
(5)利用K2Cr2O7可测定Fe3O4磁流体中的Fe2+含量。若Fe3O4磁流体与K2Cr2O7充分反应消耗了0.01 mol·L-1的K2Cr2O7标准溶液100 mL,则磁流体中含有Fe2+的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】铁是人类较早使用的金属之一。运用所学知识,回答下列问题:
(1)鉴别Fe(OH)3胶体和FeCl3溶液的方法是
(2)电子工业用FeC13溶液腐蚀敷在绝缘板上的铜,制造印刷电路板。请写出FeC13溶液与铜反应的化学方程式;当向盛有氯化铁溶液的烧杯中同时加入铁粉和铜粉,反应结束后,烧杯底部不可能出现的是( )
(3)工程师欲从制造印刷电路板的废水中回收铜,并获得FeC13溶液,设计如图方案:

①滤渣C的化学式为
②加过量D发生反应的离子方程式为
③通入F发生反应的化学方程式为
(1)鉴别Fe(OH)3胶体和FeCl3溶液的方法是
(2)电子工业用FeC13溶液腐蚀敷在绝缘板上的铜,制造印刷电路板。请写出FeC13溶液与铜反应的化学方程式;当向盛有氯化铁溶液的烧杯中同时加入铁粉和铜粉,反应结束后,烧杯底部不可能出现的是( )
| A.有铜无铁 | B.有铁有铜 | C.有铁无铜 | D.无铁无铜 |
(3)工程师欲从制造印刷电路板的废水中回收铜,并获得FeC13溶液,设计如图方案:

①滤渣C的化学式为
②加过量D发生反应的离子方程式为
③通入F发生反应的化学方程式为
您最近一年使用:0次