如表是元素周期表的一部分,其中每个数字序号代表一种短周期元素。

(1)⑧⑨⑩三元素的最高价氧化物对应的水化物酸性由强到弱的顺序是____ (写化学式),氢化物还原性由强到弱的顺序是____ (写化学式)。
(2)元素①和②形成的最简单化合物的电子式是____ 。
(3)元素⑥⑩形成的化合物含有的化学键类型是____ 。
(4)元素⑤的最高价氧化物的水化物与元素⑦的单质反应的化学方程式是____ 。
(5)元素②的最简单氢化物与其最高价氧化物的水化物反应的离子方程式是____ 。

(1)⑧⑨⑩三元素的最高价氧化物对应的水化物酸性由强到弱的顺序是
(2)元素①和②形成的最简单化合物的电子式是
(3)元素⑥⑩形成的化合物含有的化学键类型是
(4)元素⑤的最高价氧化物的水化物与元素⑦的单质反应的化学方程式是
(5)元素②的最简单氢化物与其最高价氧化物的水化物反应的离子方程式是
更新时间:2022-05-12 19:48:52
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】某化学兴趣小组用含A、B两种金属单质的粉末状混合物进行如下实验,其转化关系如图所示(部分反应物或生成物未列出),其中E为白色沉淀,I为红褐色沉淀。

(1)写出下列物质的化学式:F____________________ ,G_______________
(2)分离粉末状混合物最简单的方法是__________________________________
(3)D→E转化中,加入足量的X,试剂X可能是________
(4)写出下列转化的化学方程式:
A→C:_____________________________________________________________________
H→I:____________________________________________________________________
(5)过量的B加入稀硝酸中的化学反应方程式为:____________________________________
(6)若对G溶液中的阳离子进行检验:用所给试剂(KSCN溶液、氯水)设计检验G溶液中阳离子的方法。________________________________________________________________________________________________________________________________________ 。

(1)写出下列物质的化学式:F
(2)分离粉末状混合物最简单的方法是
(3)D→E转化中,加入足量的X,试剂X可能是________
| A.饱和NaCl溶液 | B.NaOH溶液 | C.氨水 | D.Ba(OH)2溶液 |
A→C:
H→I:
(5)过量的B加入稀硝酸中的化学反应方程式为:
(6)若对G溶液中的阳离子进行检验:用所给试剂(KSCN溶液、氯水)设计检验G溶液中阳离子的方法。
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】下列转化关系中,X、Y是生活中用途广泛的两种金属单质,A、B是氧化物,A呈红棕色,C、D、E是中学常见的三种化合物。分析转化关系回答问题。
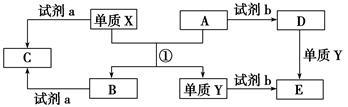
(1)请写出反应①的化学方程式:_________________ 。
(2)检验D溶液中Y离子的方法是___________ 。
(3)若试剂a是NaOH溶液,写出单质X与NaOH溶液反应的离子方程式____________ 。
(4)若试剂b是H2SO4,工业上用E、H2SO4和NaNO2为原料制取高效净水剂Y(OH)SO4,已知还原产物为NO,则该反应的化学方程式是______________ 。
(5)工业上电解熔融的B制取X时,若阳极产生的气体在标准状况下的体积为33.6 L,则阴极产物的质量为____________ 。

(1)请写出反应①的化学方程式:
(2)检验D溶液中Y离子的方法是
(3)若试剂a是NaOH溶液,写出单质X与NaOH溶液反应的离子方程式
(4)若试剂b是H2SO4,工业上用E、H2SO4和NaNO2为原料制取高效净水剂Y(OH)SO4,已知还原产物为NO,则该反应的化学方程式是
(5)工业上电解熔融的B制取X时,若阳极产生的气体在标准状况下的体积为33.6 L,则阴极产物的质量为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】X、Y、Z、M、W为原子序数依次增大的五种短周期元素,元素的性质或原子结构的相关叙述如表所示,回答下列问题。
(1)分别依次写出X、W的元素名称___________ 、___________ 。
(2)Y、Z、M的简单离子半径依次增大的顺序为___________ (填微粒符号)。
(3)X的简单气态氢化物与W的最高价氧化物对应的水化物反应的化学方程式为___________ 。
(4)X和Y简单气态氢化物的热稳定性较强的是___________ (填化学式)。
(5)Z的最高价氧化物对应的水化物的电子式为___________ ,该物质所含化学键类型为___________ ,该物质与M的单质反应的离子方程式为___________ 。
| 元素编号 | 元素性质或原子结构的相关叙述 |
| X | 元素原子L层是K层电子数的2.5倍 |
| Y | 元素原子最外层电子数比其次外层电子数多4 |
| Z | 元素原子最外层有1个电子,其阳离子与Y的阴离子核外电子总数相同 |
| M | 地壳中含量最多的金属元素 |
| W | 最高正化合价与最低负化合价代数和为6 |
(2)Y、Z、M的简单离子半径依次增大的顺序为
(3)X的简单气态氢化物与W的最高价氧化物对应的水化物反应的化学方程式为
(4)X和Y简单气态氢化物的热稳定性较强的是
(5)Z的最高价氧化物对应的水化物的电子式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】下表是元素周期表的一部分,按要求回答下列问题:
(1)①的简单氢化物的电子式:___________ 。
(2)⑥的原子结构示意图:___________ 。
(3)⑤、⑥、⑦的最高价氧化物对应水化物的酸性由强到弱的顺序为___________ (用化学式表示),③的最高价氧化物对应水化物中含有的化学键的类型为___________ 。
(4)能证明元素⑦比元素⑥的非金属性强的实验事实的是___________(填字母)。
(5)④的单质在空气中因表面氧化可以形成致密的氧化物保护膜,从而可以保护内部的单质不被氧化,该氧化物与NaOH溶液反应的离子方程式为___________ 。
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA |
2 | ① | ② | |||||
3 | ③ | ④ | ⑤ | ⑥ | ⑦ |
(2)⑥的原子结构示意图:
(3)⑤、⑥、⑦的最高价氧化物对应水化物的酸性由强到弱的顺序为
(4)能证明元素⑦比元素⑥的非金属性强的实验事实的是___________(填字母)。
| A.常温下元素⑦的单质为气态,而元素⑥的单质为固态 |
| B.元素⑦的气态氢化物比元素⑥的气态氢化物稳定 |
| C.元素⑦的氧化物对应水化物比⑥的氧化物对应水化物酸性强 |
| D.元素⑦的单质能与⑥的氢化物溶液反应生成⑥的单质 |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】短周期主族元素A、B、C、D、E在元素周期表中的位置如图所示,A的简单离子半径是同周期元素简单离子中半径最小的。请回答下列问题:

(1)描述D在元素周期表中的位置:_____________________________ 。
(2)在A、B、C、E四种元素最高价氧化物对应的水化物中酸性最强的是__________ (写化学式,下同),非金属最简单气态氢化物最不稳定的是_____________________ 。
(3)写出满足下列条件分子的结构式_________________________
①所有原子最外层是8个电子; ②C和E组成的化合物

(1)描述D在元素周期表中的位置:
(2)在A、B、C、E四种元素最高价氧化物对应的水化物中酸性最强的是
(3)写出满足下列条件分子的结构式
①所有原子最外层是8个电子; ②C和E组成的化合物
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】下表为元素周期表中短周期的一部分,A—G代表6种短周期元素。
已知C与氢元素能组成生活中最常见的化合物W。请填写下列空白。
(1)写出A元素的两种核素___________ (用 形式表示);
形式表示);
(2)与D同主族的下一周期元素的简单离子的结构示意图___________ ;
(3)G的单质与W反应的离子方程式为___________ ;
(4)B元素与氢元素组成含有10个电子和18个电子的分子的化学式分别为___________ ;
(5)A、B、C非金属性由强到弱的顺序为___________ (用元素符号表示);理由是___________ ;
(6)设计能说明E、F的金属性或非金属性强弱的实验___________ 。
| A | B | C | ||||
| D | E | F | G |
(1)写出A元素的两种核素
 形式表示);
形式表示);(2)与D同主族的下一周期元素的简单离子的结构示意图
(3)G的单质与W反应的离子方程式为
(4)B元素与氢元素组成含有10个电子和18个电子的分子的化学式分别为
(5)A、B、C非金属性由强到弱的顺序为
(6)设计能说明E、F的金属性或非金属性强弱的实验
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】下表是元素周期表的一部分,表中所列的字母分别代表一种元素。

试回答下列问题:
(1)D元素的基态原子的电子排布图是图①、②中的一个。
① ②
②
另一个电子排布图错误的原因是:它不符合_______ (填标号)。
A. 构造原理 B. 泡利原理 C. 洪特规则
(2)一个J原子(基态)中未成对电子数为_______ ,L的原子序数为_______ ,M的简化电子排布式为_______ 。
(3)K位于元素周期表中第_______ 周期、_______ 族,属于_______ 区元素;
(4)根据对角线规则及已知元素性质,写出B、E元素最高价氧化物的水化物在溶液反应的离子方程式_______ 。
(5)下列有关说法正确的是_______

试回答下列问题:
(1)D元素的基态原子的电子排布图是图①、②中的一个。
①
 ②
②
另一个电子排布图错误的原因是:它不符合
A. 构造原理 B. 泡利原理 C. 洪特规则
(2)一个J原子(基态)中未成对电子数为
(3)K位于元素周期表中第
(4)根据对角线规则及已知元素性质,写出B、E元素最高价氧化物的水化物在溶液反应的离子方程式
(5)下列有关说法正确的是_______
A.第一电离能 | B.氢化物稳定性 |
C.原子半径 | D.最高价含氧酸的酸性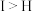 |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】已知A、B、C、D、E、F、G是原子序数依次递增的短周期元素,已知A和D为同一主族元素,C和F为同一主族元素,A元素的原子半径是所有主族元素中原子半径最小的,B原子的最外层电子数比次外层多3,G元素的最高正化合价与最低负化合价的代数和为6,E是同周期中金属离子半径最小的元素,F形成的化合物是形成酸雨的主要原因。请回答下列问题:
(1)写出B元素的名称:_____ 。
(2)写出C元素在周期表中的位置_____ 。
(3)E元素的原子结构示意图为_____ 。
(4)B、D、E三种元素的原子半径由大到小的顺序为_____ (填元素符号)。
(5)根据元素周期律,推断:
①C、F元素的氢化物还原性较强的是_____ (填对应氢化物的化学式)。
②F、G的元素最高价氧化物对应水化物酸性较强的是_____ (填对应酸的化学式)。
(6)由C、D形成的一种化合物可与水反应,生成标况下33.6L气体时转移的电子的物质的量为_____ 。
(7)G元素的单质有毒,可用D的最高价氧化物对应的水化物的溶液吸收,其离子方程式为_____ 。
(8)镓(Ga)与E同主族,工业制备镓的流程如图所示:
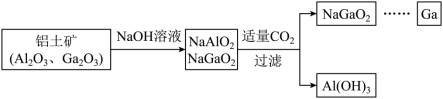
氢氧化镓与NaOH反应的化学方程式为_____ ;酸性:Al(OH)3_____ Ga(OH)3(填“>”或“<”)。
(1)写出B元素的名称:
(2)写出C元素在周期表中的位置
(3)E元素的原子结构示意图为
(4)B、D、E三种元素的原子半径由大到小的顺序为
(5)根据元素周期律,推断:
①C、F元素的氢化物还原性较强的是
②F、G的元素最高价氧化物对应水化物酸性较强的是
(6)由C、D形成的一种化合物可与水反应,生成标况下33.6L气体时转移的电子的物质的量为
(7)G元素的单质有毒,可用D的最高价氧化物对应的水化物的溶液吸收,其离子方程式为
(8)镓(Ga)与E同主族,工业制备镓的流程如图所示:

氢氧化镓与NaOH反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】A、B、C、D、E五种短周期元素(A、B、C、D、E分别代表元素符号),它们的原子序数依次增大;A是元素周期表中原子半径最小的元素;B元素最高价氧化物对应的水化物与其氢化物反应生成一种盐X;D与A同主族,且与E同周期;E元素原子的最外层电子数是其次外层电子数的3/4倍;C与E同主族。
请回答下列问题:
(1)X的化学式为_____ _,元素D与E形成的酸式盐的电子式:___ __。
(2)元素的非金属性C、E的强弱比较,下列各项中,能说明这一结论的事实有_____(填序号)。
①氢化物H2E的酸性比H2C强
②氢化物H2C的热稳定性比H2E强
③氢化物H2E的水溶液放置在空气中会变浑浊
(3)将由BC和BC2组成的混合气体通入下图所示装置中,用来验证浓硝酸的氧化性比稀硝酸的氧化性强。

已知(ⅰ) 浓硝酸能将气体BC氧化成BC2,而稀硝酸不能氧化BC。
(ⅱ) NaOH溶液与BC2反应的化学方程式为:2NaOH+2BC2═NaBC2+NaBC3+H2O ;NaOH溶液与BC气体不反应。
a.装置①、②中盛放的药品依次是______、______。
b.能够说明实验已成功的现象是 __ ____。
请回答下列问题:
(1)X的化学式为_____ _,元素D与E形成的酸式盐的电子式:___ __。
(2)元素的非金属性C、E的强弱比较,下列各项中,能说明这一结论的事实有_____(填序号)。
①氢化物H2E的酸性比H2C强
②氢化物H2C的热稳定性比H2E强
③氢化物H2E的水溶液放置在空气中会变浑浊
(3)将由BC和BC2组成的混合气体通入下图所示装置中,用来验证浓硝酸的氧化性比稀硝酸的氧化性强。

已知(ⅰ) 浓硝酸能将气体BC氧化成BC2,而稀硝酸不能氧化BC。
(ⅱ) NaOH溶液与BC2反应的化学方程式为:2NaOH+2BC2═NaBC2+NaBC3+H2O ;NaOH溶液与BC气体不反应。
a.装置①、②中盛放的药品依次是______、______。
b.能够说明实验已成功的现象是 __ ____。
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】如表列出了①~⑪11种元素在周期表中的位置。
(1)上述元素中,最不活泼的是(填元素符号,下同)____ ,金属性最强的是___ ,①⑥⑦三种元素的原子半径由大到小的顺序是___ 。
(2)上述元素的最高价氧化物对应的水化物中酸性最强的是___ (填化学式,下同),呈两性的氢氧化物是___ 。
(3)元素②的简单氢化物的电子式为___ ;比较②和⑧简单氢化物的稳定性由强到弱的顺序是___ (填化学式)。
(4)元素③和⑤形成的具有非极性共价键的化合物的电子式是___ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||
| 4 | ⑩ | ⑪ |
(2)上述元素的最高价氧化物对应的水化物中酸性最强的是
(3)元素②的简单氢化物的电子式为
(4)元素③和⑤形成的具有非极性共价键的化合物的电子式是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】A、B、C、D都是短周期元素,原子半径D>C>A>B,其中A、B处于同一周期,A、C处于同一主族。C原子核内的质子数等于A、B原子核内的质子数之和,C原子最外层电子数是D原子最外层电子数的4倍。试回答下列问题。
(1)这4种元素分别是:A________ ,B________ ,C________ ,D________ (填元素名称)。
(2)这4种元素中能形成的气态氢化物的稳定性由大到小的顺序______________________ 。
(3)A与B形成的三原子分子的化学式是__________ ,B与D形成的原子个数之比为1:1的化合物的化学式是____________________ 。
(4)A元素的某氧化物与D元素的某含氧化合物反应生成单质的化学方程式是____________________ 。
(1)这4种元素分别是:A
(2)这4种元素中能形成的气态氢化物的稳定性由大到小的顺序
(3)A与B形成的三原子分子的化学式是
(4)A元素的某氧化物与D元素的某含氧化合物反应生成单质的化学方程式是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】A、B、C、D、E、F、G、H 是八种短周期主族元素。根据下表完成后面填空:(所有空都用元素符号或化学式填写)
(1)表中所标出的A、B、C、D、E、F 六种元素中,原子半径最大的元素是___________ , 非金属性最强的元素是___________ ,这两种元素形成的化合物可能的化学式是___________ 。(任写一种)
(2)写出F的核外电子排布式___________ 。F 的最高价氧化物对应的水化物能与E的最高价氧化物对应的水化物发生反应,写出该反应的方程式___________ 。
(3)D元素和G元素的非金属性强弱为___________ ,用一个事例或方程式来表现这个强弱___________ 。
(4)A、B、D、E 四种元素所形成的化合物是___________ ,侯氏制碱法的第一步即制取该物质,写出该步骤的化学方程式: __________ 。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | A | |||||||
| 2 | B | C | D | |||||
| 3 | E | F | G | H | ||||
(2)写出F的核外电子排布式
(3)D元素和G元素的非金属性强弱为
(4)A、B、D、E 四种元素所形成的化合物是
您最近一年使用:0次



