下列有关分子结构的描述正确的是
A. 中心原子为 中心原子为 杂化,分子呈三角锥形 杂化,分子呈三角锥形 |
B. 的 的 模型为V形,能与 模型为V形,能与 形成配位键 形成配位键 |
C. 分子为平面三角形,分子中含3个σ键和一个π键 分子为平面三角形,分子中含3个σ键和一个π键 |
D. 为正四面体形分子,能与水分子形成分子间氢键 为正四面体形分子,能与水分子形成分子间氢键 |
更新时间:2022-05-13 14:44:19
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列说法错误的是
| A.在现代化学中,常利用原子光谱中的特征谱线来鉴定元素 |
B.H-Cl中是p-p 键 键 |
C.1mol丙酮(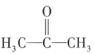 )分子中含有 )分子中含有 键的数目为 键的数目为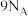 |
| D.一般来说,分子的极性越大,范德华力越大 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】设 为阿伏加德罗常数的值,下列叙述正确的是
为阿伏加德罗常数的值,下列叙述正确的是
 为阿伏加德罗常数的值,下列叙述正确的是
为阿伏加德罗常数的值,下列叙述正确的是A. 苯分子含碳碳双键数目为 苯分子含碳碳双键数目为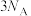 |
B. 正丁烷和 正丁烷和 异丁烷的混合物中共价键数目为 异丁烷的混合物中共价键数目为 |
C.常温常压下, 乙烯含 乙烯含 键数目为 键数目为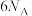 |
D. 羟基所含电子数为 羟基所含电子数为 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列各组物质性质的比较,结论正确的是
A.分子的极性: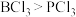 | B.沸点:邻羟基苯甲酸<对羟基苯甲酸 |
C.熔点: | D.硬度:C(金刚石)<SiC |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】用价层电子对互斥理论(VSEPR)可以预测许多分子或离子的空间构型,有时也能用来推测键角大小,下列判断正确的是
| A.SO2、CS2、HCN都是直线形的分子 | B.BF3键角为120°,SnBr2键角大于120° |
C.CH2O、CO 、SO3都是平面三角形的粒子 、SO3都是平面三角形的粒子 | D.PCl3、NH3、PCl5都是三角锥形的分子 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】超氧化钾( )与
)与 反应会生成
反应会生成 并放出
并放出 ,下列说法正确的是
,下列说法正确的是
 )与
)与 反应会生成
反应会生成 并放出
并放出 ,下列说法正确的是
,下列说法正确的是A. 中K的化合价为+2 中K的化合价为+2 | B. 的空间结构为平面三角形 的空间结构为平面三角形 |
C. 的空间填充模型为 的空间填充模型为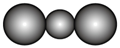 | D. 只含离子键 只含离子键 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】反应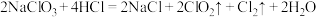 可制含氯消毒剂。下列说法正确的是
可制含氯消毒剂。下列说法正确的是
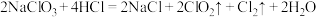 可制含氯消毒剂。下列说法正确的是
可制含氯消毒剂。下列说法正确的是| A.HCl和NaCl所含化学键类型相同 |
B. 是由极性键构成的非极性分子 是由极性键构成的非极性分子 |
C. 的空间结构为三角锥形 的空间结构为三角锥形 |
D.中子数为18的Cl原子: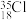 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列物质的变化规律,与共价键的键能有关的是
| A.F2、Cl2、Br2、I2的熔、沸点逐渐升高 |
| B.HF的熔、沸点高于HCl |
| C.金刚石的硬度、熔点、沸点都高于晶体硅 |
| D.NaF、NaCl、NaBr、NaI的熔点依次降低 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】关于化合物 ,下列叙述正确的是( )
,下列叙述正确的是( )
 ,下列叙述正确的是( )
,下列叙述正确的是( )| A.分子间可形成氢键 | B.分子中既有极性键又有非极性键 |
| C.分子中有7个σ键和1个π键 | D.该分子在水中的溶解度小于2-丁烯 |
您最近半年使用:0次

 可用于印染、畜牧等领域,其晶体的部分结构如下图所示。下列说法正确的是
可用于印染、畜牧等领域,其晶体的部分结构如下图所示。下列说法正确的是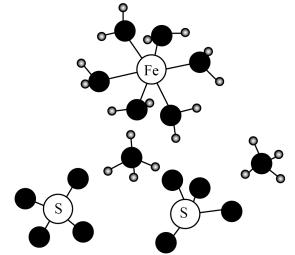
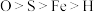
 的价层电子排布式为
的价层电子排布式为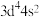
 和
和 原子的轨道杂化类型均为
原子的轨道杂化类型均为


