锂、铍等金属广泛应用于航空航天、核能和新能源汽车等高新产业。一种从萤石矿(主要含BeO、Li2O、CaF2及少量CaCO3、SiO2、FeO、Fe2O3、Al2O3)中提取的工艺如图:
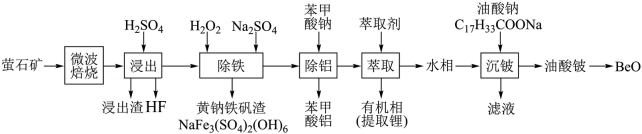
已知:苯甲酸是一元弱酸,白色片状晶体,常温下微溶于水,随温度升高,溶解度增大。
回答下列问题:
(1)“微波焙烧”使矿物内部变得疏松多孔,目的是__________ 。
(2)浸出渣的主要成分是__________ ,“除铁”中可替代H2O2的物质是__________ 。
(3)“除铁”中发生反应的离子方程式:__________ 、__________ 。
(4)“除铝”时,溶液的pH越小,铝的去除率__________ (填“越高”、“越低”或“不变”)。利用“除铝”所得苯甲酸铝沉淀再生苯甲酸的方案为:将苯甲酸铝沉淀溶于热的稀硫酸中,__________ 。
(5)由油酸铍制备BeO的方法是高温焙烧,检验焙烧已完全的操作实验为________ 。

已知:苯甲酸是一元弱酸,白色片状晶体,常温下微溶于水,随温度升高,溶解度增大。
回答下列问题:
(1)“微波焙烧”使矿物内部变得疏松多孔,目的是
(2)浸出渣的主要成分是
(3)“除铁”中发生反应的离子方程式:
(4)“除铝”时,溶液的pH越小,铝的去除率
(5)由油酸铍制备BeO的方法是高温焙烧,检验焙烧已完全的操作实验为
2022·山东泰安·模拟预测 查看更多[3]
湖南省株洲市第一中学2021届高三下学期第二次模拟检测化学试题(已下线)第05练 以简单工业流程突破金属及其化合物-2022年【暑假分层作业】高二化学(2023届一轮复习通用)山东省肥城市2022届高考适应性训练(一)化学试题
更新时间:2022-05-16 18:38:45
|
相似题推荐
【推荐1】明矾[KAl(SO4)2·12H2O]在生产、生活中有广泛用途:饮用水的净化;造纸工业上作施胶剂;食品工业的发酵剂等。利用炼铝厂的废料(主要含Al、Al2O3及少量SiO2和FeO·xFe2O3)可制备明矾。工艺流程如图:

(1)“酸浸”过程中的应选择____ (写酸的化学式),适当增大酸的浓度、将废料粉碎可提高浸出速率。
(2)操作Ⅰ的名称是___ ,浸渣1的主要成分是____ 。
(3)检验溶液A中是否存在Fe2+的实验操作是____ 。
(4)将炼铝厂废料投入氢氧化钠溶液中生成气体的化学方程式是____ ,在溶液A中加入酸性高锰酸钾发生反应的离子方程式为____ 。
(5)已知:生成氢氧化物沉淀的pH如表所示
调节pH=3的目的是____ 。

(1)“酸浸”过程中的应选择
(2)操作Ⅰ的名称是
(3)检验溶液A中是否存在Fe2+的实验操作是
(4)将炼铝厂废料投入氢氧化钠溶液中生成气体的化学方程式是
(5)已知:生成氢氧化物沉淀的pH如表所示
| Al(OH)3 | Fe(OH)2 | Fe(OH)3 | |
| 开始沉淀时 | 3.4 | 6.3 | 1.5 |
| 完全沉淀时 | 4.7 | 8.3 | 2.8 |
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】新型锂电池正极材料 有望取代广泛使用的
有望取代广泛使用的 ,由软锰矿(主要成分为
,由软锰矿(主要成分为 ,还含有少量
,还含有少量 、FeO、
、FeO、 、
、 等杂质)为原料制备锰酸锂的流程如图:
等杂质)为原料制备锰酸锂的流程如图: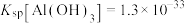 ,
,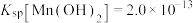 ;
;
②离子浓度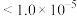 mol⋅L-1时除尽;
mol⋅L-1时除尽;
回答下列问题:
(1)软锰矿水磨浆化处理的作用是___________ 。
(2)锂电池放电时正极反应式为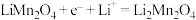 ,则锰酸锂中锰元素的化合价为
,则锰酸锂中锰元素的化合价为___________ 。
(3)用 代替
代替 氧化除杂,反应物利用率会更高,理由是
氧化除杂,反应物利用率会更高,理由是___________ 。
(4)调pH时加入的X不能选用下列物质的是______。
(5)常温下,调节 ,除去
,除去 、
、 ,写出
,写出 已经除尽的计算过程:
已经除尽的计算过程:___________ 。
(6)其他条件一定,沉锰过程中 的沉淀率与溶液温度的关系如下图。:50℃后,随溶液温度升高,
的沉淀率与溶液温度的关系如下图。:50℃后,随溶液温度升高, 的沉淀率下降的原因是
的沉淀率下降的原因是___________ 。 反应的化学方程式为
反应的化学方程式为___________ 。
(8)一种锰的氧化物四方晶胞结构如图所示,该晶胞由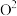 和
和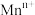 构成。
构成。___________ ,基态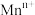 的价层电子轨道表示式为
的价层电子轨道表示式为___________ 。
 有望取代广泛使用的
有望取代广泛使用的 ,由软锰矿(主要成分为
,由软锰矿(主要成分为 ,还含有少量
,还含有少量 、FeO、
、FeO、 、
、 等杂质)为原料制备锰酸锂的流程如图:
等杂质)为原料制备锰酸锂的流程如图: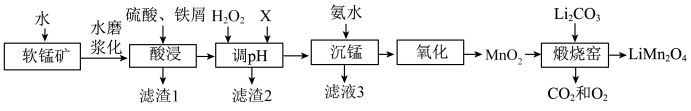
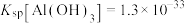 ,
,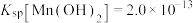 ;
;②离子浓度
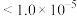 mol⋅L-1时除尽;
mol⋅L-1时除尽;回答下列问题:
(1)软锰矿水磨浆化处理的作用是
(2)锂电池放电时正极反应式为
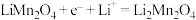 ,则锰酸锂中锰元素的化合价为
,则锰酸锂中锰元素的化合价为(3)用
 代替
代替 氧化除杂,反应物利用率会更高,理由是
氧化除杂,反应物利用率会更高,理由是(4)调pH时加入的X不能选用下列物质的是______。
| A.NaOH | B.氨水 | C. | D. |
(5)常温下,调节
 ,除去
,除去 、
、 ,写出
,写出 已经除尽的计算过程:
已经除尽的计算过程:(6)其他条件一定,沉锰过程中
 的沉淀率与溶液温度的关系如下图。:50℃后,随溶液温度升高,
的沉淀率与溶液温度的关系如下图。:50℃后,随溶液温度升高, 的沉淀率下降的原因是
的沉淀率下降的原因是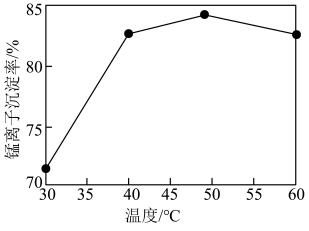
 反应的化学方程式为
反应的化学方程式为(8)一种锰的氧化物四方晶胞结构如图所示,该晶胞由
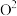 和
和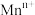 构成。
构成。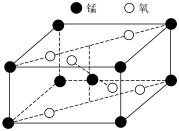
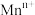 的价层电子轨道表示式为
的价层电子轨道表示式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】某化学研究小组以铜为电极电解饱和食盐水,探究过程如下:
【实验1】:如右下图装置,电源接通后,与电池负极相连的铜丝上有大量气泡产生;与电池正极相连的铜丝由粗变细。电解开始30s内,阳极附近出现白色浑浊,然后开始出现橙黄色浑浊,此时测定溶液的pH约为10。随着沉淀量的逐渐增加,橙黄色沉淀慢慢聚集在试管底部,溶液始终未出现蓝色。

【实验2】:将实验1中试管底部的橙黄色沉淀取出,分装在两
支小试管中,以后的操作和现象如下:
阅读资料:常见铜的化合物颜色如下:
请回答下列问题:
(1)铜的常见正化合价为________ 、_______ ,最终试管底部橙黄色沉淀的化学式___________ 。
(2) 电解开始30s内,阴极上发生的反应为:_________ 、阳极上发生的反应为:___________ 。
(3)写出实验2中①、②的离子方程式:①_______________ ;②___________________ 。
【实验1】:如右下图装置,电源接通后,与电池负极相连的铜丝上有大量气泡产生;与电池正极相连的铜丝由粗变细。电解开始30s内,阳极附近出现白色浑浊,然后开始出现橙黄色浑浊,此时测定溶液的pH约为10。随着沉淀量的逐渐增加,橙黄色沉淀慢慢聚集在试管底部,溶液始终未出现蓝色。

【实验2】:将实验1中试管底部的橙黄色沉淀取出,分装在两
支小试管中,以后的操作和现象如下:
| 序号 | 操作 | 现象 |
| ① | 滴入稀硝酸溶液 | 沉淀溶解,有无色气泡产生,最终得到蓝色溶液。 |
| ② | 滴入稀硫酸溶液 | 橙黄色沉淀转变为紫红色不溶物,溶液呈现蓝色 |
| 物质 | 颜色 | 物质 | 颜色 |
| 氯化铜 | 固体呈棕色,浓溶液呈绿色,稀溶液呈蓝色 | 氢氧化亚铜(不稳定) | 橙黄色 |
| 碱式氯化铜 | 绿色 | 氢氧化铜 | 蓝色 |
| 氧化亚铜 | 砖红色或橙黄色 | 氯化亚铜 | 白色 |
请回答下列问题:
(1)铜的常见正化合价为
(2) 电解开始30s内,阴极上发生的反应为:
(3)写出实验2中①、②的离子方程式:①
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】绿矾(FeSO4·7H2O)是治疗缺铁性贫血药品的重要成分,某化学兴趣小组利用工厂的废铁屑(主要成分为Fe,此外还含有少量Cu、Al,Al2O3和Fe2O3)制备磁性Fe3O4胶体粒子、绿矾和净水剂Na2FeO4的实验流程如图:
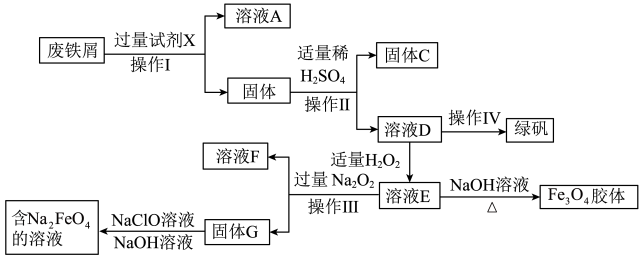
请回答下列问题:
(1)试剂X为_____ ,操作Ⅰ、Ⅱ、Ⅲ均为______ 操作。
(2)固体C为_____ ,溶液D中加入KSCN溶液,无血红色产生,原因是_____ (用离子方程式表示)。
(3)D中加入适量H2O2生成E的离子方程式_____ ;若D中含amolFe2+,则理论上加入_____ molH2O2可使溶液E中铁元素恰好转化为Fe3O4胶体。
(4)证明Fe3O4胶体已经生成的方法是_____ 。
(5)Na2FeO4中铁元素的化合价为______ ,据此可推断其在水处理过程中具有_____ 的作用,由固体G生成Na2FeO4的离子方程式为______ 。

请回答下列问题:
(1)试剂X为
(2)固体C为
(3)D中加入适量H2O2生成E的离子方程式
(4)证明Fe3O4胶体已经生成的方法是
(5)Na2FeO4中铁元素的化合价为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】钴蓝(化学式Al2CoO4)是一种耐热、耐光、耐酸、耐碱腐蚀的蓝色颜料。某企业利用含铝锂钴废料(铝箱、CoO和Co2O3、Li2O)制备钴蓝的工艺流程如下:
回答下列问题:
(1)碱浸时要有防火、防爆措施,原因是______ ,操作I的内容是_______ 。
(2)在实验室模拟工业生产时,也可用盐酸酸浸出钴,但实际工业生产中却不用盐酸,请 从反应原理分析不用盐酸浸出钴的主要原因___ 。
(3)写出“还原”过程中反应的离子方程式____ 。
(4)料渣2的主要成分是A1(OH)3 、____ ,写出灼烧时反应的化学方程式______ 。
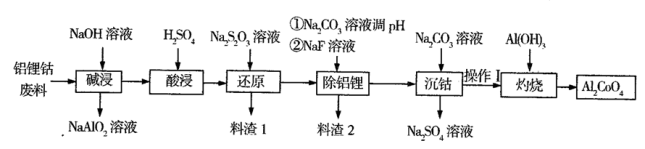
回答下列问题:
(1)碱浸时要有防火、防爆措施,原因是
(2)在实验室模拟工业生产时,也可用盐酸酸浸出钴,但实际工业生产中却不用盐酸,请 从反应原理分析不用盐酸浸出钴的主要原因
(3)写出“还原”过程中反应的离子方程式
(4)料渣2的主要成分是A1(OH)3 、
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】以镍黄铁矿为原料制备 的工艺流程如下:
的工艺流程如下:

已知:①高镍锍的主要成分为 、
、 、
、 、
、 的低价硫化物及合金;
的低价硫化物及合金;
②氧化性: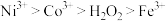 ;
;
③ ,
,  ,
, 。
。
回答下列问题:
(1)“酸浸”时,H2SO4溶液需过量,其目的是________ 。
(2)“过滤”时滤渣1的主要成分是________ 。
(3)“氧化”时反应的化学方程式为_________ ,若用NaClO代替H2O2溶液,使0.2molFe2+转化为Fe3+,则需NaClO至少为___ mol。
(4)“除铁”的原理是_________ 。
(5)“除钴”时,发生反应的离子方程式为____________ 。
(6)“沉镍”后需过滤、洗涤,证明沉淀已洗涤干净的方法是_____ 。若“沉镍”后的滤液中 ,则滤液的pH>
,则滤液的pH>____
 的工艺流程如下:
的工艺流程如下:
已知:①高镍锍的主要成分为
 、
、 、
、 、
、 的低价硫化物及合金;
的低价硫化物及合金;②氧化性:
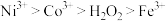 ;
;③
 ,
,  ,
, 。
。回答下列问题:
(1)“酸浸”时,H2SO4溶液需过量,其目的是
(2)“过滤”时滤渣1的主要成分是
(3)“氧化”时反应的化学方程式为
(4)“除铁”的原理是
(5)“除钴”时,发生反应的离子方程式为
(6)“沉镍”后需过滤、洗涤,证明沉淀已洗涤干净的方法是
 ,则滤液的pH>
,则滤液的pH>
您最近一年使用:0次



