元素周期表是学习物质结构与性质的重要工具, 如图所示是元素周期表前三周期的一部分。下到关于五种元素的叙述正确的是
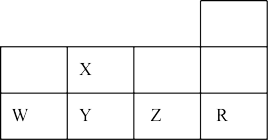

| A.Z的基态原子最外层p轨道上有2个未成对电子 |
| B.WZ3分子的VSEPR模型为三角锥形 |
| C.H2Y键角小于H2X |
| D.第一电离能:R>Y>W |
更新时间:2022-05-26 21:47:52
|
相似题推荐
多选题
|
适中
(0.65)
【推荐1】短周期主族元素M、W、X、Y、Z的原子序数依次递增。M最高正价与最低负价的绝对值之和等于2,X在短周期元素中原子半径最大,W和X的最外层电子数之和等于Z的最外层电子数,Y最外层电子数是电子层数的2倍。下列说法正确的是
| A.离子半径:Z-<X+ |
| B.由W与X形成的一种化合物可作供氧剂 |
| C.最高价氧化物对应的水化物的酸性:Y>Z |
| D.气态氢化物的稳定性:W>Y |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐2】X、Y、Z、M、Q五种短周期主族元素,原子序数依次增大。X的核外电子数等于其周期数,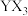 分子呈三角锥形,Z的核外电子数等于X、Y核外电子数之和。M与X同主族,Q是同周期中非金属性最强的元素。下列说法正确的是
分子呈三角锥形,Z的核外电子数等于X、Y核外电子数之和。M与X同主族,Q是同周期中非金属性最强的元素。下列说法正确的是
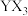 分子呈三角锥形,Z的核外电子数等于X、Y核外电子数之和。M与X同主族,Q是同周期中非金属性最强的元素。下列说法正确的是
分子呈三角锥形,Z的核外电子数等于X、Y核外电子数之和。M与X同主族,Q是同周期中非金属性最强的元素。下列说法正确的是| A.X与Z形成的10电子微粒有2种 |
| B.Z与Q形成的一种化合物可用于饮用水的消毒 |
C.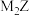 与 与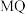 都是离子化合物 都是离子化合物 |
| D.由X、Y、Z三种元素组成的化合物的水溶液均显酸性 |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐1】下列Li原子电子排布图表示的状态中,能量最高和最低的分别为。
A. | B.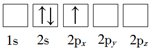 |
C. | D.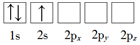 |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐2】下列有关轨道表示式的表述正确的是
A. 可表示单核10电子粒子基态时的电子排布 可表示单核10电子粒子基态时的电子排布 |
B. 违背了洪特规则 违背了洪特规则 |
C. 表示基态N原子的价层电子排布道表示式 表示基态N原子的价层电子排布道表示式 |
D. 表示处于激发态的B原子的轨 表示处于激发态的B原子的轨 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐3】某离子液体的阴离子的结构如图所示,其中W、X、Y、Z、M为原子序数依次增大的短周期非金属元素,W是有机分子的骨架元素。下列说法正确的是


A.Z元素的最高价态为 | B.基态原子未成对电子数:W=Y |
| C.该阴离子中X不满足8电子稳定结构 | D.基态M原子核外有5种能量不同的电子 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列对有关事实的解释错误的是
| 选项 | 事实 | 解释 |
| A | SiO2的熔点比干冰高 | SiO2晶体是共价晶体,分子间作用力大 |
| B | HF的热稳定性比HCl强 | H—F比H—Cl的键能大 |
| C | CO2与SO2的空间结构不同 | 中心原子杂化方式相同,孤电子对数不同 |
| D | 某些金属盐灼烧时呈现不同焰色 | 电子从低能级轨道跃迁至高能级轨道后,又从高能级轨道跃迁至低能级轨道,释放出不同波长的光 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列关于粒子结构的描述不正确的是
| A.H2S和NH3均是价电子总数为8的极性分子,且H2S分子的键角较小 |
| B.HS﹣和HCl均是含一个非极性键的18电子微粒 |
| C.1 mol D216O中含中子、质子、电子各10 NA(NA代表阿伏加德罗常数的值) |
| D.CH2Cl2和CCl4均是四面体构型的极性分子 |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐1】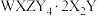 可用作膳食补充剂、药物制剂的压片剂及用于一些旨在消除体味的产品中已知X、Y、Z、W为原子序数依次增大的前20号主族元素,四种元素均位于不同周期。其中X、Y、Z三种元素原子序数为等差数列,基态Y原子s轨道电子数与p轨道电子数相等,基态W原子核外无未成对电子。下列说法正确的是
可用作膳食补充剂、药物制剂的压片剂及用于一些旨在消除体味的产品中已知X、Y、Z、W为原子序数依次增大的前20号主族元素,四种元素均位于不同周期。其中X、Y、Z三种元素原子序数为等差数列,基态Y原子s轨道电子数与p轨道电子数相等,基态W原子核外无未成对电子。下列说法正确的是
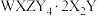 可用作膳食补充剂、药物制剂的压片剂及用于一些旨在消除体味的产品中已知X、Y、Z、W为原子序数依次增大的前20号主族元素,四种元素均位于不同周期。其中X、Y、Z三种元素原子序数为等差数列,基态Y原子s轨道电子数与p轨道电子数相等,基态W原子核外无未成对电子。下列说法正确的是
可用作膳食补充剂、药物制剂的压片剂及用于一些旨在消除体味的产品中已知X、Y、Z、W为原子序数依次增大的前20号主族元素,四种元素均位于不同周期。其中X、Y、Z三种元素原子序数为等差数列,基态Y原子s轨道电子数与p轨道电子数相等,基态W原子核外无未成对电子。下列说法正确的是A.第一电离能: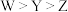 |
B.最简单氢化物的熔、沸点: |
| C.上述化合物的固体为分子晶体 |
| D.Z的最高价氧化物的水化物的阴离子空间结构为正四面体形 |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐2】《科学》杂志发表了中国科学家的原创性重大突破——首次在实验室实现CO2到淀粉的合成的文章,其合成路线如图所示,下列说法正确的是


| A.淀粉分子中含有π键 |
B. 的空间结构为平面三角形 的空间结构为平面三角形 |
C.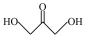 为手性分子。 为手性分子。 |
| D.HCHO中键角:∠OCH大于∠HCH |
您最近一年使用:0次


 分子一定为平面三角形
分子一定为平面三角形


