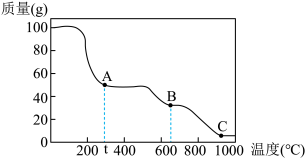
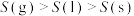750℃时, 和
和 发生的两个反应的方程式分别如下:
发生的两个反应的方程式分别如下:
①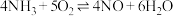 ;
;
② ;
;
下列说法正确的是
 和
和 发生的两个反应的方程式分别如下:
发生的两个反应的方程式分别如下:①
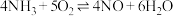 ;
;
②
 ;
;
下列说法正确的是
A.反应①的平衡常数可表示为 |
B.反应②的 |
C.如希望 尽可能转化为NO,可利用催化剂的选择性 尽可能转化为NO,可利用催化剂的选择性 |
D.反应②的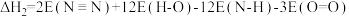 |
21-22高三下·江苏南京·阶段练习 查看更多[3]
(已下线)江苏省2022年普通高中学业水平选择性考试变式题(选择题6-10)(已下线)2022年江苏卷高考真题变式题1-13江苏省南京师范大学附属中学2022届高三下学期5月(第二十三次)模拟考试化学试题
更新时间:2022-05-30 17:21:28
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
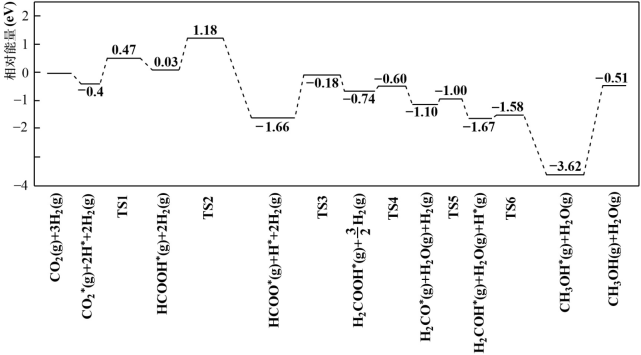
【推荐1】反应CO2(g)+3H2(g) CH3OH(g)+H2O(g)使用不同催化剂的调控中,研究发现,一定条件下,Pt单原子催化剂有着高达90.3%的甲醇选择性。反应历程如图所示,其中吸附在催化剂表面上的物种用“*”表示,“TS”表示过渡态。下列说法正确的是( )
CH3OH(g)+H2O(g)使用不同催化剂的调控中,研究发现,一定条件下,Pt单原子催化剂有着高达90.3%的甲醇选择性。反应历程如图所示,其中吸附在催化剂表面上的物种用“*”表示,“TS”表示过渡态。下列说法正确的是( )
 CH3OH(g)+H2O(g)使用不同催化剂的调控中,研究发现,一定条件下,Pt单原子催化剂有着高达90.3%的甲醇选择性。反应历程如图所示,其中吸附在催化剂表面上的物种用“*”表示,“TS”表示过渡态。下列说法正确的是( )
CH3OH(g)+H2O(g)使用不同催化剂的调控中,研究发现,一定条件下,Pt单原子催化剂有着高达90.3%的甲醇选择性。反应历程如图所示,其中吸附在催化剂表面上的物种用“*”表示,“TS”表示过渡态。下列说法正确的是( )
| A.经历TS1,CO2共价键发生断裂,且生成羧基 |
| B.Pt为固体催化剂,其表面积对催化效果无影响 |
C.能垒(活化能)为1.48eV的反应为HCOOH*(g)+2H2(g)=H2COOH*(g)+ H2 H2 |
| D.如果换用铜系催化剂,所得反应历程与图示相同 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】已知: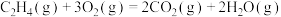
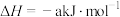


其他数据如下表:
下列说法正确的是
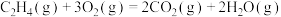
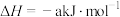


其他数据如下表:
| 化学键 | C=O | O=O | C-H | O-H | C=C |
键能/( ) ) | 798 | x | 413 | 463 | 615 |
A.乙烯的燃烧热为 |
B.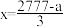 |
C.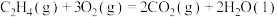 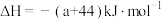 |
| D.当生成4molO-H键时,该反应放出热量一定为akJ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】反应2CO2(g)+6H2(g) C2H4(g)+4H2O(g)是综合利用CO2的热点研究领域——催化加氢合成乙烯的重要反应。该反应往往伴随副反应,生成C3H6、C3H8、C4H8等低碳烃。下列有关催化加氢合成乙烯重要反应的说法正确的是
C2H4(g)+4H2O(g)是综合利用CO2的热点研究领域——催化加氢合成乙烯的重要反应。该反应往往伴随副反应,生成C3H6、C3H8、C4H8等低碳烃。下列有关催化加氢合成乙烯重要反应的说法正确的是
 C2H4(g)+4H2O(g)是综合利用CO2的热点研究领域——催化加氢合成乙烯的重要反应。该反应往往伴随副反应,生成C3H6、C3H8、C4H8等低碳烃。下列有关催化加氢合成乙烯重要反应的说法正确的是
C2H4(g)+4H2O(g)是综合利用CO2的热点研究领域——催化加氢合成乙烯的重要反应。该反应往往伴随副反应,生成C3H6、C3H8、C4H8等低碳烃。下列有关催化加氢合成乙烯重要反应的说法正确的是| A.该反应ΔH<0,ΔS>0 |
B.该反应的平衡常数K=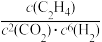 |
| C.用E表示键能,该反应ΔH=4E(C=O)+6E(H-H)-4E(C-H)-8E(H-O) |
| D.一定温度和压强条件下,选用合适的催化剂可以提高反应速率和乙烯选择性 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】常温时,分别改变相同物质的量浓度的H2CO3和氨水的pH,H2CO3、HCO3-、CO32-物质的量分数 (δ)及NH3·H2O、NH4+的物质的量分数(δ)如下图所示(不考虑溶液中的CO2和NH3分子):
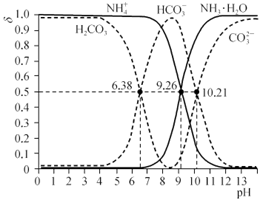
[已知δ=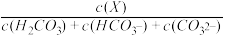 、δ=
、δ=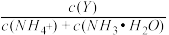 ]
]
下列说法正确的是

[已知δ=
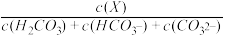 、δ=
、δ=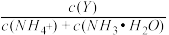 ]
]下列说法正确的是
| A.NH4HCO3溶液显酸性 |
| B.pH=5时,c(HCO3-)>c(H2CO3) >c(CO32-) |
| C.lgK1(H2CO3)=6.38 |
| D.HCO3-+ NH3·H2O=NH4++CO32-+H2O的lgK=-0.95 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】某工业生产中发生反应:2A(g)+B(g) 2M(g) ΔH>0。下列有关该工业生产的说法不正确的是
2M(g) ΔH>0。下列有关该工业生产的说法不正确的是
 2M(g) ΔH>0。下列有关该工业生产的说法不正确的是
2M(g) ΔH>0。下列有关该工业生产的说法不正确的是| A.工业上合成M时,一定采用高压条件,因为高压有利于M的生成 |
| B.若物质B价廉易得,工业上一般采用加入过量的B以提高A的转化率 |
| C.工业上一般采用较高温度合成M,因温度越高,反应物的转化率越高 |
| D.工业生产中常采用催化剂,因为生产中使用催化剂可提高M的日产量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】已知放热反应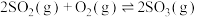 ,若起始时按
,若起始时按 和
和 物质的量比2:1投料,反应达到平衡时
物质的量比2:1投料,反应达到平衡时 的转化率(%)随温度和压强变化如下表:
的转化率(%)随温度和压强变化如下表:
下列说法不正确 的是
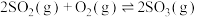 ,若起始时按
,若起始时按 和
和 物质的量比2:1投料,反应达到平衡时
物质的量比2:1投料,反应达到平衡时 的转化率(%)随温度和压强变化如下表:
的转化率(%)随温度和压强变化如下表:| 温度/℃ | 平衡时 的转化率/% 的转化率/% | ||||
| 0.1MPa | 0.5MPa | 1MPa | 2.5MPa | 5MPa | |
| 400 | 99.2 | 99.6 | 99.7 | 99.8 | 99.9 |
| 450 | 97.5 | 98.9 | 99.2 | 99.5 | 99.6 |
| 500 | 93.5 | 96.9 | 97.8 | 98.6 | 99.0 |
A.反应过程中, 和 和 的转化率始终相等 的转化率始终相等 |
B.降低温度或增大压强,可使 的转化率达到100% 的转化率达到100% |
| C.其他条件不变,升高温度,正反应速率和逆反应速率均增大 |
| D.实际生产中,该反应常采用400~500℃、常压并使用催化剂 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】碳酸铵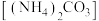 在室温下能自发分解产生氨气、水和二氧化碳,下列说法正确的是
在室温下能自发分解产生氨气、水和二氧化碳,下列说法正确的是
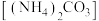 在室温下能自发分解产生氨气、水和二氧化碳,下列说法正确的是
在室温下能自发分解产生氨气、水和二氧化碳,下列说法正确的是| A.碳酸铵分解是因为生成了易挥发的气体,使体系的熵增大 |
| B.碳酸铵分解是吸热反应,体系的熵减小 |
| C.碳酸铵分解是吸热反应,根据焓判据能说明它能自发分解 |
| D.碳酸盐都不稳定,室温下都能自发分解 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】已知体系自由能变化ΔG=ΔH-TΔS。已知两个反应的ΔG与温度的关系如图所示,下列说法不正确的是
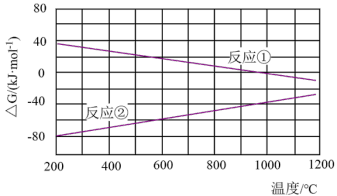
已知:ΔH和ΔS随温度变化很小

已知:ΔH和ΔS随温度变化很小
| A.反应②的ΔS<0 | B.反应①在1200℃时能自发进行 |
| C.在一定温度范围内,反应①②均能自发 | D.反应②的ΔH>0 |
您最近一年使用:0次

 A(g)+2B(g)
A(g)+2B(g)