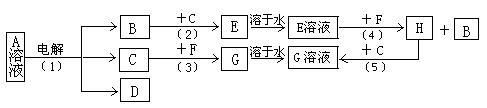
下列各物质均含有同一种元素,其中只有A和H为单质,A是目前用量最大、用途最广的合金的主要成分,H为黄绿色气体;C和F所含元素种类相同;将D的悬浊液露置在空气中,可观察到白色絮状沉淀迅速变为灰绿色,最后变为红褐色沉淀E,各物质间的转化关系如下图(部分反应物、生成物及反应条件已略去)
回答下列问题:
(1)A是_______ ,C是_______ (填化学式)。
(2)G的俗名为_______ 。
(3)若要除去F溶液中混有的C,应采取的实验操作为_______ ;若要除去C溶液中混有的F,涉及的化学反应的离子方程式为_______ 。
(4)写出D转化为E的化学反应方程式_______ 。
(5)人体正常的血红蛋白中含有D的阳离子,若误食亚硝酸盐,会导致血红蛋白中此阳离子被氧化而使人中毒。服用维生素C可以解毒,在此过程中体现了维生素C的_______ 性。

回答下列问题:
(1)A是
(2)G的俗名为
(3)若要除去F溶液中混有的C,应采取的实验操作为
(4)写出D转化为E的化学反应方程式
(5)人体正常的血红蛋白中含有D的阳离子,若误食亚硝酸盐,会导致血红蛋白中此阳离子被氧化而使人中毒。服用维生素C可以解毒,在此过程中体现了维生素C的
更新时间:2022-07-10 17:35:22
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
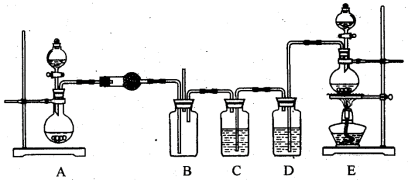
【推荐1】某研究性学习小组在查阅资料时发现,化工厂常用氨气来检验氯气是否泄漏,于是他们设计实验来探究氯气与氨气之间的反应。该小组设计的实验装置如下图
实验可用药品有:a.二氧化锰 b.浓盐酸 c.浓氨水 d.氯化铵 e.碱石灰 f.浓硫酸 g.饱和食盐水 h.NaOH 固体 i.消石灰
请回答下列问题:
(1)实验室制备氨气有多种方法。通常用加热固体混合物的方法制备氨气,反应的化学方程式是_____________ ,本实验中装置A 烧瓶内的固体可选用_______________ (填上述给定药品的序号)。
(2)装置E 的烧瓶中发生反应的离子方程式是_____________________ 。
(3)装置D 中盛装的药品是________________ (填序号),装置C的作用是_________________ 。
(4)通入B 装置的两根导管左边的较长、右边的较短,其目的是_________________________ 。
(5)实验中观察到装置B 内出现浓厚的白烟,并在容器壁上凝结成白色固体,白色固体的化学式为__________ 。

实验可用药品有:a.二氧化锰 b.浓盐酸 c.浓氨水 d.氯化铵 e.碱石灰 f.浓硫酸 g.饱和食盐水 h.NaOH 固体 i.消石灰
请回答下列问题:
(1)实验室制备氨气有多种方法。通常用加热固体混合物的方法制备氨气,反应的化学方程式是
(2)装置E 的烧瓶中发生反应的离子方程式是
(3)装置D 中盛装的药品是
(4)通入B 装置的两根导管左边的较长、右边的较短,其目的是
(5)实验中观察到装置B 内出现浓厚的白烟,并在容器壁上凝结成白色固体,白色固体的化学式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】铁是人类较早使用的金属之一、运用铁及其化合物的知识,完成下列问题。
Ⅰ.工业上用赤铁矿(含Fe2O3、FeO,也含有Al2O3、MnO2、CuO等)制备绿矾FeSO4·7H2O的流程如下:
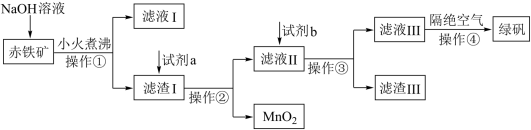
(1)赤铁矿中加入氢氧化钠溶液,发生反应的离子方程式为___________ 。
(2)图中加入的试剂a的名称为___________ ,试剂b的化学式为___________ 。
(3)操作④隔绝空气的目的是___________ 。
Ⅱ.(1)高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,比Cl2、O2、ClO2、KMnO4氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出,反应离子方程式为___________ 。
(2)干法制备高铁酸钠的主要反应为:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,该反应中Na2O2是___________ (填字母)
A.氧化剂B.还原剂C.既是氧化剂又是还原剂D.既不是氧化剂又不是还原剂
(3)湿法制备高铁酸钾的反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、 、Cl-、H2O。
、Cl-、H2O。
①写出碱性条件下湿法制高铁酸钾的离子反应方程式:___________ 。
②若反应过程中转移了0.9mol电子,则生成氧化产物的物质的量为___________ mol。
(4)球墨铸铁中含有一种铁碳化合物X。实验小组为测定X的组成设计实验如下:

固体2的俗名是铁红,则X的化学式可以表示为___________ 。
Ⅰ.工业上用赤铁矿(含Fe2O3、FeO,也含有Al2O3、MnO2、CuO等)制备绿矾FeSO4·7H2O的流程如下:

(1)赤铁矿中加入氢氧化钠溶液,发生反应的离子方程式为
(2)图中加入的试剂a的名称为
(3)操作④隔绝空气的目的是
Ⅱ.(1)高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,比Cl2、O2、ClO2、KMnO4氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出,反应离子方程式为
(2)干法制备高铁酸钠的主要反应为:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,该反应中Na2O2是
A.氧化剂B.还原剂C.既是氧化剂又是还原剂D.既不是氧化剂又不是还原剂
(3)湿法制备高铁酸钾的反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、
 、Cl-、H2O。
、Cl-、H2O。①写出碱性条件下湿法制高铁酸钾的离子反应方程式:
②若反应过程中转移了0.9mol电子,则生成氧化产物的物质的量为
(4)球墨铸铁中含有一种铁碳化合物X。实验小组为测定X的组成设计实验如下:

固体2的俗名是铁红,则X的化学式可以表示为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】某同学取海带灰加蒸馏水煮沸 ,冷却,过滤,获得含I-的溶液,并设计如图所示实验方案,从中提取I2。
,冷却,过滤,获得含I-的溶液,并设计如图所示实验方案,从中提取I2。
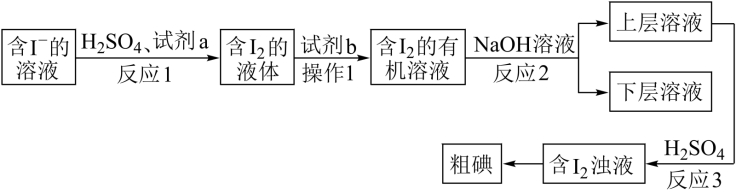
(1)反应1中硫酸的作用是提供酸性环境,则试剂a的作用是_______ 。
(2)试剂b应选择_______ (填标号)。
A.CCl4 B.酒精 C.醋酸
(3)操作1的名称是_______ 。实验室里进行操作1需要的玻璃仪器除烧杯外,还需要_______ ,有机层呈_______ 色
(4)反应2为3I2+6NaOH=5NaI+NaIO3+3H2O。此反应的氧化剂是_______ ,氧化产物是_______ 。
(5)反应3的离子方程式是_______ ,氧化产物和还原产物的物质的量之比_______
 ,冷却,过滤,获得含I-的溶液,并设计如图所示实验方案,从中提取I2。
,冷却,过滤,获得含I-的溶液,并设计如图所示实验方案,从中提取I2。
(1)反应1中硫酸的作用是提供酸性环境,则试剂a的作用是
(2)试剂b应选择
A.CCl4 B.酒精 C.醋酸
(3)操作1的名称是
(4)反应2为3I2+6NaOH=5NaI+NaIO3+3H2O。此反应的氧化剂是
(5)反应3的离子方程式是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】甲、乙是同主族非金属元素组成的单质,乙通常状况下是深红棕色液体。X、Y、Z是化合物。X溶液呈淡绿色,Y、Z的溶液都能使KSCN溶液变红。它们之间有如下图所示转化关系。
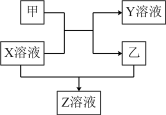
请回答:
(1)将Y的饱和溶液滴入沸水中,继续加热可得红褐色液体,此液体不具有的性质是_____
(2)①单质甲、乙和Y溶液中的阳离子氧化性由强到弱的顺序为:____________________ (用化学式表示)
②少量单质甲通入X溶液中发生的离子方程式为______________________________
(3)实验室制备、收集纯净干燥的甲单质,所需仪器如下,装置A为发生装置;除装置A中所需的药品外,其他装置中供选择的药品有:浓硫酸、碱石灰、五氧化二磷、饱和食盐水、氢氧化钠溶液。
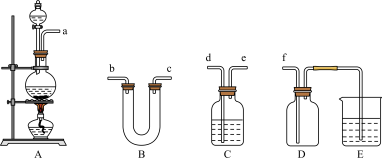
①装置A中发生反应的化学反应方程式:______________________
②按气流的方向连接各仪器接口,顺序为
a→_________ →_________ →_________ →_________ →f。
③指出装置B、C、E中的药品(从提供的药品中选择):
B:________________ C:___________________ E:__________________

请回答:
(1)将Y的饱和溶液滴入沸水中,继续加热可得红褐色液体,此液体不具有的性质是_____
| A.光束通过该液体时形成光亮的“通路” |
| B.插入电极通过直流电后,有一极附近液体颜色加深 |
| C.向该液体中加入硝酸银溶液,无沉淀产生 |
| D.将该液体加热蒸干、灼烧后,有氧化物生成 |
②少量单质甲通入X溶液中发生的离子方程式为
(3)实验室制备、收集纯净干燥的甲单质,所需仪器如下,装置A为发生装置;除装置A中所需的药品外,其他装置中供选择的药品有:浓硫酸、碱石灰、五氧化二磷、饱和食盐水、氢氧化钠溶液。

①装置A中发生反应的化学反应方程式:
②按气流的方向连接各仪器接口,顺序为
a→
③指出装置B、C、E中的药品(从提供的药品中选择):
B:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】下图所示的是一些常见单质、化合物之间的转化关系图,有些反应中的部分物质和反应条件被略去。已知X、Y、Z是日常生活中常见金属单质,X由地壳中含量最高的金属元素组成;D、E是常见气态非金属单质,其中D呈黄绿色。A的焰色反应呈紫色(透过蓝色钴玻璃),F的稀溶液呈蓝色。

请回答下列问题:
(1)C的电子式为________________ 。
(2)I露置于空气中,颜色由白色迅速变成灰绿色,最终变成红褐色,I的化学式为____ 。
(3)X与C溶液反应的离子方程式为___________ 。
(4)写出J与Y反应的化学方程式,并标出电子转移的方向和数目:___________ 。

请回答下列问题:
(1)C的电子式为
(2)I露置于空气中,颜色由白色迅速变成灰绿色,最终变成红褐色,I的化学式为
(3)X与C溶液反应的离子方程式为
(4)写出J与Y反应的化学方程式,并标出电子转移的方向和数目:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
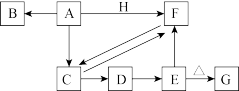
【推荐1】A~I分别表示中学化学中常见的一种物质,其中A、I为常见金属,它们之间的相互关系如图所示(部分反应物、生成物没有列出),且已知G为主族元素的固态氧化物,A、B、C、D、E、F六种物质中均含同一种元素。请填写下列空白:
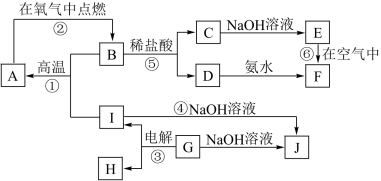
(1)A、B、C、D、E、F六种物质中所含同一种元素在周期表中的位置是________ 。
(2)写出C物质的化学式:________ 。
(3)写出①、⑥反应的化学方程式:
①:____________________________ 。
⑥:____________________________ 。
(4)从能量变化的角度看,反应①②③中,属于放热反应的是________ (填序号)。

(1)A、B、C、D、E、F六种物质中所含同一种元素在周期表中的位置是
(2)写出C物质的化学式:
(3)写出①、⑥反应的化学方程式:
①:
⑥:
(4)从能量变化的角度看,反应①②③中,属于放热反应的是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】已知A是一种常见金属,C是强碱,各物质有以下物质相互转化。试回答:
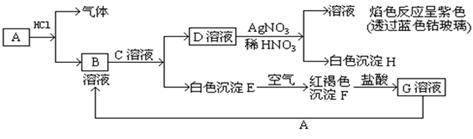
(1)写出A的化学式______ ,C的化学式______ 。
(2)写出由D转变成H的化学方程式______ 。
(3)写出向G溶液加入A的离子反应方程式______ 。

(1)写出A的化学式
(2)写出由D转变成H的化学方程式
(3)写出向G溶液加入A的离子反应方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】高铁酸钠(Na2FeO4)具有很强的氧化性,是高铁电池的重要原料,也是一种新型的绿色净水消毒剂。工业上可以通过次氯酸钠氧化法制备高铁酸钠,生产过程如下:

回答下列问题:
(1)Cl2与NaOH溶液反应的离子方程式是__________________ 。
(2)经过步骤①后,加入NaOH固体的原因是________________________ 。
(3)步骤②反应的离子方程式是_______________ 。
(4)从溶液I中分离出Na2FeO4后,还有副产品Na2SO4、NaCl,则步骤③中反应的离子方程式为_______________ 。
(5)Na2FeO4投入到污水中杀菌消毒,生成的Fe(OH)3可以起到絮凝剂的作用。通过计算得知Na2FeO4的消毒效率(以单位质量的消毒剂得到的电子数表示)比氯气的_________ (填“高”或“低”),用高铁酸钠代替氯气作净水消毒剂的优点是_________ (答出一点即可)。
(6)高铁电池的总反应为:3Zn+2K2FeO4+8H2O 3Zn(OH)2+2Fe(OH)3+4KOH放电时,负极的电极反应式是
3Zn(OH)2+2Fe(OH)3+4KOH放电时,负极的电极反应式是_____ 。正极附近溶液的碱性______ (填“增强”、“不变”或“减弱”)。

回答下列问题:
(1)Cl2与NaOH溶液反应的离子方程式是
(2)经过步骤①后,加入NaOH固体的原因是
(3)步骤②反应的离子方程式是
(4)从溶液I中分离出Na2FeO4后,还有副产品Na2SO4、NaCl,则步骤③中反应的离子方程式为
(5)Na2FeO4投入到污水中杀菌消毒,生成的Fe(OH)3可以起到絮凝剂的作用。通过计算得知Na2FeO4的消毒效率(以单位质量的消毒剂得到的电子数表示)比氯气的
(6)高铁电池的总反应为:3Zn+2K2FeO4+8H2O
 3Zn(OH)2+2Fe(OH)3+4KOH放电时,负极的电极反应式是
3Zn(OH)2+2Fe(OH)3+4KOH放电时,负极的电极反应式是
您最近一年使用:0次
【推荐1】铁是人类较早使用的金属之一,运用铁及其化合物的知识,完成下列问题。印刷电路板(PCB)是用腐蚀液(FeCl3溶液)将覆铜板上的部分铜腐蚀掉而制得。一种制作PCB 并将腐蚀后废液(其中金属阳离子主要含 Fe3+、Cu2+、Fe2+ )回收再生的流程如图。
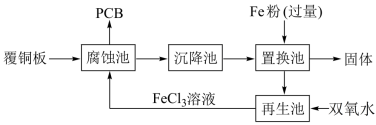
(1)腐蚀池中发生反应的化学方程式是_______ 。
(2)上述各池中,没有发生化学变化的是_______ 池。
(3)由置换池中得到固体的操作名称是_______ 。
(4)向再生池中通入Cl2也可以使废液再生,请写出通入氯气后再生池中发生的离子方程式:_______ 。相比Cl2,用双氧水的优点是_______ 。
(5)若取少量循环使用的氯化铁溶液于烧杯中,同时加入铁粉和铜粉。反应结束后,下列结果不可能出现的是_______。(填写编号)

(1)腐蚀池中发生反应的化学方程式是
(2)上述各池中,没有发生化学变化的是
(3)由置换池中得到固体的操作名称是
(4)向再生池中通入Cl2也可以使废液再生,请写出通入氯气后再生池中发生的离子方程式:
(5)若取少量循环使用的氯化铁溶液于烧杯中,同时加入铁粉和铜粉。反应结束后,下列结果不可能出现的是_______。(填写编号)
| A.有铜无铁 | B.有铁无铜 | C.铁、铜都有 | D.铁、铜都无 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】Ⅰ.除去下列物质中所混有的少量杂质,写出有关的反应方程式。
(1)铜粉中混有少量铝粉___________________________________________ ;
(2) FeCl3中混有少量FeCl2______________________________________________ ;
(3)Na2CO3固体中混有少量NaHCO3______________________________________ 。
Ⅱ.氯气溶于水发生反应,写出其化学方程式__________________________ 。某学生为了探究氯水的成分,请你与他一起完成探究过程,并书写实验报告。
(1)铜粉中混有少量铝粉
(2) FeCl3中混有少量FeCl2
(3)Na2CO3固体中混有少量NaHCO3
Ⅱ.氯气溶于水发生反应,写出其化学方程式
实验步骤 | 操作方法 | 实验现象 | 结论或解释 |
1 | 观察氯水的颜色 | 含有Cl2 | |
2 | 有无色气体产生 | 含有H+ | |
3 | 取少量氯水于试管中,加入稀硝酸酸化的硝酸银溶液 | 有白色沉淀生成 | |
4 | 取少量氯水于试管中,放入红色布条 |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】部分铁的化合物“价—类”二维关系如图所示。
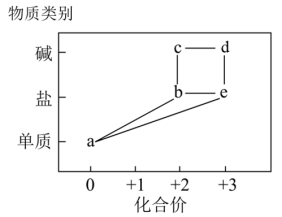
回答下列问题:
(1)c很不稳定,写出c露置在空气中被氧化的化学方程为:___________ ;观察到的现象为:___________ ;下图中___________ (填序号)能较长时间看到c。

(2)硫酸盐b的溶液中含少量硫酸盐e,除去杂质的方法是___________ 。
(3)若在b中加入盐酸,产生无色无味气体,将该气体通入澄清石灰水中,溶液变浑浊。如果在空气中高温灼烧b,可得到红色粉末,写出b在空气中灼烧的化学方程式:___________ 。
(4)工业上,常用一氧化碳在高温下与赤铁矿反应制备a,制备112kga时至少需要___________ LCO(标准状况),该反应中转移电子的物质的量是___________ 。

回答下列问题:
(1)c很不稳定,写出c露置在空气中被氧化的化学方程为:

(2)硫酸盐b的溶液中含少量硫酸盐e,除去杂质的方法是
(3)若在b中加入盐酸,产生无色无味气体,将该气体通入澄清石灰水中,溶液变浑浊。如果在空气中高温灼烧b,可得到红色粉末,写出b在空气中灼烧的化学方程式:
(4)工业上,常用一氧化碳在高温下与赤铁矿反应制备a,制备112kga时至少需要
您最近一年使用:0次