回答下列问题
(1)下面是石蜡油在炽热碎瓷片的作用下产生 并检验
并检验 性质的实验,完成下列各问题。
性质的实验,完成下列各问题。

①B中溶液褪色的原因是_______ 。
②在D处点燃时必须进行的操作是_______ 。
(2)实验室制取的乙烯中常混有少量的 ,有人设计如图实验装置以证明上述混合气体中含有乙烯和二氧化硫。试回答下列问题:
,有人设计如图实验装置以证明上述混合气体中含有乙烯和二氧化硫。试回答下列问题:
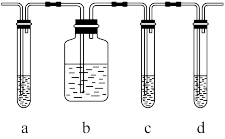
①图中a、b、c、d装置盛放的试剂依次是_______ (填序号)。
A.品红溶液 B.NaOH溶液 C.浓硫酸 D.酸性高锰酸钾溶液
②能说明 存在的实验现象是
存在的实验现象是_______ 。
③使用装置b的目的是_______ 。
④使用装置c的目的是_______ 。
⑤能证明混合气体中含有乙烯的现象是_______ 。
(1)下面是石蜡油在炽热碎瓷片的作用下产生
 并检验
并检验 性质的实验,完成下列各问题。
性质的实验,完成下列各问题。
①B中溶液褪色的原因是
②在D处点燃时必须进行的操作是
(2)实验室制取的乙烯中常混有少量的
 ,有人设计如图实验装置以证明上述混合气体中含有乙烯和二氧化硫。试回答下列问题:
,有人设计如图实验装置以证明上述混合气体中含有乙烯和二氧化硫。试回答下列问题:
①图中a、b、c、d装置盛放的试剂依次是
A.品红溶液 B.NaOH溶液 C.浓硫酸 D.酸性高锰酸钾溶液
②能说明
 存在的实验现象是
存在的实验现象是③使用装置b的目的是
④使用装置c的目的是
⑤能证明混合气体中含有乙烯的现象是
更新时间:2022-07-14 23:21:55
|
相似题推荐
解答题-实验探究题
|
较易
(0.85)
【推荐1】某化学兴趣小组为制备并探究 的性质,按如图所示装置进行实验。
的性质,按如图所示装置进行实验。

已知: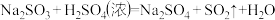
(1)装置A中盛放浓硫酸的仪器名称是_______ 。
(2)装置B中发生反应后溶液的酸性将_______ 。(填“增强”“不变”或“减弱”)
(3)装置C中现象为_______ ;装置D中发生反应的化学方程式为_______ 。
(4)装置E的目的是探究 与品红作用的可逆性,请写出实验操作及现象:
与品红作用的可逆性,请写出实验操作及现象:_______ 。
(5)装置F中发生反应的离子方程式为_______ 。
(6)装置A与装置G相比,其优点是_______ (任写一点)。
 的性质,按如图所示装置进行实验。
的性质,按如图所示装置进行实验。
已知:
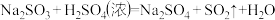
(1)装置A中盛放浓硫酸的仪器名称是
(2)装置B中发生反应后溶液的酸性将
(3)装置C中现象为
(4)装置E的目的是探究
 与品红作用的可逆性,请写出实验操作及现象:
与品红作用的可逆性,请写出实验操作及现象:(5)装置F中发生反应的离子方程式为
(6)装置A与装置G相比,其优点是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐2】硫代硫酸钠(Na2S2O3),又名大苏打,易溶于水,易被氧化,遇酸易分解;其工业制备原理为2Na2S+Na2CO3+4SO2==3Na2S2O3+CO2,用途广泛,其中之一为处理含氰化钠的废水。实验室通过如下图所示装置制备Na2S2O3。
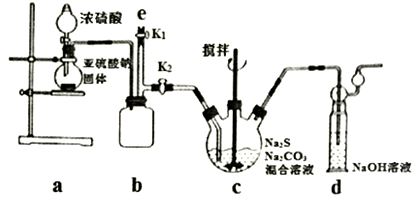
(1)实验中生成SO2的化学方程式_________________________________ 。
(2)b装置的作用是___________________ 。
(3)反应开始后,c中观察到逐渐析出了淡黄色固体,后又消失的现象,请用离子方程式解释淡黄色固体出现的原因______________________________________ 。
(4)实验结束后,在e处最好连接盛_________ 的仪器,目的是___________________ 。
(5)为了提高产品的产量,通入的SO2不能过量,原因是___________________ 。
(6)测定用硫代硫酸钠溶液处理后的废水中氰化钠的含量。
已知:①废水中氰化钠的最高排放标准为0.50 mg/L;
②Ag++2CN-=[Ag(CN)2]-,Ag++I-=AgI↓,AgI呈黄色,且CN-优先与Ag+反应。
实验如下:取20.00 mL处理后的氰化钠废水于锥形瓶中,并滴加几滴KI溶液作指示剂,用1.00×10-4mol/L的标准六AgNO3溶液滴定,消耗AgNO3溶液的体积为1.50mL。
滴定终点的现象:_____________________ ;处理后的废水是否达到排放标准:____________ (填“是”或“否”)。

(1)实验中生成SO2的化学方程式
(2)b装置的作用是
(3)反应开始后,c中观察到逐渐析出了淡黄色固体,后又消失的现象,请用离子方程式解释淡黄色固体出现的原因
(4)实验结束后,在e处最好连接盛
(5)为了提高产品的产量,通入的SO2不能过量,原因是
(6)测定用硫代硫酸钠溶液处理后的废水中氰化钠的含量。
已知:①废水中氰化钠的最高排放标准为0.50 mg/L;
②Ag++2CN-=[Ag(CN)2]-,Ag++I-=AgI↓,AgI呈黄色,且CN-优先与Ag+反应。
实验如下:取20.00 mL处理后的氰化钠废水于锥形瓶中,并滴加几滴KI溶液作指示剂,用1.00×10-4mol/L的标准六AgNO3溶液滴定,消耗AgNO3溶液的体积为1.50mL。
滴定终点的现象:
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐3】某化学兴趣小组为探究SO2的性质,按如图所示装置进行实验。

已知: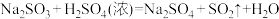 ;请回答下列问题:
;请回答下列问题:
(1)装置A中盛放浓硫酸的仪器名称是___________ 。
(2)反应后,装置B中产生的现象是___________ ,发生反应的离子方程式为___________ 。
(3)装置C中的现象是___________ ,表现了SO2的___________ (填选项字母);装置D中的现象是___________ ,表现了SO2的___________ 。(同上)
A、漂白性 B、氧化性 C、还原性 D、酸性

已知:
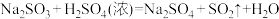 ;请回答下列问题:
;请回答下列问题:(1)装置A中盛放浓硫酸的仪器名称是
(2)反应后,装置B中产生的现象是
(3)装置C中的现象是
A、漂白性 B、氧化性 C、还原性 D、酸性
您最近一年使用:0次
解答题-有机推断题
|
较易
(0.85)
名校
【推荐1】我国科学家成功实现甲烷在催化剂及无氧条件下,一步高效生产乙烯、芳烃等化学品,为天然气化工开发了一项革命性技术。以甲烷为原料合成部分化工产品流程如下(部分反应条件已略去):

(1)乙醇分子中所含官能团的名称:________ 。
(2)反应②的反应类型是:________ 。
(3)反应⑥在生成溴苯的同时生成另一物质,该物质的化学式为________ 。
(4)为除去乙酸乙酯产品中混有的少量乙酸,实验室可采取的操作:向装有乙酸乙酯产品的分液漏斗中加入一定量________ (试剂名称),充分振荡、________ 、分液,并重复多次。
(5)CH4有多种同系物,其中________ (填分子式)有两种同分异构体。

(1)乙醇分子中所含官能团的名称:
(2)反应②的反应类型是:
(3)反应⑥在生成溴苯的同时生成另一物质,该物质的化学式为
(4)为除去乙酸乙酯产品中混有的少量乙酸,实验室可采取的操作:向装有乙酸乙酯产品的分液漏斗中加入一定量
(5)CH4有多种同系物,其中
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐2】A、B、C、D四种有机物的有关信息如下:
A:①能使溴的四氯化碳溶液褪色;②比例模型为 ;③能与水在一定条件下反应生成C。
;③能与水在一定条件下反应生成C。
B:①由碳、氢两种元素组成;②球棍模型为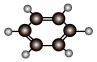 ;
;
C:①由碳、氢、氧三种元素组成;②能与Na反应,但不能与NaOH溶液反应;③能与D反应生成相对分子质量为88的酯。
D:①由碳、氢、氧三种元素组成;②球棍模型为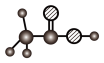 。
。
(1)A的分子式为___________ ,与溴的四氯化碳溶液反应的化学方程式为___________ 。
(2)B所具有的性质是__________ (填序号)。
①无色无味液体;②有毒;③不溶于水;④密度比水大;⑤与酸性高锰酸钾溶液和溴水反应褪色;⑥任何条件下不与氢气反应。
写出在浓硫酸作用下,B与浓硝酸反应的化学方程式_________________________ 。
(3)C所含的官能团的名称为______________ 。C与D反应能生成相对分子质量为88的酯,该反应的反应类型为______________ ,其化学方程式为______________ .
A:①能使溴的四氯化碳溶液褪色;②比例模型为
 ;③能与水在一定条件下反应生成C。
;③能与水在一定条件下反应生成C。B:①由碳、氢两种元素组成;②球棍模型为
 ;
;C:①由碳、氢、氧三种元素组成;②能与Na反应,但不能与NaOH溶液反应;③能与D反应生成相对分子质量为88的酯。
D:①由碳、氢、氧三种元素组成;②球棍模型为
 。
。(1)A的分子式为
(2)B所具有的性质是
①无色无味液体;②有毒;③不溶于水;④密度比水大;⑤与酸性高锰酸钾溶液和溴水反应褪色;⑥任何条件下不与氢气反应。
写出在浓硫酸作用下,B与浓硝酸反应的化学方程式
(3)C所含的官能团的名称为
您最近一年使用:0次
解答题-有机推断题
|
较易
(0.85)
【推荐3】从石油和煤中可以提炼出化工原料A和B,A是一种果实催熟剂,它的产量用来 衡量一个国家的石油化工发展水平。B是一种比水轻的油状液体,仅由碳氢两种元素组成,碳元素与氢元素的质量比为12:1,B的相对分子质量为78。回答下列问题:
(1)A的结构简式:________ ;
(2)A使溴的四氯化碳溶液褪色的化学反应方程式:___________ ;
(3)在碘水中加入B振荡静置后的现象:_______________ ,该操作叫______________ ;
(4)B与浓硫酸和浓硝酸在50~60℃反应的化学反应方程式:_________ ;
反应类型为:_________________ ;
(5)等质量的A、B完全燃烧时消耗O2的物质的量________ (填“A>B”、“A<B”或“A=B”)。
(1)A的结构简式:
(2)A使溴的四氯化碳溶液褪色的化学反应方程式:
(3)在碘水中加入B振荡静置后的现象:
(4)B与浓硫酸和浓硝酸在50~60℃反应的化学反应方程式:
反应类型为:
(5)等质量的A、B完全燃烧时消耗O2的物质的量
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐1】某同学设计实验探究工业制乙烯的原理和乙烯的主要化学性质,装置如图所示。回答下列问题。
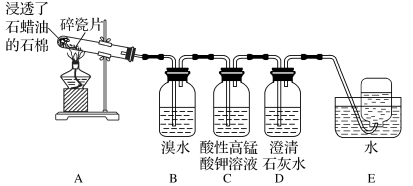
(1)装置A模拟工业制备乙烯的过程,该过程的名称为_____ 。
(2)装置B中的实验现象为_____ ,反应方程式为_____ 。
(3)装置C的反应类型为_____ ,装置D中出现_____ 的现象也可证明C中反应发生。
(4)为探究溴与乙烯反应是加成反应而不是取代反应,可选择的实验操作有_____ 。
(5)实验室制备的乙烯直接通入酸性KMnO4中不能证明有乙烯生成的原因为_____ 。

(1)装置A模拟工业制备乙烯的过程,该过程的名称为
(2)装置B中的实验现象为
(3)装置C的反应类型为
(4)为探究溴与乙烯反应是加成反应而不是取代反应,可选择的实验操作有
(5)实验室制备的乙烯直接通入酸性KMnO4中不能证明有乙烯生成的原因为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐2】甲、乙两化学实验小组进行实验室制取乙烯并验证乙烯性质的实验。
(1)甲组用如图装置进行实验。当温度迅速上升后,可观察到试管中的浓溴水褪色,烧瓶中浓硫酸与乙醇的混合液变为棕黑色。请回答下列问题:
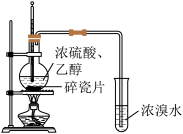
①该实验中生成乙烯的化学方程式为___________ 。
②一些同学认为,溴水褪色的现象不能证明反应中有乙烯生成及乙烯具有不饱和性,因为棕黑色物质与浓硫酸反应可能生成某种能使溴水褪色的气体。该气体使溴水褪色的化学方程式为___________ ;
③还有同学提出通过测定反应后溶液的pH可探究乙烯与溴水发生的反应是加成反应还是取代反应,原因是___________ 。
(2)乙组用如图装置进行实验。请回答下列问题:
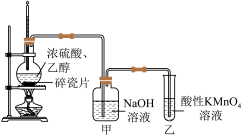
①烧瓶中碎瓷片的作用是___________ 。
②能够说明乙烯具有还原性的现象是___________ ;装置甲的作用是___________ ;若无甲装置,是否也能检验乙烯具有还原性,简述其理由:___________ 。
(1)甲组用如图装置进行实验。当温度迅速上升后,可观察到试管中的浓溴水褪色,烧瓶中浓硫酸与乙醇的混合液变为棕黑色。请回答下列问题:

①该实验中生成乙烯的化学方程式为
②一些同学认为,溴水褪色的现象不能证明反应中有乙烯生成及乙烯具有不饱和性,因为棕黑色物质与浓硫酸反应可能生成某种能使溴水褪色的气体。该气体使溴水褪色的化学方程式为
③还有同学提出通过测定反应后溶液的pH可探究乙烯与溴水发生的反应是加成反应还是取代反应,原因是
(2)乙组用如图装置进行实验。请回答下列问题:

①烧瓶中碎瓷片的作用是
②能够说明乙烯具有还原性的现象是
您最近一年使用:0次
解答题-有机推断题
|
较易
(0.85)
名校
【推荐3】以石油、煤为原料可获得多种有机物。A能发生银镜反应,CH2=CH2生成C的原子利用率为100%,D与乙醇互为同系物,B和E属于同一类别的有机物。它们之间的转化关系如图(含有相同官能团的有机物通常具有相似的化学性质):

请回答:
(1)化合物A中官能团的名称是_______ 。
(2)C+D→E的化学方程式是_______ 。
(3)下列说法不正确的是_______ 。
A.化合物B是一种具有浓郁香味、不易溶于水的油状液体
B.可用新制Cu(OH)2悬浊液鉴别A、B、C
C.从石油中获得CH2=CH2的方法是裂化
D.相同质量的A和B充分燃烧时消耗O2的量相同

请回答:
(1)化合物A中官能团的名称是
(2)C+D→E的化学方程式是
(3)下列说法不正确的是
A.化合物B是一种具有浓郁香味、不易溶于水的油状液体
B.可用新制Cu(OH)2悬浊液鉴别A、B、C
C.从石油中获得CH2=CH2的方法是裂化
D.相同质量的A和B充分燃烧时消耗O2的量相同
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐1】海洋是巨大的资源宝库,可以提取到我们需要的食盐、溴和碘。
I.从海水中提取食盐和溴的过程如下:
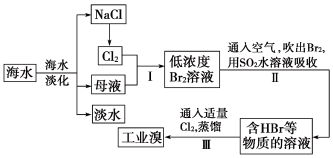
(1)步骤I中已获得Br2,步骤Ⅱ中又将Br2还原为Br-,其目的为:_______ 。
(2)步骤Ⅱ用SO2水溶液吸收Br2,吸收率可达95%,有关反应的化学方程式为:_______ 。
Ⅱ.实验:探究硫酸浓度对化学反应速率的影响
常温下,酸性KI溶液在空气中会被氧化为碘单质,现取三支试管,先向其中各加入1mL相同浓度的KI溶液(含指示剂),再分别加入2 mol∙L−1的硫酸和一定量蒸馏水,其显色时间如下表所示:
(3)V2=_______ mL。通过实验Ⅰ、Ⅱ,本小组得出的实验结论为_______ 。
Ⅲ.如图石蜡油在炽热碎瓷片的作用下产生C2H4并检验C2H4性质的实验,完成下列各问题。
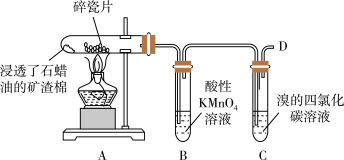
(4)B中溶液褪色,是因为乙烯被_______ 。
(5)C中溶液褪色,发生反应的化学方程式为_______ 。
(6)在D处点燃前必须进行的操作是_______ 。
I.从海水中提取食盐和溴的过程如下:

(1)步骤I中已获得Br2,步骤Ⅱ中又将Br2还原为Br-,其目的为:
(2)步骤Ⅱ用SO2水溶液吸收Br2,吸收率可达95%,有关反应的化学方程式为:
Ⅱ.实验:探究硫酸浓度对化学反应速率的影响
常温下,酸性KI溶液在空气中会被氧化为碘单质,现取三支试管,先向其中各加入1mL相同浓度的KI溶液(含指示剂),再分别加入2 mol∙L−1的硫酸和一定量蒸馏水,其显色时间如下表所示:
组别 | 硫酸/mL | 蒸馏水/mL | 显色时间/s |
i | 3 | 0 | 120 |
ii | 2 | V1 | 140 |
iii | 1 | V2 | 200 |
Ⅲ.如图石蜡油在炽热碎瓷片的作用下产生C2H4并检验C2H4性质的实验,完成下列各问题。

(4)B中溶液褪色,是因为乙烯被
(5)C中溶液褪色,发生反应的化学方程式为
(6)在D处点燃前必须进行的操作是
您最近一年使用:0次
解答题-有机推断题
|
较易
(0.85)
解题方法
【推荐2】以石蜡油为原料,有机物A、B、C、D的转化关系如图,气态烃A的密度为1.25g•L-1(标准状况下),C可以和碳酸氢钠溶液反应,D具有果香气味

(1)石蜡油成分中含有的主要元素有_______ 。
(2)A的结构简式为_______ ,B中所含官能团的名称是_______ 。
(3)B+C→D的化学方程式为_______ ,反应类型为_______ 。
(4)实验室中制取D的装置如图所示。
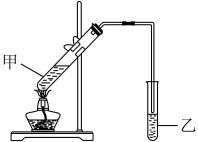
①乙试管中的溶液最合理的是_______ 。
A.饱和氯化钠溶液 B.饱和碳酸钠溶液 C.氢氧化钠溶液 D.水
②乙试管中的玻璃导管不能伸入液面下的目的是_______ ,从试管乙中分离出D的试验方法是_______ 。

(1)石蜡油成分中含有的主要元素有
(2)A的结构简式为
(3)B+C→D的化学方程式为
(4)实验室中制取D的装置如图所示。

①乙试管中的溶液最合理的是
A.饱和氯化钠溶液 B.饱和碳酸钠溶液 C.氢氧化钠溶液 D.水
②乙试管中的玻璃导管不能伸入液面下的目的是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐3】如图所示为实验室模拟工业上催化裂化的装置示意图,根据图示回答下列问题。
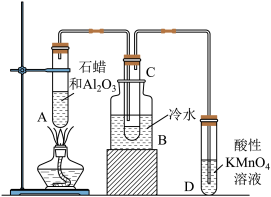
(1)工业上石油裂化的主要目的是_______________________ 。
(2)A中氧化铝的作用是_____________ ,B中冷水的作用是___________________ 。
(3)C中得到的液体具有汽油的气味,该液体________________ (填“能”或“不能”,下同)通过化学反应使溴水褪色,而通过石油分馏得到的汽油_______________ 通过化学反应使溴水褪色。
(4)D中酸性高锰酸钾溶液褪色,说明石蜡裂化时除有液态不饱和烃生成外,还有__________ 生成。

(1)工业上石油裂化的主要目的是
(2)A中氧化铝的作用是
(3)C中得到的液体具有汽油的气味,该液体
(4)D中酸性高锰酸钾溶液褪色,说明石蜡裂化时除有液态不饱和烃生成外,还有
您最近一年使用:0次



