某学习小组设计如下实验方案,探究25℃时酸性高锰酸钾溶液与 溶液反应时,影响反应速率的因素:
溶液反应时,影响反应速率的因素:
已知: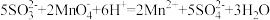 。
。
(1)通过测定混合溶液完全褪色所用的时间计算反应速率的大小,已知实验1混合溶液褪色所用的时间是2min,则实验1从反应开始到反应结束这段时间内反应速率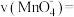
____  。
。
(2)实验2和实验3的目的是____ ;实验测得实验2的反应速率大于实验1,结论是______ 。
(3)a=_______ ,实验测得实验4的反应速率明显大于实验1,某同学在一定温度下进行酸性 溶液与
溶液与 溶液的反应时,发现刚开始一段时间,反应速率较慢,后来反应速率明显加快,该实验中反应速率明显加快的原因可能是
溶液的反应时,发现刚开始一段时间,反应速率较慢,后来反应速率明显加快,该实验中反应速率明显加快的原因可能是_______ 。
 溶液反应时,影响反应速率的因素:
溶液反应时,影响反应速率的因素:| 编号 | 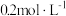 的 的 溶液/mL 溶液/mL |  的 的 溶液/ mL 溶液/ mL |  的 的 溶液/ mL 溶液/ mL |  的 的 溶液/ mL 溶液/ mL | 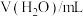 |
| 1 | 3.0 | 2.0 | 1.0 | 0 | 2.0 |
| 2 | 3.0 | 2.0 | 2.0 | 0 | 1.0 |
| 3 | 4.0 | 2.0 | 2.0 | 0 | 0 |
| 4 | 3.0 | 2.0 | 1.0 | 0.5 | a |
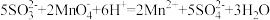 。
。(1)通过测定混合溶液完全褪色所用的时间计算反应速率的大小,已知实验1混合溶液褪色所用的时间是2min,则实验1从反应开始到反应结束这段时间内反应速率
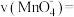
 。
。(2)实验2和实验3的目的是
(3)a=
 溶液与
溶液与 溶液的反应时,发现刚开始一段时间,反应速率较慢,后来反应速率明显加快,该实验中反应速率明显加快的原因可能是
溶液的反应时,发现刚开始一段时间,反应速率较慢,后来反应速率明显加快,该实验中反应速率明显加快的原因可能是
20-21高一下·黑龙江鸡西·期末 查看更多[4]
更新时间:2022-07-02 06:53:28
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】工业产生的废气COx、NOx、SOx对环境有害,若能合理的利用吸收,可以减少污染,变废为宝。根据题干相关信息完成(1)—(4)小题。
某研究小组利用反应: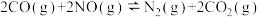 实现气体的无害化排放。
实现气体的无害化排放。 ℃时,在恒容的密闭容器中通入一定量的CO和NO、能自发进行上述反应,测得不同时间的CO和NO的浓度如下表。
℃时,在恒容的密闭容器中通入一定量的CO和NO、能自发进行上述反应,测得不同时间的CO和NO的浓度如下表。
(1)0~2s内用N2表示的化学反应速率为___________ 。该温度下,反应的平衡常数
___________ 。
(2)若该反应在绝热恒容条件下进行,则反应达到平衡后体系的温度为 ℃,根据该反应的特点判断,下列说法正确的是___________。
℃,根据该反应的特点判断,下列说法正确的是___________。
(3)向甲、乙两个容积均为1L的恒温恒容的密闭容器中,分别充入一定量的:SO2和O2,甲充入2molSO2、1molO2,乙充入1molSO2、0.5molO2,容器中均发生如下反应: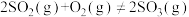
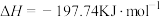 ,一段时间后达到平衡,测得两容器中
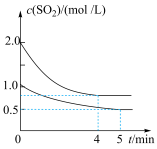
,一段时间后达到平衡,测得两容器中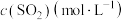 随时间t(min)的变化关系如图所示。下列说法
随时间t(min)的变化关系如图所示。下列说法正确 的是___________。
(4)CO2在自然界循环时可与CaCO3反应,CaCO3是一种难溶物质,其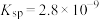 ,CaCl2溶液与Na2CO3溶液混合可形成CaCO3沉淀,现将等体积的CaCl2溶液与Na2CO3溶液混合,若使用的Na2CO3溶液的浓度为
,CaCl2溶液与Na2CO3溶液混合可形成CaCO3沉淀,现将等体积的CaCl2溶液与Na2CO3溶液混合,若使用的Na2CO3溶液的浓度为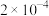 mol/L,则生成沉淀所需CaCl2溶液混合前的最小浓度为
mol/L,则生成沉淀所需CaCl2溶液混合前的最小浓度为___________ 。
某研究小组利用反应:
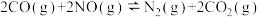 实现气体的无害化排放。
实现气体的无害化排放。 ℃时,在恒容的密闭容器中通入一定量的CO和NO、能自发进行上述反应,测得不同时间的CO和NO的浓度如下表。
℃时,在恒容的密闭容器中通入一定量的CO和NO、能自发进行上述反应,测得不同时间的CO和NO的浓度如下表。| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
 | 3.60 | 3.05 | 2.85 | 2.75 | 2.70 | 2.70 |
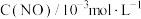 | 1.00 | 0.45 | 0.25 | 0.15 | 0.10 | 0.10 |
(1)0~2s内用N2表示的化学反应速率为

(2)若该反应在绝热恒容条件下进行,则反应达到平衡后体系的温度为
 ℃,根据该反应的特点判断,下列说法正确的是___________。
℃,根据该反应的特点判断,下列说法正确的是___________。A.  | B.  |
C.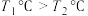 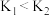 | D.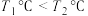 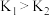 |
(3)向甲、乙两个容积均为1L的恒温恒容的密闭容器中,分别充入一定量的:SO2和O2,甲充入2molSO2、1molO2,乙充入1molSO2、0.5molO2,容器中均发生如下反应:
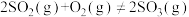
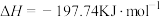 ,一段时间后达到平衡,测得两容器中
,一段时间后达到平衡,测得两容器中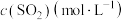 随时间t(min)的变化关系如图所示。下列说法
随时间t(min)的变化关系如图所示。下列说法
A.放出的热量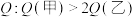 |
B.体系总压强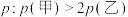 |
| C.甲容器达到化学平衡时,其化学平衡常数为4 |
D.保持其他条件不变,若起始时向乙中充入0.4molSO2、0.2molO2、0.4molSO3,则此时 |
(4)CO2在自然界循环时可与CaCO3反应,CaCO3是一种难溶物质,其
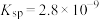 ,CaCl2溶液与Na2CO3溶液混合可形成CaCO3沉淀,现将等体积的CaCl2溶液与Na2CO3溶液混合,若使用的Na2CO3溶液的浓度为
,CaCl2溶液与Na2CO3溶液混合可形成CaCO3沉淀,现将等体积的CaCl2溶液与Na2CO3溶液混合,若使用的Na2CO3溶液的浓度为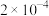 mol/L,则生成沉淀所需CaCl2溶液混合前的最小浓度为
mol/L,则生成沉淀所需CaCl2溶液混合前的最小浓度为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】某温度下,在一个 2L 的密闭容器中,X、Y、Z 三种物质的物质的量随时间的变化曲线如图所示。根据图中数据,填写下列空白:
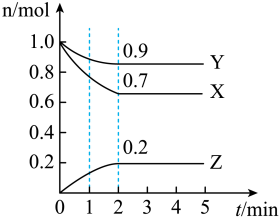
(1)从开始至 2min,Y 的平均反应速率为____ 。
(2)该反应的化学方程式为____ 。
(3)1min 时,ν(逆)____ ν(正),3min 时,ν(正)____ ν(逆) (填“大于”或“小于”或“等于”) 。
(4)上述反应在甲、乙两个相同容器内同时进行,分别测得甲中 v(X)=9mol•L-1min-1,乙中 v(Y)=0.5mol•L-1s-1,则____ 中反应更快。
(5) 若 X、Y、Z 均为气体(容器体积不变),下列能说明反应已达平衡的是____ 。
a.X、Y、Z 三种气体的浓度不再改变
b.气体混合物物质的量不再改变
c.反应已经停止
d.反应速率 v(X)∶v(Y)=3∶1
e.单位时间内消耗 X 的物质的量∶单位时间内消耗 Z 的物质的量=3∶2
f.混合气体的密度不随时间变化

(1)从开始至 2min,Y 的平均反应速率为
(2)该反应的化学方程式为
(3)1min 时,ν(逆)
(4)上述反应在甲、乙两个相同容器内同时进行,分别测得甲中 v(X)=9mol•L-1min-1,乙中 v(Y)=0.5mol•L-1s-1,则
(5) 若 X、Y、Z 均为气体(容器体积不变),下列能说明反应已达平衡的是
a.X、Y、Z 三种气体的浓度不再改变
b.气体混合物物质的量不再改变
c.反应已经停止
d.反应速率 v(X)∶v(Y)=3∶1
e.单位时间内消耗 X 的物质的量∶单位时间内消耗 Z 的物质的量=3∶2
f.混合气体的密度不随时间变化
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】在4L恒容密闭容器中投入2mol N2和5mol H2发生合成氨反应:N2(g)+3H2(g) 2NH3(g)放热(
2NH3(g)放热(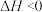 )
)
(1)在一定条件下,合成氨反应一段时间后,下列可能的是___________。
(2)若在某条件下合成氨反应2min后,H2变为0.8mol·L-1,则这2min内的化学反应速率为v(NH3)=___________ 。
(3)下列能说明合成氨反应达到化学平衡的是___________ 。
①气体密度不变
②每生成3mol H2,同时就生成1mol N2
③气体总压强不变
④每断裂1根H-H键,同时断裂2根N-H键
⑤氨气的体积分数不变
⑥N2和NH3的分子数为1:2
(4)若恒容通入He气使容器内压强增大,则合成氨的化学反应速率___________ (填:增大、减小、不变,不确定)。
(5)如图为合成氨反应速率(ν)与时间(t)关系的示意图,由图判断,在t1时刻曲线发生变化的原因可能是___________ 。升温,氨气的平衡浓度___________ (填:增大、减小、不变,不确定)。

(6)合成氨反应达到化学平衡后,压缩容器体积,v正、v逆的变化倍数谁更大?___________ (填:v正、v逆、一样大、不确定)。若恒压通入He气,则氢气的平衡转化率___________ (填:增大、减小、不变,不确定)。
 2NH3(g)放热(
2NH3(g)放热(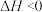 )
)(1)在一定条件下,合成氨反应一段时间后,下列可能的是___________。
| A.0.3mol N2 | B.1.0mol H2 |
| C.3.6mol NH3 | D.7mol气体 |
(3)下列能说明合成氨反应达到化学平衡的是
①气体密度不变
②每生成3mol H2,同时就生成1mol N2
③气体总压强不变
④每断裂1根H-H键,同时断裂2根N-H键
⑤氨气的体积分数不变
⑥N2和NH3的分子数为1:2
(4)若恒容通入He气使容器内压强增大,则合成氨的化学反应速率
(5)如图为合成氨反应速率(ν)与时间(t)关系的示意图,由图判断,在t1时刻曲线发生变化的原因可能是

(6)合成氨反应达到化学平衡后,压缩容器体积,v正、v逆的变化倍数谁更大?
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】已知MnO2、Fe3+、Cu2+等均可以催化过氧化氢的分解。某化学实验小组为确定过氧化氢分解的最佳催化条件,用如图装置进行实验,反应物用量和反应停止的时间数据如下表:
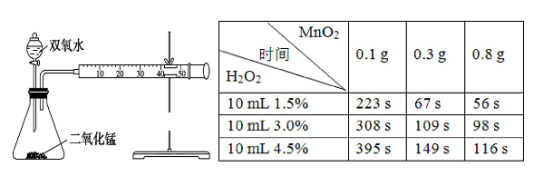
请回答下列问题:
(1)盛装双氧水的化学仪器名称是__________ 。
(2)如何检验该套装置的气密性__________________________________________________ 。
(3)相同浓度的过氧化氢,其分解速率随着二氧化锰用量的增加而__________ 。
(4)从实验效果和“绿色化学”角度考虑,双氧水的浓度相同时,加入______ g的二氧化锰为较佳选择。
(5)某同学查阅资料知道,H2O2是一种常见的氧化剂,可以将Fe2+氧化为Fe3+,他在FeCl2溶液中加入过氧化氢溶液,发现溶液由浅绿色变成了棕黄色,过了一会,又产生了气体,猜测该气体可能为______ ,产生该气体的原因是_____________________ 。

请回答下列问题:
(1)盛装双氧水的化学仪器名称是
(2)如何检验该套装置的气密性
(3)相同浓度的过氧化氢,其分解速率随着二氧化锰用量的增加而
(4)从实验效果和“绿色化学”角度考虑,双氧水的浓度相同时,加入
(5)某同学查阅资料知道,H2O2是一种常见的氧化剂,可以将Fe2+氧化为Fe3+,他在FeCl2溶液中加入过氧化氢溶液,发现溶液由浅绿色变成了棕黄色,过了一会,又产生了气体,猜测该气体可能为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】如图是研究催化剂对过氧化氢分解反应速率影响的实验装置图。某学生研究小组在50mL量筒中盛满水,倒置于水槽中,通过分液漏斗把过氧化氢溶液加入锥形瓶中(瓶中已有适量催化剂),记录各时间段收集到的氧气的体积。
实验一:以二氧化锰作催化剂,进行以下四组实验。
第1组:粉末状的二氧化锰0.2g+5mL6%H2O2
第2组:粉末状的二氧化锰0.2g+5mL10%H2O2
第3组:粉末状的二氧化锰0.1g+5mL6%H2O2
第4组:颗粒状的二氧化锰0.1g+5mL6%H2O2
实验二:以不同的催化剂对过氧化氢(均为5mL6%H2O2)分解反应速率影响进行研究,记录反应的时间t和相应的量筒内的气体体积读数V,用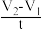 t作为反应速率的表达式(单位:mL•s﹣1),得到以下实验数据:
t作为反应速率的表达式(单位:mL•s﹣1),得到以下实验数据:
(1)写出实验一中H2O2分解的反应方程式_________ 。
(2)实验一的几组数据能够说明在实验中影响反应速率的因素主要有_________ 。
(3)实验二的几组数据反映出的问题是_________ 。
(4)用碰撞理论解释使用正催化剂能增大化学反应速率的原因_________ 。
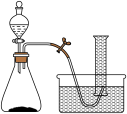
实验一:以二氧化锰作催化剂,进行以下四组实验。
第1组:粉末状的二氧化锰0.2g+5mL6%H2O2
第2组:粉末状的二氧化锰0.2g+5mL10%H2O2
第3组:粉末状的二氧化锰0.1g+5mL6%H2O2
第4组:颗粒状的二氧化锰0.1g+5mL6%H2O2
| 催化剂:MnO2 | 0.2g粉末状的MnO2+5mL6%H2O2 | 0.2g粉末状的MnO2+5mL10%H2O2 | 0.1g粉末状的MnO2+5mL6%H2O2 | 0.1g颗粒状的MnO2+5mL6%H2O2 |
| 前15s产生O2(mL) | 11 | 15 | 8 | 7 |
| 前30s产生O2(mL) | 21 | 24 | 11 | 9 |
| 前45s产生O2(mL) | 31 | 35 | 18 | 12 |
| 前60s产生O2(mL) | 45 | 48 | 26 | 15 |
实验二:以不同的催化剂对过氧化氢(均为5mL6%H2O2)分解反应速率影响进行研究,记录反应的时间t和相应的量筒内的气体体积读数V,用
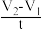 t作为反应速率的表达式(单位:mL•s﹣1),得到以下实验数据:
t作为反应速率的表达式(单位:mL•s﹣1),得到以下实验数据:| 催化剂 | 产生气体速率/mL•s﹣1 | 催化剂 | 产生气体速率/mL•s﹣1 |
| MnO2 | 0.03 | 土豆 | 0.03 |
| CuO | 0.07 | 活性炭 | 0.12 |
(1)写出实验一中H2O2分解的反应方程式
(2)实验一的几组数据能够说明在实验中影响反应速率的因素主要有
(3)实验二的几组数据反映出的问题是
(4)用碰撞理论解释使用正催化剂能增大化学反应速率的原因

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】控制变量法是化学探究的重要方法,明明同学利用 稀硫酸与铁反应,探究响化学反应速率的因素时得到如下实验数据:
稀硫酸与铁反应,探究响化学反应速率的因素时得到如下实验数据:
分析上述数据,回答下列问题:
(1)实验1和2表明,影响反应速率因素是_______ 。表中x=_______ 判断依据为_______ 。
(2)表明反应物浓度对化学反应速率影响的实验组是_______ (填实验序号)。
(3)本实验中影响反应速率的因素还有_______ 。
(4)实验3中若在铁片上放一只碳棒,金属消失的时间会远小于125s,其原因是_______ 。
 稀硫酸与铁反应,探究响化学反应速率的因素时得到如下实验数据:
稀硫酸与铁反应,探究响化学反应速率的因素时得到如下实验数据:| 实验序号 | 铁的质量/g | 铁的形状 | 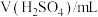 | 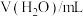 | 初始溶液的温度/℃ | 金属消失的时间/s |
| 1 | 0.10 | 铁片 | 40 | 10 | 20 | 200 |
| 2 | 0.10 | 铁粉 | 40 | x | 20 | 25 |
| 3 | 0.10 | 铁片 | 50 | 0 | 20 | 125 |
| 4 | 0.10 | 铁片 | 50 | 0 | 35 | 50 |
(1)实验1和2表明,影响反应速率因素是
(2)表明反应物浓度对化学反应速率影响的实验组是
(3)本实验中影响反应速率的因素还有
(4)实验3中若在铁片上放一只碳棒,金属消失的时间会远小于125s,其原因是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】某研究性学习小组欲探究影响锌和稀硫酸反应速率的外界条件,设计如下实验:
(1)上述实验中,反应速率最快的是实验___________ (填序号)。
(2)实验2和3表明,___________ 对反应速率有影响。
(3)进行实验2时,小组同学根据实验过程绘制的气体体积(标准状况下)与时间的图象如图所示。
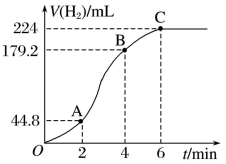
①在OA、AB、BC三段中,反应速率最快的是___________ 段,原因是___________ 。
②2~4min内以硫酸的浓度变化表示的平均反应速率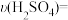
___________  (假设溶液的体积不变)。
(假设溶液的体积不变)。
(4)实验过程中,小组同学发现实验4的速率明显大于实验3的速率,原因是___________ 。
| 实验序号 | 锌的质量/g | 锌的状态 | 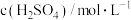 | 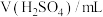 | 反应前溶液的温度/℃ | 添加剂 |
| 1 | 0.65 | 颗粒 | 0.5 | 50 | 20 | 无 |
| 2 | 0.65 | 粉末 | 0.5 | 50 | 20 | 无 |
| 3 | 0.65 | 粉末 | 0.8 | 50 | 20 | 无 |
| 4 | 0.65 | 粉末 | 0.8 | 50 | 35 | 2滴CuSO4溶液 |
(2)实验2和3表明,
(3)进行实验2时,小组同学根据实验过程绘制的气体体积(标准状况下)与时间的图象如图所示。

①在OA、AB、BC三段中,反应速率最快的是
②2~4min内以硫酸的浓度变化表示的平均反应速率
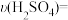
 (假设溶液的体积不变)。
(假设溶液的体积不变)。(4)实验过程中,小组同学发现实验4的速率明显大于实验3的速率,原因是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】NaNO2溶液和NH4Cl溶液可发生反应:NaNO2+NH4Cl NaCl+N2↑+2H2O↑。为探究反应速率与c(NaNO2)的关系,利用下列装置(夹持仪器略去)进行实验。
NaCl+N2↑+2H2O↑。为探究反应速率与c(NaNO2)的关系,利用下列装置(夹持仪器略去)进行实验。
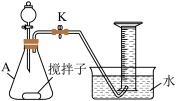
实验步骤:往A中加入一定体积(V)的2.0mol•L-1NaNO2溶液、2.0mol•L-1NH4Cl溶液和水,充分搅拌。控制体系温度,通过分液漏斗往A中加入1.0mol•L-1醋酸。当导管口气泡均匀稳定冒出时,开始用排水法收集气体。用秒表测量收集1.0mLN2所需的时间,重复多次取平均值(t)。
每组实验过程中,反应物浓度变化很小,忽略其对反应速率测定的影响。实验数据如表所示。
(1)V1=______ ,V3=______ 。
(2)该反应的速率方程为v=k•cm(NaNO2)•c(NH4Cl)•c(H+),k为反应速率常数。利用实验数据计算得m=______ (填整数)。
(3)醋酸的作用是______ 。
 NaCl+N2↑+2H2O↑。为探究反应速率与c(NaNO2)的关系,利用下列装置(夹持仪器略去)进行实验。
NaCl+N2↑+2H2O↑。为探究反应速率与c(NaNO2)的关系,利用下列装置(夹持仪器略去)进行实验。
实验步骤:往A中加入一定体积(V)的2.0mol•L-1NaNO2溶液、2.0mol•L-1NH4Cl溶液和水,充分搅拌。控制体系温度,通过分液漏斗往A中加入1.0mol•L-1醋酸。当导管口气泡均匀稳定冒出时,开始用排水法收集气体。用秒表测量收集1.0mLN2所需的时间,重复多次取平均值(t)。
每组实验过程中,反应物浓度变化很小,忽略其对反应速率测定的影响。实验数据如表所示。
| 实验编号 | VmL | t/s | |||
| NaNO2溶液 | NH4Cl溶液 | 醋酸 | 水 | ||
| 1 | 4.0 | V1 | 4.0 | 8.0 | 334 |
| 2 | V2 | 4.0 | 4.0 | V3 | 150 |
| 3 | 8.0 | 4.0 | 4.0 | 4.0 | 83 |
| 4 | 12.0 | 4.0 | 4.0 | 0.0 | 38 |
(2)该反应的速率方程为v=k•cm(NaNO2)•c(NH4Cl)•c(H+),k为反应速率常数。利用实验数据计算得m=
(3)醋酸的作用是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】某实验小组用酸性 溶液和
溶液和 (草酸)反应研究影响反应速率的因素,反应的方程式为
(草酸)反应研究影响反应速率的因素,反应的方程式为 。他们通过测定单位时间内生成
。他们通过测定单位时间内生成 的体积,探究某种影响化学反应速率的因素,设计方案如下(
的体积,探究某种影响化学反应速率的因素,设计方案如下( 溶液已酸化):
溶液已酸化):
(1)酸性 溶液中所加的酸应是(填字母序号)___________。
溶液中所加的酸应是(填字母序号)___________。
(2)该实验探究的是___________ 对化学反应速率的影响。
(3)实验停止前,相同时间内针筒中所得 体积较大是
体积较大是___________ (填实验序号)。
(4)若实验①在2min末注射器的活塞从最左端(刻度为20mL)向右移动到了V mL的位置,则这段时间内的平均反应速率可表示为
___________  。
。
(5)若实验②在t min收集了2.24mL (标准状况),则t min末
(标准状况),则t min末 的物质的量浓度为
的物质的量浓度为___________  。
。
(6)该小组同学发现反应速率总是如图,其中 ~
~ 时间内速率变快的主要原因可能是:①
时间内速率变快的主要原因可能是:①___________ ,②___________
 溶液和
溶液和 (草酸)反应研究影响反应速率的因素,反应的方程式为
(草酸)反应研究影响反应速率的因素,反应的方程式为 。他们通过测定单位时间内生成
。他们通过测定单位时间内生成 的体积,探究某种影响化学反应速率的因素,设计方案如下(
的体积,探究某种影响化学反应速率的因素,设计方案如下( 溶液已酸化):
溶液已酸化):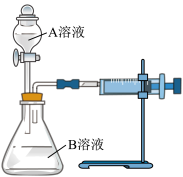
| 实验序号 | A溶液 | B溶液 |
| ① | 20mL 0.2  溶液 溶液 | 30mL 0.01  溶液 溶液 |
| ② | 20mL 0.1  溶液 溶液 | 30mL 0.01  溶液 溶液 |
(1)酸性
 溶液中所加的酸应是(填字母序号)___________。
溶液中所加的酸应是(填字母序号)___________。| A.硫酸 | B.盐酸 | C.硝酸 | D.以上三种酸都可 |
(2)该实验探究的是
(3)实验停止前,相同时间内针筒中所得
 体积较大是
体积较大是(4)若实验①在2min末注射器的活塞从最左端(刻度为20mL)向右移动到了V mL的位置,则这段时间内的平均反应速率可表示为

 。
。(5)若实验②在t min收集了2.24mL
 (标准状况),则t min末
(标准状况),则t min末 的物质的量浓度为
的物质的量浓度为 。
。(6)该小组同学发现反应速率总是如图,其中
 ~
~ 时间内速率变快的主要原因可能是:①
时间内速率变快的主要原因可能是:①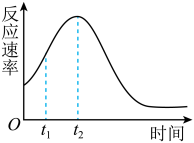
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】回答下列问题:
(1)某小组利用H2C2O4溶液和硫酸酸化的KMnO4溶液反应来探究“外界条件对化学反应速率的影响”。实验时通过测定酸性KMnO4溶液褪色所需时间来判断反应的快慢。该小组设计了如表方案。
①该过程发生反应的化学方程式____ 。
②表中V1=___ mL。
③实验①测得KMnO4溶液的褪色时间为2min,忽略混合前后溶液体积的微小变化,这段时间内平均反应速率v(H2C2O4)____ mol·L-1·min-1。
(2)一种新型催化剂能使NO和CO发生反应:2NO+2CO 2CO2+N2。已知增大催化剂的比表面税可提高该反应速率。为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,如表所示。
2CO2+N2。已知增大催化剂的比表面税可提高该反应速率。为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,如表所示。
①表中a=____ 。
②能验证温度对化学反应速率影响规律的是实验____ (填实验编号)。
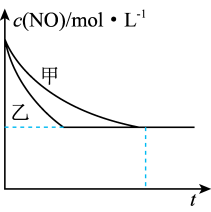
③实验I和实验Ⅱ中,NO的物质的量浓度c(NO)随时间t的变化曲线如图所示,其中表示实验II的是曲线____ (填“甲”或“乙”)。
(1)某小组利用H2C2O4溶液和硫酸酸化的KMnO4溶液反应来探究“外界条件对化学反应速率的影响”。实验时通过测定酸性KMnO4溶液褪色所需时间来判断反应的快慢。该小组设计了如表方案。
| 实验 编号 | 0.1mol/L酸性KMnO4溶液的体积/mL | 0.6mol/LH2C2O4溶液的体积/mL | H2O的体积/mL | 实验温度/℃ | 溶液褪色所需 时间/min |
| ① | 10 | V1 | 35 | 25 | |
| ② | 10 | 10 | 30 | 25 | |
| ③ | 10 | 10 | V2 | 50 |
②表中V1=
③实验①测得KMnO4溶液的褪色时间为2min,忽略混合前后溶液体积的微小变化,这段时间内平均反应速率v(H2C2O4)
(2)一种新型催化剂能使NO和CO发生反应:2NO+2CO
 2CO2+N2。已知增大催化剂的比表面税可提高该反应速率。为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,如表所示。
2CO2+N2。已知增大催化剂的比表面税可提高该反应速率。为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,如表所示。| 实验编号 | t/℃ | NO初始浓度/mol·L-1 | CO初始浓度/mol·L-1 | 催化剂的比表面积/m2/g |
| I | 280 | 1.20×10-3 | 5.80×10-3 | 82 |
| II | 280 | 1.20×10-3 | b | 124 |
| Ⅲ | 350 | a | 5.80×10-3 | 82 |
②能验证温度对化学反应速率影响规律的是实验
③实验I和实验Ⅱ中,NO的物质的量浓度c(NO)随时间t的变化曲线如图所示,其中表示实验II的是曲线

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】化学反应都伴随有能量变化。
(1)以甲烷为原料制取氢气是工业上常用的制氢方法。
已知:
 kJ⋅mol-1
kJ⋅mol-1

 kJ⋅mol-1
kJ⋅mol-1

 kJ⋅mol-1
kJ⋅mol-1
 与
与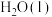 反应生成
反应生成 和
和 的热化学方程式为
的热化学方程式为___________ 。
(2)如图所示为常温常压下,1mol 和1mol
和1mol 完全反应生成
完全反应生成 和
和 过程中的能量变化。
过程中的能量变化。
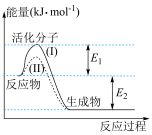
①曲线II表示___________ (填“有”或“无”)催化剂作用时的能量变化。
②若能量变化如曲线I所示,该反应逆反应的活化能为___________ kJ⋅mol-1。
③若常温常压下,1mol 完全燃烧放出的热量为
完全燃烧放出的热量为 kJ,则
kJ,则

___________ kJ⋅mol-1。
(3)工业上,在一定条件下利用乙烯和水蒸气反应制备乙醇。键能如下表所示,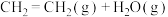
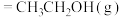 反应的
反应的
___________ kJ⋅mol-1。
(1)以甲烷为原料制取氢气是工业上常用的制氢方法。
已知:

 kJ⋅mol-1
kJ⋅mol-1
 kJ⋅mol-1
kJ⋅mol-1
 kJ⋅mol-1
kJ⋅mol-1 与
与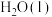 反应生成
反应生成 和
和 的热化学方程式为
的热化学方程式为(2)如图所示为常温常压下,1mol
 和1mol
和1mol 完全反应生成
完全反应生成 和
和 过程中的能量变化。
过程中的能量变化。
①曲线II表示
②若能量变化如曲线I所示,该反应逆反应的活化能为
③若常温常压下,1mol
 完全燃烧放出的热量为
完全燃烧放出的热量为 kJ,则
kJ,则

(3)工业上,在一定条件下利用乙烯和水蒸气反应制备乙醇。键能如下表所示,
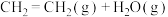
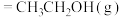 反应的
反应的
| 化学键 |  |  |  |  |  |
| 键能/(kJ·mol-1) | 413 | 615 | 463 | 348 | 351 |
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】现代社会的一切活动都离不开能量,化学反应发生物质变化的同时伴随着能量的变化,是人类获取能量的重要途径。回答下列问题:
(1)汽车尾气中NO生成过程的能量变化如图所示。1 mol 和1 mol
和1 mol  完全反应生成NO会
完全反应生成NO会___________ (填“吸收”或“放出”)___________ kJ能量。
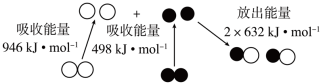
1 mol (g)和1 mol
(g)和1 mol  (g)反应生成2 mol NO(g)过程中的能量变化
(g)反应生成2 mol NO(g)过程中的能量变化
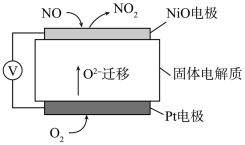
(2)通过NO传感器可监测汽车尾气中NO的含量,其工作原理如图所示, 可在固体电解质中自由移动。则NiO电极上发生的是
可在固体电解质中自由移动。则NiO电极上发生的是___________ (填“氧化”或“还原”)反应;Pt电极上的电极反应式为___________ 。
(3)一种新型催化剂能使NO和CO发生反应: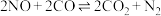 。已知增大催化剂的比表面积可提高该反应速率。为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,如表所示。
。已知增大催化剂的比表面积可提高该反应速率。为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,如表所示。
①表中a=___________ ;能验证温度对化学反应速率影响规律的是___________ (填实验编号)。
②实验Ⅰ和实验Ⅱ中,NO的物质的量浓度c(NO)随时间t的变化曲线如图所示,其中表示实验Ⅱ的是曲线___________ (填“甲”或“乙”)

(1)汽车尾气中NO生成过程的能量变化如图所示。1 mol
 和1 mol
和1 mol  完全反应生成NO会
完全反应生成NO会
1 mol
 (g)和1 mol
(g)和1 mol  (g)反应生成2 mol NO(g)过程中的能量变化
(g)反应生成2 mol NO(g)过程中的能量变化(2)通过NO传感器可监测汽车尾气中NO的含量,其工作原理如图所示,
 可在固体电解质中自由移动。则NiO电极上发生的是
可在固体电解质中自由移动。则NiO电极上发生的是
(3)一种新型催化剂能使NO和CO发生反应:
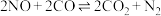 。已知增大催化剂的比表面积可提高该反应速率。为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,如表所示。
。已知增大催化剂的比表面积可提高该反应速率。为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,如表所示。| 实验编号 | T/℃ | NO初始浓度( ) ) | CO初始浓度( ) ) | 催化剂的比表面积(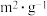 ) ) |
| Ⅰ | 280 |  |  | 82 |
| Ⅱ | 280 |  |  | 124 |
| Ⅲ | 350 | a |  | 82 |
①表中a=
②实验Ⅰ和实验Ⅱ中,NO的物质的量浓度c(NO)随时间t的变化曲线如图所示,其中表示实验Ⅱ的是曲线

您最近一年使用:0次



