下列实验操作、现象描述、得出的结论均正确的是
| 实验 | 结论 | |
| A | 将充满氨气的试管倒置于滴有石蕊的水槽中,试管内迅速充满红色液体 | NH3极易溶于水且溶液显碱性 |
| B | 向酸性KMnO4溶液中加入维生素C含片,溶液褪色 | 维生素C具有还原性 |
| C | 向含有BaSO4沉淀的溶液中加入过量饱和Na2CO3溶液 后过滤、洗涤,向所得沉淀中加入稀盐酸,有气泡产生 | Ksp(BaSO4)一定大于Ksp(BaCO3) |
| D | 向可乐中加入牛奶,有沉淀产生 | 牛奶中的钙元素和可乐中的碳酸生成了CaCO3沉淀 |
| A.A | B.B | C.C | D.D |
更新时间:2022-07-06 18:26:47
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】常温下,已知CaSO4的Ksp=4.9×10-5,CaCO3的Ksp=3.6×10-9,下列说法正确的是
| A.该温度下,将5×10-2 mol/L氯化钙溶液与2×10-3 mol/L硫酸钠溶液等体积混合(忽略体积变化),混合后没有沉淀生成 |
B.向CaSO4悬浊液中加入稀硫酸,c(SO )增大,Ksp增大 )增大,Ksp增大 |
C.向只含CaCO3的悬浊液中加入Na2SO4固体至c(SO )=8.2×10-2 mol/L时,CaCO3开始向CaSO4沉淀转化 )=8.2×10-2 mol/L时,CaCO3开始向CaSO4沉淀转化 |
| D.向只含CaCO3的悬浊液中加入少量的水,c(Ca2+)减小 |
您最近一年使用:0次
【推荐2】已知常温下,Ksp(CuS)=1.0×10-36,Ksp(HgS)=1.6×10-52,;pM=-lgc(M2+)。常温下,向10mL0.2mol/LCu(NO3)2溶液中逐滴滴加0.1mol/LNa2S溶液,溶液pM与加入Na2S溶液的体积(V)的关系如图所示。下列说法中错误的是


| A.V0=20.0 mL,m=18 |
| B.若c[Cu(NO3)2]=0.1mol/L,则反应终点可能为e点 |
| C.a、b、d三点中,由水电离的c(H+)和c(OH-)之和最大的为b点 |
| D.若用等浓度等体积Hg(NO3)2溶液代替Cu(NO3)2溶液,则反应终点b向c方向移动 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
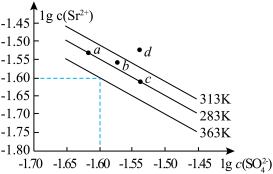
【推荐1】某温度下,向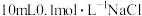 溶液和
溶液和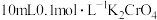 溶液中分别滴加
溶液中分别滴加 溶液.滴加过程中
溶液.滴加过程中 [
[ 或
或 ]与所加
]与所加 溶液体积之间的关系如下图所示。已知
溶液体积之间的关系如下图所示。已知 为红棕色沉淀。下列说法错误的是
为红棕色沉淀。下列说法错误的是

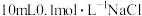 溶液和
溶液和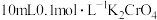 溶液中分别滴加
溶液中分别滴加 溶液.滴加过程中
溶液.滴加过程中 [
[ 或
或 ]与所加
]与所加 溶液体积之间的关系如下图所示。已知
溶液体积之间的关系如下图所示。已知 为红棕色沉淀。下列说法错误的是
为红棕色沉淀。下列说法错误的是
A.该温度下, |
B.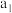 、b、c三点所示溶液中 、b、c三点所示溶液中 : : |
C.若将上述 溶液浓度改为 溶液浓度改为 则 则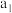 点会平移至 点会平移至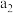 点 点 |
D.用 标准溶液滴定 标准溶液滴定 溶液时,可用 溶液时,可用 溶液作指示剂 溶液作指示剂 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】已知25℃时Ksp[Mg(OH)2]=1.8×10-11,Ksp [Fe(OH)3]=8.0×10-38,Kb(NH3·H2O)= 1.8×10-5,下列叙述不正确的是
| A.Mg(OH)2、Fe(OH)3的饱和溶液中c(OH-)的大小顺序:Mg(OH)2>Fe(OH)3,25℃时,向等浓度的MgCl2和FeCl3混合溶液中逐滴加入氨水,先出现红褐色沉淀, |
| B.25℃时,加大量水稀释氨水,电离程度增大,溶液pH减小 |
C.25℃时,NH4++H2O NH3·H2O+H+的平衡常数为5.6×10-10 NH3·H2O+H+的平衡常数为5.6×10-10 |
| D.将0.02 mol•L-1MgCl2溶液和0.02 mol•L-1NaOH溶液等体积混合,没有沉淀生成 |
您最近一年使用:0次

 。某温度下,饱和溶液中
。某温度下,饱和溶液中 、
、 与
与 的关系如图所示。下列说法正确的是
的关系如图所示。下列说法正确的是
 时两溶液中
时两溶液中
 值为
值为
 )之间的关系,下列有关说法正确的是
)之间的关系,下列有关说法正确的是