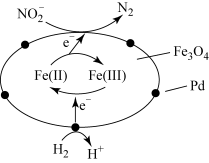
在催化剂作用下,H2可处理废水中的NO ,反应原理如图所示。下列说法错误的是
,反应原理如图所示。下列说法错误的是
 ,反应原理如图所示。下列说法错误的是
,反应原理如图所示。下列说法错误的是
| A.Fe3O4具有传递电子的作用 |
| B.Pd和Fe3O4均是该过程的催化剂 |
| C.处理后的废水中酸性增强 |
D.每消耗67.2L(标准状况下)H2,可还原2molNO |
更新时间:2022-07-14 14:34:55
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】 煤和石油是重要的能源物质,一方面对其开发利用推动人类社会快速进入工业文明时代,另一方面化石燃料燃烧产生 带来的环境问题日益凸显,“碳中和”已成为新时代绿色发展理念。煤经汽化、液化后再利用,可提高效能、降低污染,其常见原理为:
带来的环境问题日益凸显,“碳中和”已成为新时代绿色发展理念。煤经汽化、液化后再利用,可提高效能、降低污染,其常见原理为:
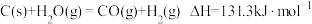
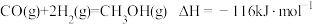
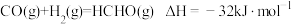
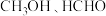 等产物在化工生产中都有广泛用途。对于反应
等产物在化工生产中都有广泛用途。对于反应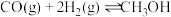 ,下列说法
,下列说法不 正确的是
 带来的环境问题日益凸显,“碳中和”已成为新时代绿色发展理念。煤经汽化、液化后再利用,可提高效能、降低污染,其常见原理为:
带来的环境问题日益凸显,“碳中和”已成为新时代绿色发展理念。煤经汽化、液化后再利用,可提高效能、降低污染,其常见原理为: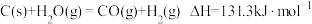
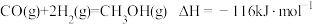
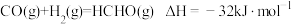
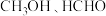 等产物在化工生产中都有广泛用途。对于反应
等产物在化工生产中都有广泛用途。对于反应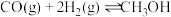 ,下列说法
,下列说法A.反应的平衡常数可表示为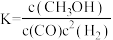 |
B.反应活化能: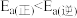 |
C. 和 和 充分反应,转移电子数目约为 充分反应,转移电子数目约为 个 个 |
D.平衡后增大容器的体积, 、 、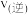 都减小 都减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】将磁性氧化铁放入稀HNO3中可发生如下反应:
3Fe3O4 + 28HNO3 =9Fe(NO3)x + NO↑+ 14H2O下列判断合理的是
3Fe3O4 + 28HNO3 =9Fe(NO3)x + NO↑+ 14H2O下列判断合理的是
| A.Fe(NO3)x中的x为2 |
| B.反应中每还原0.4 mol氧化剂,就有1.2 mol电子转移 |
| C.稀HNO3在反应中只表现氧化性 |
| D.磁性氧化铁中的所有铁元素全部被氧化 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列离子方程式书写正确的是
| A.少量SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO-=CaSO3↓+2HClO |
| B.Fe(NO3)3溶液中加入过量的HI溶液2Fe3++2I-=2Fe2++I2 |
C.NaNO2溶液中加入酸性KMnO4溶液:2MnO +5NO +5NO +6H+=2Mn2++5NO +6H+=2Mn2++5NO +3H2O +3H2O |
D.NaHCO3溶液加入过量的Ba(OH)2溶液:2HCO +Ba2++2OH-=BaCO3↓+2H2O+CO +Ba2++2OH-=BaCO3↓+2H2O+CO |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】元素及其化合物性质丰富。下列离子方程式书写正确的是
A.铜和稀硝酸反应: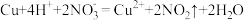 |
B.硫代硫酸钠中加入稀硫酸: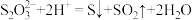 |
C.少量二氧化硫通入溴水中: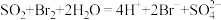 |
D.碘化亚铁溶液与等物质的量的氯气: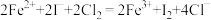 |
您最近一年使用:0次
【推荐3】高铁酸钾(K2FeO4)是一种既能杀菌、消毒、又能絮凝净水的水处理剂,工业制备高铁酸钾的离子方程式为Fe(OH)3+ClO-+OH-→FeO +Cl-+H2O(未配平)。下列有关说法不正确的是
+Cl-+H2O(未配平)。下列有关说法不正确的是
 +Cl-+H2O(未配平)。下列有关说法不正确的是
+Cl-+H2O(未配平)。下列有关说法不正确的是| A.高铁酸钾中铁显+6价 |
B.由上述反应可知,Fe(OH)3的氧化性强于FeO |
| C.上述反应中氧化剂和还原剂的物质的量之比为3∶2 |
| D.K2FeO4处理水时,生成的Fe3+水解形成Fe(OH)3胶体,能吸附水中的悬浮杂质 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】研究催化剂对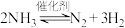 反应速率的影响。恒温恒容时,c(NH3)随时间的变化如下。
反应速率的影响。恒温恒容时,c(NH3)随时间的变化如下。
下列说法不正确 的是
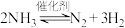 反应速率的影响。恒温恒容时,c(NH3)随时间的变化如下。
反应速率的影响。恒温恒容时,c(NH3)随时间的变化如下。| 时间/min 催化剂 c(NH3)/(×10−3 mol·L−1) | 0 | 20 | 40 | 60 | 80 |
| 催化剂Ⅰ | 2.40 | 2.00 | 1.60 | 1.20 | 0.80 |
| 催化剂Ⅱ | 2.40 | 1.60 | 0.80 | 0.40 | 0.40 |
| A.使用催化剂Ⅰ,0~20 min的平均反应速率v(N2)=1.00×10−5 mol·L−1·min−1 |
B.使用催化剂Ⅰ,达平衡后容器内的压强是初始时的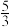 倍 倍 |
| C.相同条件下,使用催化剂Ⅱ可使该反应的活化能降低更多,反应更快 |
| D.相同条件下,使用催化剂Ⅱ不会使该反应的化学平衡常数更大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】已知2NO(g)+O2(g) 2NO2(g) △H<0,反应历程分两步:
2NO2(g) △H<0,反应历程分两步:
快反应:①2NO(g) N2O2(g) △H1<0,v1正=k1正c2(NO),v 1逆=k1逆c(N2O2)
N2O2(g) △H1<0,v1正=k1正c2(NO),v 1逆=k1逆c(N2O2)
慢反应:②N2O2(g)+O2(g) 2NO2(g) △H2<0,v2正=k2正c(N2O)·c(O2),v2逆=k2逆c2(NO2)
2NO2(g) △H2<0,v2正=k2正c(N2O)·c(O2),v2逆=k2逆c2(NO2)
下列说法正确的是
 2NO2(g) △H<0,反应历程分两步:
2NO2(g) △H<0,反应历程分两步:快反应:①2NO(g)
 N2O2(g) △H1<0,v1正=k1正c2(NO),v 1逆=k1逆c(N2O2)
N2O2(g) △H1<0,v1正=k1正c2(NO),v 1逆=k1逆c(N2O2)慢反应:②N2O2(g)+O2(g)
 2NO2(g) △H2<0,v2正=k2正c(N2O)·c(O2),v2逆=k2逆c2(NO2)
2NO2(g) △H2<0,v2正=k2正c(N2O)·c(O2),v2逆=k2逆c2(NO2)下列说法正确的是
| A.N2O2是该反应的催化剂 |
| B.温度升高k1正、k2正均减小, k1逆、k2逆均增大 |
| C.反应②中N2O2与O2的碰撞仅部分有效 |
| D.反应①正反应的活化能大于逆反应的活化能 |
您最近一年使用:0次