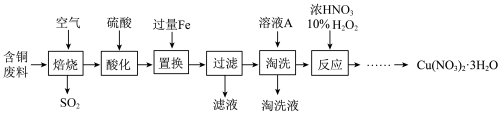
下列物质去除杂质的方法中,不合理的是
| 物质(杂质) | 除杂试剂 | 分离方法 | |
| A | NO( ) ) |  | 洗气 |
| B | 乙酸乙酯(乙酸) | 饱和碳酸钠溶液 | 蒸馏 |
| C |  溶液 (FeCl3) 溶液 (FeCl3) | 氨水 | 过滤 |
| D | 乙炔 (H2S) |  溶液 溶液 | 洗气 |
| A.A | B.B | C.C | D.D |
21-22高三·湖北·阶段练习 查看更多[3]
更新时间:2022-08-13 18:47:04
|
相似题推荐
【推荐1】下列实验设计不能达到实验目的的是
| 选项 | 实验操作或做法 | 实验目的 |
| A | 制备乙酸乙酯实验中可用饱和 溶液洗涤分液 溶液洗涤分液 | 除去乙酸乙酯中的乙醇和乙酸 |
| B | 向苯中滴加浓溴水,并加入 作催化剂 作催化剂 | 制取溴苯 |
| C | 向 中加入大量的水,同时加热,促进水解趋于完全,所得沉淀过滤、焙烧 中加入大量的水,同时加热,促进水解趋于完全,所得沉淀过滤、焙烧 | 制备 |
| D | 在相同条件下,将颗粒大小相同的钠分别与乙醇、水反应 | 比较乙醇分子中羟基氢原子和水分子中氢原子的活泼性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】利用如图装置制备乙酸乙酯粗产品,再经除杂、干燥、蒸馏收集74~80℃的馏分,获得较高纯度乙酸乙酯。分馏柱可以分离沸点差异较小的组分。相关物质及组成共沸体系的沸点如下。

下列说法错误的是

| 物质 | 沸点/℃ | 共沸体系 | 沸点/℃ |
| 水 | 100.0 | 乙醇-水 | 78.2 |
| 乙醇 | 78.5 | 乙醇-乙酸乙酯 | 72.0 |
| 乙酸 | 117.9 | 乙酸乙酯-水 | 70.4 |
| 乙酸乙酯 | 77.0 | 乙醇-水-乙酸乙酯 | 70.2 |
| A.选择合适长度的分馏柱可减少乙醇损失 |
| B.原料中水的作用是为了形成含水共沸体系利于乙酸乙酯蒸出 |
| C.反应温度控制在120℃左右,可减少副反应发生 |
| D.粗产品除杂后直接蒸馏将导致收集到的产物质量偏大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】实验室制取乙烯并验证其化学性质,下列装置正确的是
 |  |  | 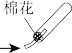 |
| A.制备乙烯 | B.除去杂质 | C.验证加成反应 | D.收集乙烯 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列除杂质选用试剂错误的是
| 编号 | 物质 | 杂质 | 试剂 |
| A | FeCl3 | FeCl2 | 氯气 |
| B | Cl2 | HCl | 饱和食盐水 |
| C | SiO2 | Fe2O3 | 盐酸 |
| D | CO2 | CO | O2 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】下列实验操作能达到预期实验目的的是
| 选项 | 实验操作 | 预期目的 |
| A. | 将氯气和氯化氢混合气体通过饱和食盐水洗气 | 除去氯化氢杂质得到纯净的氯气 |
| B. | 常温下,向 溶液中加入 溶液中加入 溶液,将带火星的木条放在试管口,木条复燃 溶液,将带火星的木条放在试管口,木条复燃 | 判断氧化性: |
| C. | 标况下向足量次氯酸钠溶液中缓慢通入一定量含有二氧化硫的某气体,然后加入足量氯化钡溶液,过滤,洗涤,干燥,称量沉淀质量 | 可根据沉淀质量计算二氧化硫的体积分数 |
| D. | 向麦芽糖溶液中加入少量稀硫酸,加热,滴加 溶液调至呈碱性,再加入银氨溶液,水浴加热,可观察到产生银镜 溶液调至呈碱性,再加入银氨溶液,水浴加热,可观察到产生银镜 | 验证麦芽糖水解产物具有还原性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】我国电池的年市场消费量约为80亿只,其中70%是锌锰干电池,某工艺利用软锰矿(主要成分MnO2,含少量A12O3和SiO2)和闪锌矿(主要成分是ZnS,含少量FeS、CuS、CdS)为原料制备MnO2和Zn,其流程如下:
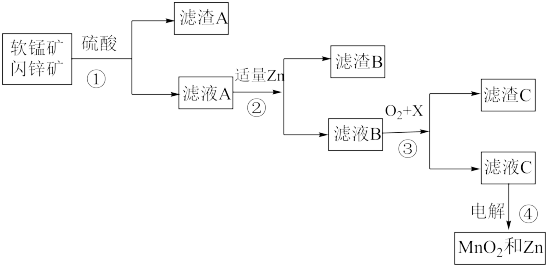
已知:I.矿石中所有金属元素均以离子形式进入滤液A中。
II.各种金属离子完全沉淀的pH如下表:
下列说法中不正确的是

已知:I.矿石中所有金属元素均以离子形式进入滤液A中。
II.各种金属离子完全沉淀的pH如下表:
| Zn2+ | Mn2+ | Fe2+ | Fe3+| | Al3+ | |
| pH | 8.0 | 10.1 | 9.0 | 3.2 | 4.7 |
| A.滤渣A主要成分:S和SiO2 |
| B.适量金属锌是为了回收金属Cu和Cd |
| C.步骤③中,加入物质X可以是MnO2,调pH:4.7≤pH<8.0 |
| D.上述流程中,可以循环使用的物质有H2SO4 |
您最近一年使用:0次
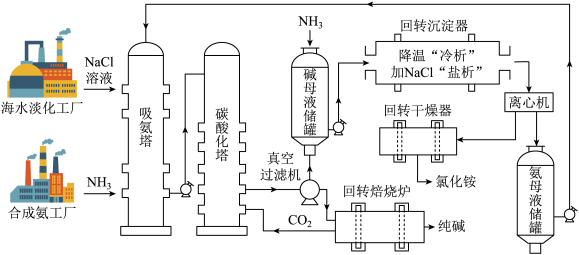
【推荐2】我国化学家侯德榜发明的“侯氏制碱法”联合合成氨工业生产纯碱和氮肥,工艺流程图如下。碳酸化塔中的反应: 。
。
 。
。
A. :碱母液储罐大于氨母液储罐 :碱母液储罐大于氨母液储罐 |
B.经“冷析”和“盐析”后的体系仅是 的饱和溶液 的饱和溶液 |
| C.该工艺的碳原子利用率理论上接近100% |
D.向氯化钠溶液中先通入 ,再通入 ,再通入 能提高 能提高 |
您最近一年使用:0次