按要求写出下列方程式:
(1)NaHCO3受热分解的化学方程式_______ 。
(2)少量Na2O2投入CuSO4溶液中的离子方程式_______ 。
(3)向NaHSO4溶液中加入Ba(OH)2至 刚好沉淀完全的离子方程式
刚好沉淀完全的离子方程式_______ 。
(4)MnO2溶于用H2SO4酸化的FeSO4溶液的离子方程式_______ 。
(1)NaHCO3受热分解的化学方程式
(2)少量Na2O2投入CuSO4溶液中的离子方程式
(3)向NaHSO4溶液中加入Ba(OH)2至
 刚好沉淀完全的离子方程式
刚好沉淀完全的离子方程式(4)MnO2溶于用H2SO4酸化的FeSO4溶液的离子方程式
更新时间:2022-04-06 10:02:16
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】弱电解质在水溶液中的电离状况可以进行定量计算和推测。
(1)已知:25℃时, ,
, 、
、 。
。
①25℃时,0.100mol/L的NaA溶液中, 、
、 、
、 、
、 、HA的物质的量浓度由大到小的顺序为
、HA的物质的量浓度由大到小的顺序为___________ ;pH=8的NaA溶液中由水电离出的
___________ mol/L。
②25℃时,0.100mol/L的NaHB溶液呈酸性,理由是___________ 。(结合数据分析)
③25℃时,向0.100mol/L的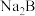 溶液中滴加足量0.100mol/L的HA溶液,对应反应的离子方程式为
溶液中滴加足量0.100mol/L的HA溶液,对应反应的离子方程式为___________ 。
(2)已知:25℃时,向0.100mol/L的 溶液中滴加NaOH溶液,各含磷微粒的物质的量分数随pH变化的关系如图所示。
溶液中滴加NaOH溶液,各含磷微粒的物质的量分数随pH变化的关系如图所示。
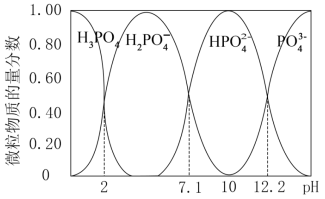
①将NaOH溶液逐滴加入到 溶液中,当溶液由无色变为浅红色时停止滴加。该过程中主要反应的离子方程式为
溶液中,当溶液由无色变为浅红色时停止滴加。该过程中主要反应的离子方程式为___________ 。
②pH=2时,溶液中
___________ 。
(3)等物质的量浓度的 和
和 溶液等体积混合,所得溶液中
溶液等体积混合,所得溶液中 、
、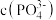 、
、 、
、 、
、 的守恒关系式为
的守恒关系式为___________ 。
(1)已知:25℃时,
 ,
, 、
、 。
。①25℃时,0.100mol/L的NaA溶液中,
 、
、 、
、 、
、 、HA的物质的量浓度由大到小的顺序为
、HA的物质的量浓度由大到小的顺序为
②25℃时,0.100mol/L的NaHB溶液呈酸性,理由是
③25℃时,向0.100mol/L的
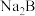 溶液中滴加足量0.100mol/L的HA溶液,对应反应的离子方程式为
溶液中滴加足量0.100mol/L的HA溶液,对应反应的离子方程式为(2)已知:25℃时,向0.100mol/L的
 溶液中滴加NaOH溶液,各含磷微粒的物质的量分数随pH变化的关系如图所示。
溶液中滴加NaOH溶液,各含磷微粒的物质的量分数随pH变化的关系如图所示。
①将NaOH溶液逐滴加入到
 溶液中,当溶液由无色变为浅红色时停止滴加。该过程中主要反应的离子方程式为
溶液中,当溶液由无色变为浅红色时停止滴加。该过程中主要反应的离子方程式为②pH=2时,溶液中

(3)等物质的量浓度的
 和
和 溶液等体积混合,所得溶液中
溶液等体积混合,所得溶液中 、
、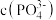 、
、 、
、 、
、 的守恒关系式为
的守恒关系式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】某同学探究Ba(OH)2和H2SO4反应的实质,利用下图装置进行实验。向20 ml 0.01 mol/L Ba(OH)2 溶液中滴入几滴酚酞溶液,然后向其中匀速逐滴加入2 ml 0.2 mol/L H2SO4溶液。

(1)实验过程中溶液中的现象为________ 、 ________ 。
(2)该反应的离子方程式是__________________ 。
(3)画出反应过程中溶液电导率变化示意图__________________ 。
(4)解释反应过程中溶液电导率出现上述变化的原因___ 。

(1)实验过程中溶液中的现象为
(2)该反应的离子方程式是
(3)画出反应过程中溶液电导率变化示意图
(4)解释反应过程中溶液电导率出现上述变化的原因
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】Ⅰ.分类是学习化学的重要方法之一。现有下列物质:①CaCO3,②熔融氯化钠,③澄清石灰水,④小苏打,⑤乙醇,⑥FeCl3溶液,⑦CO2,⑧Cu。回答下列问题:
(1)在上述8种物质中,属于电解质的有______ (填序号,下同),上述状态下能导电的有______ 。
(2)④在水中的电离方程式为____________________ 。
(3)④的溶液和少量③发生反应的离子方程式为____________________ 。
Ⅱ.某化学兴趣小组利用下图装置探究Na2O2与水反应的能量变化。在图中,调节U形管内两侧液面相平,向试管中加入Na2O2粉末,再滴加10 mL蒸馏水。观察到试管内产生大量气泡。

(4)观察到U形管内液面______ (填标号),说明该反应放出热量。
A.左侧较高 B.右侧较高 C.左、右两侧一样高
(5)写出Na2O2与水反应的化学方程式____________________ 。
(1)在上述8种物质中,属于电解质的有
(2)④在水中的电离方程式为
(3)④的溶液和少量③发生反应的离子方程式为
Ⅱ.某化学兴趣小组利用下图装置探究Na2O2与水反应的能量变化。在图中,调节U形管内两侧液面相平,向试管中加入Na2O2粉末,再滴加10 mL蒸馏水。观察到试管内产生大量气泡。

(4)观察到U形管内液面
A.左侧较高 B.右侧较高 C.左、右两侧一样高
(5)写出Na2O2与水反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)研究物质时会涉及物质的组成、分类、性质和用途等方面。
①Na2O2属于____________ (填物质的类别),检验其组成中所含阳离子的方法是_____________ 。
②将包有少量____ 色Na2O2固体的棉花放在石棉网上,用滴管向棉花上滴几滴水,观察到的现象是__________________ ,由此得出的结论是_________________________________ 。
③在潜水艇和消防员的呼吸面具中,Na2O2所发生反应的化学方程式为_________________________ ,从氧化剂和还原剂的角度分析,在该反应中Na2O2的作用是___________________ 。某潜水艇上有25人,如果每人每分钟消耗的O2在标准状况下体积为0.80L(标准状况下O2的密度为1.429g/L),假设所需要的O2全部由Na2O2来提供,则该潜水艇一天所需要的Na2O2的物质的量是_____________ 。
(2)写出下列反应的离子方程式:
①NaHCO3溶于醋酸:__________________________________________________ 。
②过量CO2与NaOH溶液:_____________________________________________ 。
③工业制漂白液:______________________________________________________ 。
④生活中漂白粉的漂白原理:____________________________________________ 。
①Na2O2属于
②将包有少量
③在潜水艇和消防员的呼吸面具中,Na2O2所发生反应的化学方程式为
(2)写出下列反应的离子方程式:
①NaHCO3溶于醋酸:
②过量CO2与NaOH溶液:
③工业制漂白液:
④生活中漂白粉的漂白原理:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】1807年通过电解氢氧化钠制得金属钠,这个原理应用于工业生产,约在1891年才获得成功。1921年实现了电解氯化钠制钠的工业方法,其反应原理是 。回答下列有关单质钠的问题:
。回答下列有关单质钠的问题:
(1)下列各项中属于保存金属钠的正确方法是______ (填序号)。
A.放在棕色瓶中 B.放在细沙中
C.放在水中 D.放在煤油中
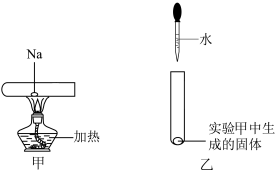
(2)将一小块钠放在水平放置的试管中部,用酒精灯加热充分反应,如图甲所示,生成物的颜色为______ ,请写出该反应的化学方程式:__________________ 。将该试管冷却后直立,滴加几滴水,如图乙所示,发生反应的离子方程式为__________________ 。
 。回答下列有关单质钠的问题:
。回答下列有关单质钠的问题:(1)下列各项中属于保存金属钠的正确方法是
A.放在棕色瓶中 B.放在细沙中
C.放在水中 D.放在煤油中
(2)将一小块钠放在水平放置的试管中部,用酒精灯加热充分反应,如图甲所示,生成物的颜色为

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】某汽车安全气囊的产气药剂主要含有 、
、 、
、 、
、 等物质。当汽车发生碰撞时,产气药剂产生大量气体使气嚢迅速膨胀,从而起到保护作用。回答下列问题:
等物质。当汽车发生碰撞时,产气药剂产生大量气体使气嚢迅速膨胀,从而起到保护作用。回答下列问题:
(1) 是气体发生剂,受热分解产生
是气体发生剂,受热分解产生 和Na,
和Na, 含有共价键的类型为
含有共价键的类型为_______ 。
(2) 是主氧化剂,Fe在周期表中的位置是
是主氧化剂,Fe在周期表中的位置是_______ 。 与Na反应生成的还原产物为
与Na反应生成的还原产物为_______ (已知该反应为置换反应)。
(3) 是助氧化剂,反应过程中与Na作用生成KCl和
是助氧化剂,反应过程中与Na作用生成KCl和 。
。 的电子式为
的电子式为_______ ,K的原子结构示意图为_______ 。
(4) 是冷却剂,吸收产气过程中释放的热量而发生分解反应,其化学方程式为
是冷却剂,吸收产气过程中释放的热量而发生分解反应,其化学方程式为_______ 。
(5)50g上述产气药剂产生的气体通过碱石灰后得到 (标准状况)。
(标准状况)。
①用碱石灰除去的物质为_______ ;
②该产气药剂中 的质量分数为
的质量分数为_______ 。
 、
、 、
、 、
、 等物质。当汽车发生碰撞时,产气药剂产生大量气体使气嚢迅速膨胀,从而起到保护作用。回答下列问题:
等物质。当汽车发生碰撞时,产气药剂产生大量气体使气嚢迅速膨胀,从而起到保护作用。回答下列问题:(1)
 是气体发生剂,受热分解产生
是气体发生剂,受热分解产生 和Na,
和Na, 含有共价键的类型为
含有共价键的类型为(2)
 是主氧化剂,Fe在周期表中的位置是
是主氧化剂,Fe在周期表中的位置是 与Na反应生成的还原产物为
与Na反应生成的还原产物为(3)
 是助氧化剂,反应过程中与Na作用生成KCl和
是助氧化剂,反应过程中与Na作用生成KCl和 。
。 的电子式为
的电子式为(4)
 是冷却剂,吸收产气过程中释放的热量而发生分解反应,其化学方程式为
是冷却剂,吸收产气过程中释放的热量而发生分解反应,其化学方程式为(5)50g上述产气药剂产生的气体通过碱石灰后得到
 (标准状况)。
(标准状况)。①用碱石灰除去的物质为
②该产气药剂中
 的质量分数为
的质量分数为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】2021年是国际化学年十周年纪念,中国的宣传口号是“化学一我们的生活,我们的未来”。
(1)高纯度单晶硅是典型的无机非金属材料,它的发现和使用曾引起计算机的一场“革命”。下列有关硅材料的说法正确的是_______(填字母)。
(2)工业上常用金属钠冶炼钛,是利用金属钠的强_______ 性。
(3)常温下,可用铁或铝制器皿盛放浓硝酸,是因为_______ 。
(4)纯碱和小苏打均为常见的厨房用品。兴趣小组同学用如图装置比较纯碱(Na2CO3)和小苏打(NaHCO3)的热稳定性。实验过程中可以观察到烧杯_______ (填“I”或“II”)中澄清石灰水变浑浊。加热后试管中发生反应的化学方程式为_______ 。

(5)智利硝石矿层中含有碘酸钠,可用亚硫酸氢钠与其反应来制备单质碘:NaIO3+NaHSO3→NaHSO4+Na2SO4+I2+H2O(未配平)。配平该方程式_______ 。
(1)高纯度单晶硅是典型的无机非金属材料,它的发现和使用曾引起计算机的一场“革命”。下列有关硅材料的说法正确的是_______(填字母)。
| A.晶体硅用于制作半导体材料 | B.硅在常温下化学性比较活泼 |
| C.玻璃属于硅酸盐材料 | D.玛瑙的主要成分是硅单质 |
(3)常温下,可用铁或铝制器皿盛放浓硝酸,是因为
(4)纯碱和小苏打均为常见的厨房用品。兴趣小组同学用如图装置比较纯碱(Na2CO3)和小苏打(NaHCO3)的热稳定性。实验过程中可以观察到烧杯

(5)智利硝石矿层中含有碘酸钠,可用亚硫酸氢钠与其反应来制备单质碘:NaIO3+NaHSO3→NaHSO4+Na2SO4+I2+H2O(未配平)。配平该方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】小明买了一种“汽泡爽”的冲调饮料,饮料说明如下:
【主要原料】柠檬酸(C6H8O7)和小苏打(NaHCO3);
【使用说明】将一包“汽泡爽”粉末倒入玻璃杯中,加入200mL冷水,看到有大量气泡快速生成,待粉末完全溶解,就得到一杯果味饮料。小明观察了饮料说明后,他借助化学实验的方法,探究“汽泡爽”产生气体的成分,以及加水温度对产生气体量的影响。
(1)“汽泡爽”中的小苏打(NaHCO3)是我们生活中常见的一种酸式盐,请按照下列要求写出相关方程式:
①小苏打受热易分解:___________ 。
②小苏打和盐酸的反应:___________ 。
③小苏打和氢氧化钠溶液的反应:___________ 。
【实验】探究“汽泡爽”产生气体的成分。
(2)小明阅读资料发现:“汽泡爽”原料中的柠檬酸(C6H8O7)和小苏打(NaHCO3)粉末混合后加水,可以发生以下反应,填写生成气体的化学式:3NaHCO3+C6H8O7=C6H5O7Na3+3H2O+3___________ ↑
(3)为了检验该气体,小明选择的试剂是___________ 。
【主要原料】柠檬酸(C6H8O7)和小苏打(NaHCO3);
【使用说明】将一包“汽泡爽”粉末倒入玻璃杯中,加入200mL冷水,看到有大量气泡快速生成,待粉末完全溶解,就得到一杯果味饮料。小明观察了饮料说明后,他借助化学实验的方法,探究“汽泡爽”产生气体的成分,以及加水温度对产生气体量的影响。
(1)“汽泡爽”中的小苏打(NaHCO3)是我们生活中常见的一种酸式盐,请按照下列要求写出相关方程式:
①小苏打受热易分解:
②小苏打和盐酸的反应:
③小苏打和氢氧化钠溶液的反应:
【实验】探究“汽泡爽”产生气体的成分。
(2)小明阅读资料发现:“汽泡爽”原料中的柠檬酸(C6H8O7)和小苏打(NaHCO3)粉末混合后加水,可以发生以下反应,填写生成气体的化学式:3NaHCO3+C6H8O7=C6H5O7Na3+3H2O+3
(3)为了检验该气体,小明选择的试剂是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】砷为VA族元素,金属冶炼过程产生的含砷有毒废弃物需处理与检测。
I.冶炼废水中砷元素主要以亚砷酸(H3AsO3)形式存在,可用化学沉降法处理酸性高浓度含砷废水,其工艺流程如下:

已知:①As2S3与过量的S2-存在以下反应:As2S3(s)+3S2-(aq) 2AsS33-(aq);
2AsS33-(aq);
②亚砷酸盐的溶解性大于相应砷酸盐。
(1)亚砷酸中砷元素的化合价为________ ;砷酸的第一步电离方程式为_____________ 。
(2)“一级沉砷”中FeSO4的作用是___________ ;“二级沉砷”中H2O2与含砷物质反应的化学方程式为_____________ 。
(3)沉淀X为___________ (填化学式)。
Ⅱ.冶炼废渣中的砷元素主要以As2S3的形式存在,可用古氏试砷法半定量检测(As的 最低检出限为3.0×10-6g)。
步骤1:取10g废渣样品,粉碎后与锌粉混合,加入H2SO4共热,生成AsH3气体。
步骤2:将AsH3气体通入AgNO3溶液中,生成银镜和As2O3。
步骤3:取1g废渣样品,重复上述实验,未见银镜生成。
(4)AsH3的电子式为_______________ 。
(5)步骤2的离子方程式为_________________ 。
(6)固体废弃物的排放标准中,砷元素不得高于4.0×10-5g·kg-1,请通过计算说明该排放的废渣中砷元素的含量_______ (填“符合”、“不符合”)排放标准,原因是__________
I.冶炼废水中砷元素主要以亚砷酸(H3AsO3)形式存在,可用化学沉降法处理酸性高浓度含砷废水,其工艺流程如下:

已知:①As2S3与过量的S2-存在以下反应:As2S3(s)+3S2-(aq)
 2AsS33-(aq);
2AsS33-(aq);②亚砷酸盐的溶解性大于相应砷酸盐。
(1)亚砷酸中砷元素的化合价为
(2)“一级沉砷”中FeSO4的作用是
(3)沉淀X为
Ⅱ.冶炼废渣中的砷元素主要以As2S3的形式存在,可用古氏试砷法半定量检测(As的 最低检出限为3.0×10-6g)。
步骤1:取10g废渣样品,粉碎后与锌粉混合,加入H2SO4共热,生成AsH3气体。
步骤2:将AsH3气体通入AgNO3溶液中,生成银镜和As2O3。
步骤3:取1g废渣样品,重复上述实验,未见银镜生成。
(4)AsH3的电子式为
(5)步骤2的离子方程式为
(6)固体废弃物的排放标准中,砷元素不得高于4.0×10-5g·kg-1,请通过计算说明该排放的废渣中砷元素的含量
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】如图是某儿童微量元素体检报告单的部分数据:
根据上表的数据,回答下列问题:
(1)该儿童__ 元素含量偏低。
(2)报告单中“μmol/L”是__ (填“质量”、“体积”或“浓度”)的单位。
(3)服用维生素C可使食物中的Fe3+转化为Fe2+。在这个过程中体现维生素C的__ (填“氧化性”或“还原性”)。
(4)缺铁性贫血患者应补充Fe2+。一些补铁剂以硫酸亚铁为主要成分,用硫酸亚铁制成药片时外表包有一层特殊的糖衣,推测糖衣的作用是__ 。实验室制备氢氧化亚铁时就要用到硫酸亚铁,欲长时间观察到氢氧化亚铁白色沉淀,必须是新制的硫酸亚铁溶液和经过蒸馏的水配制的氢氧化钠溶液反应制备。反应的现象为___ ,方程式为___ 、___ 。
| 北京市医疗机构临床检验结果报告单分析项目 | ||||
| 分析项目 | 检测结果 | 单位 | 参考范围 | |
| 1 | 锌(Zn) | 115.92 | mol/L | 66~120 |
| 2 | 铁(Fe) | 6.95↓ | mol/L | 7.52~11.82 |
| 3 | 钙(Ca) | 1.68 | mol/L | 1.55~2.10 |
| …… | ||||
(1)该儿童
(2)报告单中“μmol/L”是
(3)服用维生素C可使食物中的Fe3+转化为Fe2+。在这个过程中体现维生素C的
(4)缺铁性贫血患者应补充Fe2+。一些补铁剂以硫酸亚铁为主要成分,用硫酸亚铁制成药片时外表包有一层特殊的糖衣,推测糖衣的作用是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】阅读下面两条科普信息,回答有关问题:
一个体重50kg的健康人身体中含铁2g,这2g铁在人体中不是以金属单质的形式存在,而是以Fe2+和Fe3+的形式存在。亚铁离子易被吸收,给贫血者补充铁时,应给予含亚铁离子的亚铁盐,如硫酸亚铁。服用维生素C,可使食物中的铁离子还原成亚铁离子,有利于铁的吸收:
在新生代的海水里有一种铁细菌,它们提取海水中的亚铁离子,利用酶为催化剂把它转变成它们的皮鞘(可以用Fe2O3来表示其中的铁),后来便沉积下来形成铁矿:该反应的另一种反应物是CO2,反应后CO2转变成有机物(用甲醛CH2O表示)。
(1)这两则科普信息分别介绍了人体内和海水中的亚铁离子与铁离子(或者铁的高价化合物)相互转化的事实、方法和途径。这说明维生素C具有______ 性,铁离子具有_______ 性,第二则则信息中CO2是_________ 剂。
(2)铁酸钠(Na2FeO4)是水处理过程中使用的一种新型净水剂,它的氧化性比高锰酸钾更强,本身在反应中被还原为Fe3+离子。制取铁酸钠的化学方程式如下:
__ Fe(NO3)3 +__ NaOH+ __ Cl2 → __ Na2FeO4+ __ NaNO3 + __ NaCl + __ H2O
①配平上述反应,并分析_______ 元素被氧化,当生成3mol还原产物时,转移电子的总数为______ ;
②铁酸钠除了能消毒外,还可以用于净水,原因是_____________________ 。
一个体重50kg的健康人身体中含铁2g,这2g铁在人体中不是以金属单质的形式存在,而是以Fe2+和Fe3+的形式存在。亚铁离子易被吸收,给贫血者补充铁时,应给予含亚铁离子的亚铁盐,如硫酸亚铁。服用维生素C,可使食物中的铁离子还原成亚铁离子,有利于铁的吸收:
在新生代的海水里有一种铁细菌,它们提取海水中的亚铁离子,利用酶为催化剂把它转变成它们的皮鞘(可以用Fe2O3来表示其中的铁),后来便沉积下来形成铁矿:该反应的另一种反应物是CO2,反应后CO2转变成有机物(用甲醛CH2O表示)。
(1)这两则科普信息分别介绍了人体内和海水中的亚铁离子与铁离子(或者铁的高价化合物)相互转化的事实、方法和途径。这说明维生素C具有
(2)铁酸钠(Na2FeO4)是水处理过程中使用的一种新型净水剂,它的氧化性比高锰酸钾更强,本身在反应中被还原为Fe3+离子。制取铁酸钠的化学方程式如下:
①配平上述反应,并分析
②铁酸钠除了能消毒外,还可以用于净水,原因是
您最近一年使用:0次



