室温下,某同学进行 与
与 反应的探究实验,回答下列问题。
反应的探究实验,回答下列问题。
(1)用如图装置制备纯净的 。
。

丙装置中盛放无水 的仪器名称是
的仪器名称是_______ ,乙装置中溶液的作用是_________ 。
(2)按照如图装置进行实验(夹持装置略)。
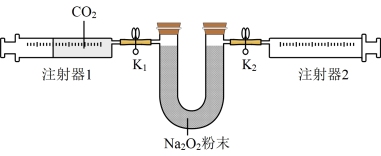
①先组装仪器,然后________ 。再用注射器1抽取 纯净的
纯净的 ,将其连接在
,将其连接在 处,注射器2的活塞推到底后连接在
处,注射器2的活塞推到底后连接在 处,具支U形管中装入足量的
处,具支U形管中装入足量的 粉末。
粉末。
②打开弹簧夹 向右推动注射器1的活塞,可观察到的现象是
向右推动注射器1的活塞,可观察到的现象是_______ 。
③实验过程中,需缓慢推入 ,反应的化学方程式为
,反应的化学方程式为_______ 。
 与
与 反应的探究实验,回答下列问题。
反应的探究实验,回答下列问题。(1)用如图装置制备纯净的
 。
。
丙装置中盛放无水
 的仪器名称是
的仪器名称是(2)按照如图装置进行实验(夹持装置略)。

①先组装仪器,然后
 纯净的
纯净的 ,将其连接在
,将其连接在 处,注射器2的活塞推到底后连接在
处,注射器2的活塞推到底后连接在 处,具支U形管中装入足量的
处,具支U形管中装入足量的 粉末。
粉末。②打开弹簧夹
 向右推动注射器1的活塞,可观察到的现象是
向右推动注射器1的活塞,可观察到的现象是③实验过程中,需缓慢推入
 ,反应的化学方程式为
,反应的化学方程式为
更新时间:2022-08-17 00:55:40
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】钠及其化合物学习与探究:
I.某课外活动小组设计了下列装置,验证 跟
跟 反应时需要与水接触。
反应时需要与水接触。

(1)①中反应的离子方程式是_______ 。
(2)装置②中的试剂是_______ (填序号),装置③中的试剂是_______ (填序号)。
a.饱和 溶液 b.饱和
溶液 b.饱和 溶液 c.浓
溶液 c.浓
Ⅱ.取 碳酸氢钠样品(含有不与盐酸反应的杂质)放入烧杯中,称得烧杯及所盛样品的总质量为
碳酸氢钠样品(含有不与盐酸反应的杂质)放入烧杯中,称得烧杯及所盛样品的总质量为 ,再把
,再把 稀盐酸平均分成四份依次加入样品中,每次均充分反应。实验数据记录如下(忽略氯化氢和水蒸气的挥发):
稀盐酸平均分成四份依次加入样品中,每次均充分反应。实验数据记录如下(忽略氯化氢和水蒸气的挥发):
(3)第一次加入稀盐酸充分反应后,生成二氧化碳的质量是_______ g。
(4)请你据此计算碳酸氢钠的质量分数_______ 。
I.某课外活动小组设计了下列装置,验证
 跟
跟 反应时需要与水接触。
反应时需要与水接触。
(1)①中反应的离子方程式是
(2)装置②中的试剂是
a.饱和
 溶液 b.饱和
溶液 b.饱和 溶液 c.浓
溶液 c.浓
Ⅱ.取
 碳酸氢钠样品(含有不与盐酸反应的杂质)放入烧杯中,称得烧杯及所盛样品的总质量为
碳酸氢钠样品(含有不与盐酸反应的杂质)放入烧杯中,称得烧杯及所盛样品的总质量为 ,再把
,再把 稀盐酸平均分成四份依次加入样品中,每次均充分反应。实验数据记录如下(忽略氯化氢和水蒸气的挥发):
稀盐酸平均分成四份依次加入样品中,每次均充分反应。实验数据记录如下(忽略氯化氢和水蒸气的挥发):| 所加盐酸的次数 | 第一次 | 第二次 | 第三次 | 第四次 |
| 盐酸的质量/g | 25 | 25 | 25 | 25 |
| 烧杯及所盛物质总质量/g | 181.2 | 204.4 | 228.6 | 253.6 |
(4)请你据此计算碳酸氢钠的质量分数
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】有A、B、C、D、E、F六种物质,它们的相互转化关系如下图(反应条件略)。已知A和B是单质,B、E、F 在常温下为气体,C为淡黄色粉末。
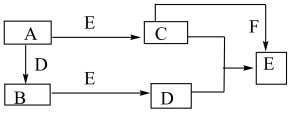
试回答:
(1)写出A、B、的化学式:A__________ ; B__________ 。
(2)写出C和D反应生成E 的化学方程式:_____________________________________ 。
(3)写出C和F反应生成E 的化学方程式:_____________________________________ 。
(4)写出C物质的电子式___________________ ,F的结构式 _____________________ 。
(5)用电子式表示D的形成过程:_______________________________ 。

试回答:
(1)写出A、B、的化学式:A
(2)写出C和D反应生成E 的化学方程式:
(3)写出C和F反应生成E 的化学方程式:
(4)写出C物质的电子式
(5)用电子式表示D的形成过程:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】在潜水艇中可用过氧化钠作为供氧剂。请选择适当的化学试剂和实验用品,用下图中的实验装置(C中盛放的是过氧化钠)进行实验,证明过氧化钠可作供氧剂。

(1)B中盛有饱和NaHCO3溶液,其作用是___________ 。
(2)写出过氧化钠与二氧化碳反应的化学方程式___________ 。
(3)D中盛放的试剂是___________ ,其目的是___________ 。
(4)试管F中收集到的气体是___________ ,如何验证?___________ 。

(1)B中盛有饱和NaHCO3溶液,其作用是
(2)写出过氧化钠与二氧化碳反应的化学方程式
(3)D中盛放的试剂是
(4)试管F中收集到的气体是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】实验室可用下列几组试剂制取少量NH3;
①固体 和
和 ;②浓氨水和固体
;②浓氨水和固体 ;③浓氨水。
;③浓氨水。
请回答下列问题:
(1)用上述三组试剂制取少量NH3,需要加热的是_______ (填序号),第②组试剂中产生NH3的化学方程式可表示为_______ 。
(2)下面的制取装置图1中,方法①应选用装置_______ (填“A”或“B”)

(3)在制取后,如果要干燥氨气,应选用的干燥剂是_______ (多选)
A.浓硫酸 B.固体氢氧化钠 C.五氧化二磷 D.碱石灰 E.固体CaO F.无水CaCl2
(4)检验集气瓶中是否收集满氨气的方法_______ 。
(5)为防止环境污染,以下装置如图2(盛放的液体为水)可用于吸收多余NH3的是_______ (填序号)。

①固体
 和
和 ;②浓氨水和固体
;②浓氨水和固体 ;③浓氨水。
;③浓氨水。请回答下列问题:
(1)用上述三组试剂制取少量NH3,需要加热的是
(2)下面的制取装置图1中,方法①应选用装置

(3)在制取后,如果要干燥氨气,应选用的干燥剂是
A.浓硫酸 B.固体氢氧化钠 C.五氧化二磷 D.碱石灰 E.固体CaO F.无水CaCl2
(4)检验集气瓶中是否收集满氨气的方法
(5)为防止环境污染,以下装置如图2(盛放的液体为水)可用于吸收多余NH3的是

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】实验室用下列装置制取并收集氯气,试回答下列问题:

①装置B的作用是__________
②若用含有 的浓盐酸与足量的
的浓盐酸与足量的 反应制取
反应制取 ,制得的
,制得的 体积(标准状况下)总是小于1.12L的原因是
体积(标准状况下)总是小于1.12L的原因是________ 。(不考虑盐酸的挥发)

①装置B的作用是
②若用含有
 的浓盐酸与足量的
的浓盐酸与足量的 反应制取
反应制取 ,制得的
,制得的 体积(标准状况下)总是小于1.12L的原因是
体积(标准状况下)总是小于1.12L的原因是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】工业上制 ,第二步为
,第二步为 的催化氧化,为测定该可逆反应中
的催化氧化,为测定该可逆反应中 的转化率,现模拟设计如下,请回答下列问题:
的转化率,现模拟设计如下,请回答下列问题:

(1)实验室制 的原理是
的原理是___________ (书写化学方程式)
(2)若 的制备装置与
的制备装置与 相同,则制取原理是
相同,则制取原理是___________ (书写化学方程式)
(3)B试剂瓶用于测定 的物质的量,则B中盛装的试剂是
的物质的量,则B中盛装的试剂是___________
A. 溶液 B.
溶液 B. 溶液 C.
溶液 C. 溶液
溶液
若B中产生的白色沉淀的质量为4.66克,且从B装置逸出的 的物质的量为
的物质的量为 。则催化氧化的过程中
。则催化氧化的过程中 的转化率为
的转化率为___________
(4)在 的密闭容器中分别充入
的密闭容器中分别充入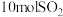 和
和 后达到平衡状态,此时测定
后达到平衡状态,此时测定 的物质的量为
的物质的量为 ,则用
,则用 表示该反应的化学反应速率
表示该反应的化学反应速率
___________ ,达到平衡时容器内的压强与反应前的压强之比是___________
 ,第二步为
,第二步为 的催化氧化,为测定该可逆反应中
的催化氧化,为测定该可逆反应中 的转化率,现模拟设计如下,请回答下列问题:
的转化率,现模拟设计如下,请回答下列问题:
(1)实验室制
 的原理是
的原理是(2)若
 的制备装置与
的制备装置与 相同,则制取原理是
相同,则制取原理是(3)B试剂瓶用于测定
 的物质的量,则B中盛装的试剂是
的物质的量,则B中盛装的试剂是A.
 溶液 B.
溶液 B. 溶液 C.
溶液 C. 溶液
溶液若B中产生的白色沉淀的质量为4.66克,且从B装置逸出的
 的物质的量为
的物质的量为 。则催化氧化的过程中
。则催化氧化的过程中 的转化率为
的转化率为(4)在
 的密闭容器中分别充入
的密闭容器中分别充入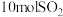 和
和 后达到平衡状态,此时测定
后达到平衡状态,此时测定 的物质的量为
的物质的量为 ,则用
,则用 表示该反应的化学反应速率
表示该反应的化学反应速率
您最近一年使用:0次
【推荐1】实验小组制备高铁酸钾 并探究其性质。
并探究其性质。
资料: 为紫色固体,微溶于
为紫色固体,微溶于 溶液;具有强氧化性,在酸性或中性溶液中快速产生
溶液;具有强氧化性,在酸性或中性溶液中快速产生 ,在0~5℃碱性溶液中较稳定。
,在0~5℃碱性溶液中较稳定。
(1)制备 (夹持装置略)
(夹持装置略)
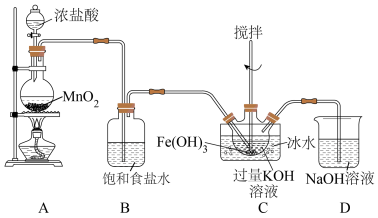
①装置A中反应的化学方程式是__________ 。
②B的作用是__________ 。
③C中得到紫色固体和溶液。C中 发生的反应有:
发生的反应有: ,还有:
,还有:__________ 。(用化学方程式表示)
(2)探究 的性质
的性质
①取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有 。为证明是否
。为证明是否 氧化了
氧化了 而产生
而产生 ,设计以下方案:
,设计以下方案:
ⅰ.由方案Ⅰ中溶液变红可知a中含有__________ 离子,但该离子的产生不能判断一定是 将
将 氧化,还可能由
氧化,还可能由__________ 反应产生(用离子方程式表示)。
ⅱ.方案Ⅱ可证明 氧化了
氧化了 。用
。用 溶液洗涤的目的是
溶液洗涤的目的是__________ 。
②根据 的制备实验得出:氧化性
的制备实验得出:氧化性
__________  (填“>”或“<”),而方案Ⅱ实验表明,
(填“>”或“<”),而方案Ⅱ实验表明, 和
和 的氧化性强弱关系相反,原因是
的氧化性强弱关系相反,原因是__________ 。
③资料表明,酸性溶液中的氧化性 ,验证实验如下:将溶液b滴入
,验证实验如下:将溶液b滴入 和足量
和足量 的混合溶液中,振荡后溶液呈浅紫色。该现象能否证明氧化性
的混合溶液中,振荡后溶液呈浅紫色。该现象能否证明氧化性 。若能,请说明理由;若不能,进一步设计实验方案。理由或方案:
。若能,请说明理由;若不能,进一步设计实验方案。理由或方案:__________ 。
 并探究其性质。
并探究其性质。资料:
 为紫色固体,微溶于
为紫色固体,微溶于 溶液;具有强氧化性,在酸性或中性溶液中快速产生
溶液;具有强氧化性,在酸性或中性溶液中快速产生 ,在0~5℃碱性溶液中较稳定。
,在0~5℃碱性溶液中较稳定。(1)制备
 (夹持装置略)
(夹持装置略)
①装置A中反应的化学方程式是
②B的作用是
③C中得到紫色固体和溶液。C中
 发生的反应有:
发生的反应有: ,还有:
,还有:(2)探究
 的性质
的性质①取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有
 。为证明是否
。为证明是否 氧化了
氧化了 而产生
而产生 ,设计以下方案:
,设计以下方案:方案Ⅰ | 取少量a,滴加 溶液至过量,溶液呈红色 溶液至过量,溶液呈红色 |
方案Ⅱ | 用 溶液充分洗涤C中所得固体,再用 溶液充分洗涤C中所得固体,再用 溶液将 溶液将 溶出,得到紫色溶液b。取少量b,滴加盐酸,有 溶出,得到紫色溶液b。取少量b,滴加盐酸,有 产生 产生 |
 将
将 氧化,还可能由
氧化,还可能由ⅱ.方案Ⅱ可证明
 氧化了
氧化了 。用
。用 溶液洗涤的目的是
溶液洗涤的目的是②根据
 的制备实验得出:氧化性
的制备实验得出:氧化性
 (填“>”或“<”),而方案Ⅱ实验表明,
(填“>”或“<”),而方案Ⅱ实验表明, 和
和 的氧化性强弱关系相反,原因是
的氧化性强弱关系相反,原因是③资料表明,酸性溶液中的氧化性
 ,验证实验如下:将溶液b滴入
,验证实验如下:将溶液b滴入 和足量
和足量 的混合溶液中,振荡后溶液呈浅紫色。该现象能否证明氧化性
的混合溶液中,振荡后溶液呈浅紫色。该现象能否证明氧化性 。若能,请说明理由;若不能,进一步设计实验方案。理由或方案:
。若能,请说明理由;若不能,进一步设计实验方案。理由或方案:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】已知:溴单质(Br2)、化合物与氯的性质相似,溴单质的水溶液呈黄色,溴单质的四氯化碳溶液呈橙红色。在足量的稀氯化亚铁溶液中,加入1~2滴液态溴单质,振荡后溶液变为黄色。
(1)甲同学认为这不是发生化学反应所致,使溶液变黄色的物质是___ (填化学式,下同);乙同学认为这是发生化学反应所致,使溶液变黄色的物质是___ 。
(2)现提供如下试剂:
A.酸性高锰酸钾溶液 B.氢氧化钠溶液 C.四氯化碳 D.硫氰化钾溶液
实验证明乙同学的推断是正确的,请用三种方法加以验证,写出选用的试剂编号及实验中观察到的现象:
(3)根据上述实验推测,若在稀溴化亚铁溶液中通入氯气,首先被氧化的离子是_____ 。
(1)甲同学认为这不是发生化学反应所致,使溶液变黄色的物质是
(2)现提供如下试剂:
A.酸性高锰酸钾溶液 B.氢氧化钠溶液 C.四氯化碳 D.硫氰化钾溶液
实验证明乙同学的推断是正确的,请用三种方法加以验证,写出选用的试剂编号及实验中观察到的现象:
| 选用试剂(代号) | 实验现象 | |
| 第一种方法 | ||
| 第二种方法 | ||
| 第三种方法 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】某校化学小组学生利用下图所列装置进行“铁与水反应”的实验,并利用产物进一步制取FeCl3·6H2O晶体。(图中夹持及尾气处理装置均已略去)
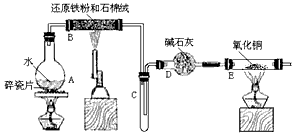
(1)装置B中发生反应的化学方程式是__________________ 。
(2)装置E中的现象是_______________________ 。
(3)停止反应,待B管冷却后,取其中的固体,加入过量稀盐酸充分反应,过滤。简述检验滤液中Fe3+的操作方法:________________________ 。
(4)该小组学生利用上述滤液制取FeCl3·6H2O晶体,设计流程如下:
滤液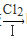 FeCl3溶液
FeCl3溶液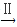 FeCl3·6H2O晶体
FeCl3·6H2O晶体
①步骤Ⅰ中通入Cl2的作用是_________________ 。
②该流程中需保持盐酸过量,主要原因是(结合离子方程式简要说明)_________ 。

(1)装置B中发生反应的化学方程式是
(2)装置E中的现象是
(3)停止反应,待B管冷却后,取其中的固体,加入过量稀盐酸充分反应,过滤。简述检验滤液中Fe3+的操作方法:
(4)该小组学生利用上述滤液制取FeCl3·6H2O晶体,设计流程如下:
滤液
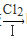 FeCl3溶液
FeCl3溶液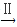 FeCl3·6H2O晶体
FeCl3·6H2O晶体①步骤Ⅰ中通入Cl2的作用是
②该流程中需保持盐酸过量,主要原因是(结合离子方程式简要说明)
您最近一年使用:0次



