下列叙述正确的是
①在基态多电子原子中,p轨道电子的能量一定高于s轨道电子的能量
② 晶体的晶胞是面心立方结构
晶体的晶胞是面心立方结构
③As是第ⅤA族的一个元素,其外围电子排布式为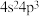 ,属于p区元素
,属于p区元素
④熔融状态的 不能导电,
不能导电, 的稀溶液有弱的导电能力且可作手术刀的消毒液,从不同角度分类
的稀溶液有弱的导电能力且可作手术刀的消毒液,从不同角度分类 是一种共价化合物、非电解质、盐、分子晶体
是一种共价化合物、非电解质、盐、分子晶体
①在基态多电子原子中,p轨道电子的能量一定高于s轨道电子的能量
②
 晶体的晶胞是面心立方结构
晶体的晶胞是面心立方结构③As是第ⅤA族的一个元素,其外围电子排布式为
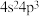 ,属于p区元素
,属于p区元素④熔融状态的
 不能导电,
不能导电, 的稀溶液有弱的导电能力且可作手术刀的消毒液,从不同角度分类
的稀溶液有弱的导电能力且可作手术刀的消毒液,从不同角度分类 是一种共价化合物、非电解质、盐、分子晶体
是一种共价化合物、非电解质、盐、分子晶体| A.①② | B.②③ | C.①③ | D.②④ |
更新时间:2022-08-28 20:49:35
|
相似题推荐
【推荐1】下列说法不正确的是
| A.CO2分子的空间构型为直线型 | B.铝原子的2s与3s轨道皆为球形分布 |
| C.Co2+的价电子排布式为3d54s2 | D.钠元素的I2大于镁元素的I2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】以下对核外电子运动状况的描述正确的是( )
| A.同一原子中,2p,3p,4p能级的轨道依次增多,均为哑铃状 |
B.当碳原子的核外电子排布由 转变为 转变为 时,这一过程中释放能量 时,这一过程中释放能量 |
| C.3p2表示3p能级有两个轨道 |
| D.在同一能级上运动的电子,其运动状态完全相同 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】氮化铬的晶胞结构如图所示, 点分数坐标为
点分数坐标为 。氮化铬的晶体密度为
。氮化铬的晶体密度为 ,摩尔质量为
,摩尔质量为 ,晶胞参数为
,晶胞参数为 ,
, 代表阿伏加德罗常数的值。下列说法正确的是
代表阿伏加德罗常数的值。下列说法正确的是
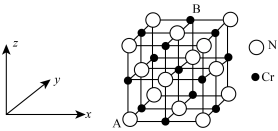
 点分数坐标为
点分数坐标为 。氮化铬的晶体密度为
。氮化铬的晶体密度为 ,摩尔质量为
,摩尔质量为 ,晶胞参数为
,晶胞参数为 ,
, 代表阿伏加德罗常数的值。下列说法正确的是
代表阿伏加德罗常数的值。下列说法正确的是
A.铬原子的价电子排布图为: | B. 点的分数坐标为 点的分数坐标为 |
C.距离 原子最近的 原子最近的 原子有8个 原子有8个 | D. |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列关于晶体的叙述不正确的是
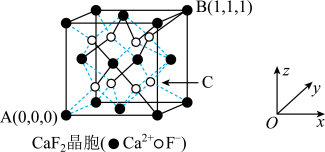
A.CaF2的晶胞结构如图,C点的坐标为( , , , , ) ) |
| B.氯化钠晶体中,每个Na+周围紧邻6个Cl- |
| C.氯化铯晶体中,每个Cs+周围紧邻8个Cl- |
| D.1个干冰晶胞中含有4个二氧化碳分子 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列是典型晶体的结构示意图,从①到⑥对应正确的是


| A.CsCl 金刚石 CaF2 Cu CO2 Fe |
| B.CaF2 SiC 金刚石 Cu CO2 CsCl |
| C.NaCl 单质硅 CaF2 Au CO2 K |
| D.NaCl BN Au CaF2 CO2 Na |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列关于物质的结构与性质的说法正确的是
| A.熔点:MgBr2<SiCl4<BN |
| B.冰和干冰均为分子晶体,冰的沸点、密度都高于干冰 |
| C.第ⅤA族元素的几种气态氢化物中,NH3是稳定性最高的氢化物 |
| D.同周期ⅦA族元素的氧化物对应水化物的酸性一定强于ⅥA族 |
您最近一年使用:0次

 原子掺杂到晶体中得到稀磁性半导体材料的结构如图乙所示,砷化镓的晶胞参数为
原子掺杂到晶体中得到稀磁性半导体材料的结构如图乙所示,砷化镓的晶胞参数为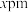 。阿伏加德罗常数的值为
。阿伏加德罗常数的值为

 原子和
原子和 原子的最近距离是
原子的最近距离是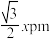
 砷化镓中配位键的数目是
砷化镓中配位键的数目是

 周围距离最近的
周围距离最近的 晶体中,每个晶胞平均占有4个
晶体中,每个晶胞平均占有4个 ,
, 的配位数是4
的配位数是4 最近且等距的
最近且等距的 有6个,距
有6个,距

