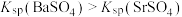V(钒)能形成多种不同颜色的离子,其转化关系如图所示(注:图中所加试剂均足量),下列说法正确的是

| A.图中转化关系只有部分存在电子转移 |
| B.由图中转化可知,I-比Zn还原性强 |
C.可加入氧化剂实现 溶液由黄色转化为蓝色 溶液由黄色转化为蓝色 |
D.V(钒)有 、 、 、 、 、 、 等多种化合价 等多种化合价 |
更新时间:2022-09-02 07:17:04
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列实验操作,现象与结论匹配的是
| 选项 | 操作 | 现象 | 结论 |
| A | 将缠绕铜丝灼烧后反复插入盛乙醇的试管,然后滴入酸性高锰酸钾溶液 | 酸性高锰酸钾溶液褪色 | 乙醇催化氧化生成乙醛 |
| B | 将装有NO2的平衡球放入热水中 | 颜色加深 | 2NO2(g) N2O4(g)ΔH>0 N2O4(g)ΔH>0 |
| C | 向含0.1mol的FeI2溶液中通入0.1molCl2,再滴加淀粉溶液 | 溶液变蓝色 | 还原性:I->Fe2+ |
| D | 向碳酸钠溶液中加入稀硫酸,反应产生的气体通入苯酚钠溶液中 | 溶液变浑浊 | 酸性:碳酸>苯酚 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
【推荐2】向CuSO4溶液中逐滴加入碘化钾溶液至过量,观察到产生白色沉淀CuI,蓝色溶液变棕色,再向反应后的溶液中通入过量SO2,溶液变无色。则下列说法正确的是
| A.通入22.4L SO2参加反应时,有2NA个电子发生转移 |
| B.通入SO2后溶液逐渐变成无色,体现了SO2的漂白性 |
| C.滴加碘化钾溶液时,KI被氧化,CuI是氧化产物 |
| D.上述实验条件下,微粒的氧化性:Cu2+>I2>SO2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
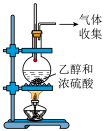
【推荐1】某实验小组用如图所示装置制备高铁酸钾(K2FeO4)并探究其性质。已知:K2FeO4为紫色固体,微溶于KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生O2,在碱性溶液中较稳定。制取实验完成后,取C中紫色溶液,加入稀盐酸,产生气体。下列说法不正确的是
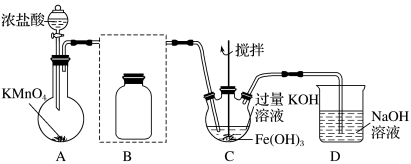

| A.B瓶应盛放饱和食盐水除去Cl2中混有的HCl |
| B.C瓶中KOH过量更有利于高铁酸钾的生成 |
| C.加盐酸产生气体可说明氧化性:K2FeO4>Cl2 |
| D.高铁酸钾是集氧化、吸附、絮凝、沉淀、灭菌、消毒等特点为一体的优良的水处理剂 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列反应的离子方程式正确的是
A.漂白粉失效的原理: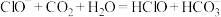 |
B.向酸性高锰酸钾溶液中加入过氧化氢,紫色变浅: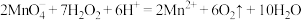 |
C.向 溶液中滴加稀硫酸,溶液变浑浊: 溶液中滴加稀硫酸,溶液变浑浊: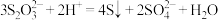 |
D.硫单质溶于强碱: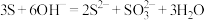 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列离子方程式书写正确的是
A.氧化亚铁与稀硫酸反应: |
B.浓硫酸与铜反应: |
C.氯化铝溶液与氨水反应: |
D.铜与稀硝酸反应: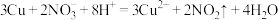 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】硫是生命代谢与发育必不可少的元素,在微生物作用下硫循环的一种途径如图所示,下列说法错误的是
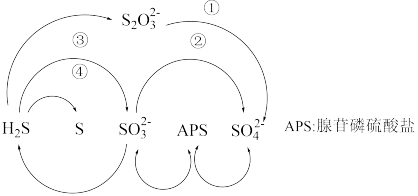
| A.自然界中存在游离态的硫 |
| B.过程①②③④均属于氧化还原反应 |
| C.S在足量的氧气中燃烧可以一步转化为SO3 |
| D.人类对化石燃料的过度开采及使用会对硫循环造成巨大影响 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】纯净物状态下电对的标准电极电势可用来比较氧化剂的氧化性强弱,现有5组标准电极电势的数据如下表所示。下列分析错误的是
| 氧化还原电对(氧化剂/还原剂) | 电极反应式 | 标准电极电势(Eϴ/V) |
| Fe3+/Fe2+ | 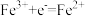 | 0.77 |
| I2/I- | 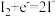 | 0.54 |
| Cl2/Cl- | 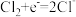 | 1.36 |
 /Mn2+ /Mn2+ |  | 1.51 |
A.氧化性: >Cl2>Fe3+>I2 >Cl2>Fe3+>I2 |
B.Fe3+能与I-发生反应,其离子方程式为: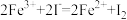 |
| C.MnO-可氧化Cl-生成Cl2 |
D.Fe3+能与Cl-反应生成Fe2+,其离子方程式为: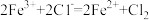 |
您最近一年使用:0次

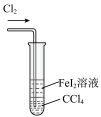
 、
、 、
、 的氧化性强弱
的氧化性强弱
 溶液的滴定管排气泡
溶液的滴定管排气泡
 、C等
、C等