工业上用磷铁渣(主要含FeP、Fe2P,以及少量Fe2O3、SiO2等杂质)制备FePO4(磷酸铁)。
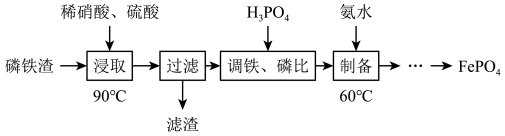
已知:FePO4难溶于水,能溶于无机强酸。
(1)“浸取”时为加速溶解,可以采取的措施有_____ (任写一种):加入硫酸的目的是_____ ;滤渣的主要成分是_____ 。
(2)“浸取”时Fe2P发生反应的离子方程式为______ 。
(3)“制备”过程中溶液的pH对磷酸铁产品中铁和磷的含量及n(Fe)/n(P)比值的影响如图所示[考虑到微量金属杂质,在pH=1时,n(Fe)/n(P)为0.973最接近理论值]。
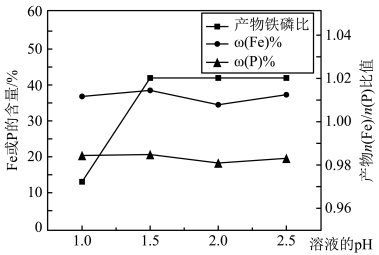
在pH范围为1~1.5时,随pH增大,n(Fe)/n(P)明显增大,其原因是_______ 。
(4)工业上也可以用电解磷铁渣的方法制备FePO4。
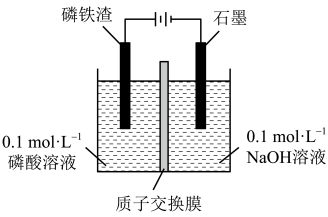
①FeP在阳极放电的电极反应式为_______ 。
②常温电解一段时间,测得溶液中Fe3+浓度约为0.32mol∙L-1,为了避免生成Fe(OH)3沉淀,应控制溶液的pH不大于_______ (已知:Ksp[Fe(OH)3]=4×10-38,lg2=0.3)。

已知:FePO4难溶于水,能溶于无机强酸。
(1)“浸取”时为加速溶解,可以采取的措施有
(2)“浸取”时Fe2P发生反应的离子方程式为
(3)“制备”过程中溶液的pH对磷酸铁产品中铁和磷的含量及n(Fe)/n(P)比值的影响如图所示[考虑到微量金属杂质,在pH=1时,n(Fe)/n(P)为0.973最接近理论值]。

在pH范围为1~1.5时,随pH增大,n(Fe)/n(P)明显增大,其原因是
(4)工业上也可以用电解磷铁渣的方法制备FePO4。

①FeP在阳极放电的电极反应式为
②常温电解一段时间,测得溶液中Fe3+浓度约为0.32mol∙L-1,为了避免生成Fe(OH)3沉淀,应控制溶液的pH不大于
更新时间:2022-04-12 22:47:54
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】工业上设计将VOSO4中的K2SO4、SiO2杂质除去并回收得到V2O5的流程如下:

请回答下列问题:
(1)步骤①所得废渣的成分是____________ 写化学式),操作I的名称______ 。
(2)步骤②、③的变化过程可简化为(下式R表示VO2+,HA表示有机萃取剂):
R2(SO4)n(水层)+ 2nHA(有机层) 2RAn(有机层) + nH2SO4 (水层)
2RAn(有机层) + nH2SO4 (水层)
②中萃取时必须加入适量碱,其原因是____________________________ 。
③中X试剂为___________________ 。
(3)⑤的离子方程式为________________________ 。
(4)25℃时,取样进行试验分析,得到钒沉淀率和溶液pH之间关系如下表:
结合上表,在实际生产中,⑤中加入氨水,调节溶液的最佳pH为__________ ;
若钒沉淀率为93.1%时不产生Fe(OH)3沉淀,则溶液中c(Fe3+)<_____________ 。
(已知:25℃时,Ksp[Fe(OH)3]=2.6×10-39)
(5)该工艺流程中,可以循环利用的物质有______________ 和_______ 。

请回答下列问题:
(1)步骤①所得废渣的成分是
(2)步骤②、③的变化过程可简化为(下式R表示VO2+,HA表示有机萃取剂):
R2(SO4)n(水层)+ 2nHA(有机层)
 2RAn(有机层) + nH2SO4 (水层)
2RAn(有机层) + nH2SO4 (水层)②中萃取时必须加入适量碱,其原因是
③中X试剂为
(3)⑤的离子方程式为
(4)25℃时,取样进行试验分析,得到钒沉淀率和溶液pH之间关系如下表:
| pH | 1.3 | 1.4 | 1.5 | 1.6 | 1.7 | 1.8 | 1.9 | 2.0 | 2.1 |
| 钒沉淀率% | 88.1 | 94.8 | 96.5 | 98.0 | 98.8 | 98.8 | 96.4 | 93.1 | 89.3 |
结合上表,在实际生产中,⑤中加入氨水,调节溶液的最佳pH为
若钒沉淀率为93.1%时不产生Fe(OH)3沉淀,则溶液中c(Fe3+)<
(已知:25℃时,Ksp[Fe(OH)3]=2.6×10-39)
(5)该工艺流程中,可以循环利用的物质有
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】我国是少数几个拥有石煤资源的国家之一,工业上以伴生钒的石煤(主要成分为V2O3,含少量P2O5、SiO2等杂质)为原料制备钒的主要流程如图:
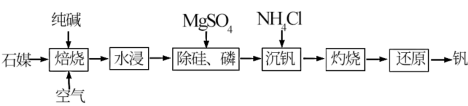
已知:①NH4VO3难溶于水。
②Ksp(MgSiO3)=2.4×10-5,Ksp[Mg3(PO4)2]=2.7×10-27。
请问答下列问题:
(1)焙烧:通入空气的条件下,向石煤中加纯碱焙烧,将V2O3转化为NaVO3的化学方程式为___ 。
(2)除硅、磷。用MgSO4溶液除硅、磷时,Si、P会形成MgSiO3、Mg3(PO4)2沉淀。若沉淀后溶液中c(PO )=1.0×10-8mol/L,则c(SiO
)=1.0×10-8mol/L,则c(SiO )=
)=___ 。随着温度升高,除磷率会显著下降,原因一是温度升高,Mg3(PO4)2溶解度增大;二是___ 。
(3)沉钒。该操作产生的滤液中,两种主要的溶质阴离子是___ (写符号);检验该滤液中两种阴离子方法是___ 。
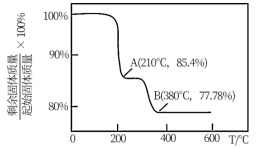
(4)灼烧。在灼烧NH4VO3的过程中,固体残留率随温度变化的曲线如图所示,则0℃~210℃,发生反应的化学方程式为___ 。
(5)还原。在高温真空条件下,用过量焦炭还原V2O5可以生成钒单质,该反应的化学方程式为___ 。

已知:①NH4VO3难溶于水。
②Ksp(MgSiO3)=2.4×10-5,Ksp[Mg3(PO4)2]=2.7×10-27。
请问答下列问题:
(1)焙烧:通入空气的条件下,向石煤中加纯碱焙烧,将V2O3转化为NaVO3的化学方程式为
(2)除硅、磷。用MgSO4溶液除硅、磷时,Si、P会形成MgSiO3、Mg3(PO4)2沉淀。若沉淀后溶液中c(PO
 )=1.0×10-8mol/L,则c(SiO
)=1.0×10-8mol/L,则c(SiO )=
)=(3)沉钒。该操作产生的滤液中,两种主要的溶质阴离子是
(4)灼烧。在灼烧NH4VO3的过程中,固体残留率随温度变化的曲线如图所示,则0℃~210℃,发生反应的化学方程式为

(5)还原。在高温真空条件下,用过量焦炭还原V2O5可以生成钒单质,该反应的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】钼酸钠晶体( )用于制造生物碱、油墨、化肥、钼红颜料等,也可用于制造阻燃剂和无公害型冷却水系统的金属缓蚀剂。如图所示是利用钼精矿(要成分为
)用于制造生物碱、油墨、化肥、钼红颜料等,也可用于制造阻燃剂和无公害型冷却水系统的金属缓蚀剂。如图所示是利用钼精矿(要成分为 ,含少量PbS等)原料生产钼酸钠晶体的工艺流程图。
,含少量PbS等)原料生产钼酸钠晶体的工艺流程图。

(1) 中Mo的化合价为
中Mo的化合价为___________
(2)“焙烧”时,有 生成,反应的化学方程式为
生成,反应的化学方程式为___________ ,氧化产物是___________
(3)“碱浸”生成 和另外一种物质,
和另外一种物质, 的电子式为
的电子式为___________ ,另外一种生成物的化学式为___________
(4)若“除重金属离子”时加入的沉淀剂为 ,则废渣的成分为
,则废渣的成分为___________ (填化学式)
(5)测得“除重金属离子”中部分离子的浓度: “结晶”前应先除去
“结晶”前应先除去 ,方法是加入
,方法是加入 固体。假设加入
固体。假设加入 固体后溶液体积不变,当
固体后溶液体积不变,当 开始沉淀时,去除的
开始沉淀时,去除的 的质量分数为
的质量分数为___________ %。(保留小数点后一位数字)[已知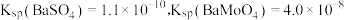 ]
]
(6)在碱性条件下,将钼精矿加入NaClO溶液中,也可以制备钼酸钠。该反应的离子方程式为___________ 。
 )用于制造生物碱、油墨、化肥、钼红颜料等,也可用于制造阻燃剂和无公害型冷却水系统的金属缓蚀剂。如图所示是利用钼精矿(要成分为
)用于制造生物碱、油墨、化肥、钼红颜料等,也可用于制造阻燃剂和无公害型冷却水系统的金属缓蚀剂。如图所示是利用钼精矿(要成分为 ,含少量PbS等)原料生产钼酸钠晶体的工艺流程图。
,含少量PbS等)原料生产钼酸钠晶体的工艺流程图。
(1)
 中Mo的化合价为
中Mo的化合价为(2)“焙烧”时,有
 生成,反应的化学方程式为
生成,反应的化学方程式为(3)“碱浸”生成
 和另外一种物质,
和另外一种物质, 的电子式为
的电子式为(4)若“除重金属离子”时加入的沉淀剂为
 ,则废渣的成分为
,则废渣的成分为(5)测得“除重金属离子”中部分离子的浓度:
 “结晶”前应先除去
“结晶”前应先除去 ,方法是加入
,方法是加入 固体。假设加入
固体。假设加入 固体后溶液体积不变,当
固体后溶液体积不变,当 开始沉淀时,去除的
开始沉淀时,去除的 的质量分数为
的质量分数为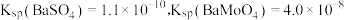 ]
](6)在碱性条件下,将钼精矿加入NaClO溶液中,也可以制备钼酸钠。该反应的离子方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】某化学兴趣小组按照如下流程进行“由镁铝合金制备硫酸铝晶体”的实验。

(1)向镁铝合金中加NaOH溶液反应的离子方程式为_________________________________________ ,金属X的原子结构示意图为__________________ ,固体A的化学式为________ 。
(2)写出硫酸铝在水中的电离方程式:_____________________________________ ;操作②包含的步骤有蒸发浓缩、________ 、过滤、洗涤、干燥。
(3)该兴趣小组为测定镁铝合金中各组分的质量分数,设计如图装置,则需要测定的数据有_______________________ 、__________________ 。


(1)向镁铝合金中加NaOH溶液反应的离子方程式为
(2)写出硫酸铝在水中的电离方程式:
(3)该兴趣小组为测定镁铝合金中各组分的质量分数,设计如图装置,则需要测定的数据有

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】正丁醚是一种用途很广的化工产品,毒性和危险性小,是安全性很高的有机溶剂,对许多天然及合成油脂、树脂、橡胶、有机酸酯、生物碱等都有很强的溶解能力,还可作为电子级清洗剂和多种有机合成材料。可通过以下反应原理制取正丁醚: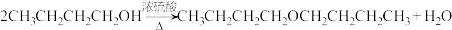
已知相关物质的部分信息如下:
某课外化学学习小组查阅相关资料设计了以下实验步骤合成正丁醚:
①在100 mL两口烧瓶中加入30.0 mL正丁醇、5.0 mL浓硫酸和几粒沸石,充分摇匀。在分水器中加入3.0 mL饱和食盐水,按图甲组装仪器,接通冷凝水;
②反应:在电热套上加热,使瓶内液体微沸,回流反应约1小时;
③精制:将馏出液倒入盛有10 mL水的分液漏斗中,充分振摇,静置弃去水液,有机层依次用5 mL水,3 mL 5% NaOH溶液、3 mL水和3 mL饱和氯化钙溶液洗涤,分去水层,将产物放入洁净干燥的小锥形瓶中,然后加入0.2~0.4 g无水氯化钙,再将液体转入装置丙中,再加几粒沸石进行蒸馏,收集到馏分9.0 mL。

请根据以上操作回答下列问题:
(1)仪器d的名称是___________ 。
(2)步骤②在电热套上加热,应控制好温度使瓶内液体微沸,切不可温度过高,导致副反应发生,产生还原性气体___________ (填化学式)。
(3)步骤①分水器中加入饱和食盐水的目的是___________ 。
(4)使用分水器不断分离出水的目的是___________ ;如何判断反应已经完成?当___________ 时,表明反应完成,即可停止实验。
(5)在步骤③蒸馏时发现忘记添加沸石,正确的处理办法是___________ 。
(6)在步骤②中采用电热套加热而不采用酒精灯直接加热的原因可能是___________ 、___________ 。
(7)本小组实验后所得正丁醚的产率约为___________ %(计算结果保留一位小数)。
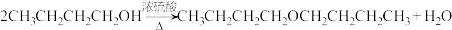
已知相关物质的部分信息如下:
| 沸点(℃) | 密度( ) ) | 溶解度(g) | 相对分子质量 | |
| 正丁醇 | 117.7 | 0.81 | 7.9 | 74 |
| 正丁醚 | 142 | 0.77 | 微溶于水 | 130 |
①在100 mL两口烧瓶中加入30.0 mL正丁醇、5.0 mL浓硫酸和几粒沸石,充分摇匀。在分水器中加入3.0 mL饱和食盐水,按图甲组装仪器,接通冷凝水;
②反应:在电热套上加热,使瓶内液体微沸,回流反应约1小时;
③精制:将馏出液倒入盛有10 mL水的分液漏斗中,充分振摇,静置弃去水液,有机层依次用5 mL水,3 mL 5% NaOH溶液、3 mL水和3 mL饱和氯化钙溶液洗涤,分去水层,将产物放入洁净干燥的小锥形瓶中,然后加入0.2~0.4 g无水氯化钙,再将液体转入装置丙中,再加几粒沸石进行蒸馏,收集到馏分9.0 mL。

请根据以上操作回答下列问题:
(1)仪器d的名称是
(2)步骤②在电热套上加热,应控制好温度使瓶内液体微沸,切不可温度过高,导致副反应发生,产生还原性气体
(3)步骤①分水器中加入饱和食盐水的目的是
(4)使用分水器不断分离出水的目的是
(5)在步骤③蒸馏时发现忘记添加沸石,正确的处理办法是
(6)在步骤②中采用电热套加热而不采用酒精灯直接加热的原因可能是
(7)本小组实验后所得正丁醚的产率约为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】聚阴离子Na2FePO4F多用于锂离子电池正极材料,一种工艺简单、绿色经济的合成流程如下:
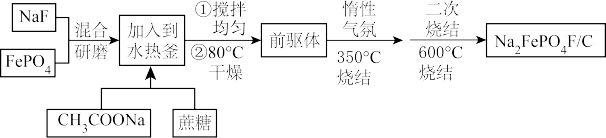
首先将含有NaF和FePO4各0.025mol的原料研磨混合30min,混合均匀转移到80mL。的水热釜中,将0.025mol的CH3COONa溶于6mL蒸馏水中,并加入1g蔗糖溶解均匀并慢慢加入水热釜中得到流变态混合物,请回答下列问题:
(1)80°C干燥的加热方式:_______ 。
(2)前驱体主要成分是NaF、FePO4、CH3COONa和蔗糖四种物质的混合物。此段操作的目的是_______ 。
(3)加入的NaF、FePO4、CH3COONa物质的量之比为1:1:1的目的是_______ 。
(4)350℃烧结主要是蔗糖碳化,产生的碳粒包裹在生成的纳米级Na2FePO4F的表面,碳层的作用是_______ 。
(5)二次烧结中有NaF、FePO4、CH3COONa反应生成Na2FePO4F、CO、水及焦炭,试写出该反应的化学方程式:_______ 。
(6)假定原料完全反应,最后称量黑色粉末Na2FePO4F/C共5.63g,则产品中Na2FePO4F含量为_______ (保留三位有效数字)。

首先将含有NaF和FePO4各0.025mol的原料研磨混合30min,混合均匀转移到80mL。的水热釜中,将0.025mol的CH3COONa溶于6mL蒸馏水中,并加入1g蔗糖溶解均匀并慢慢加入水热釜中得到流变态混合物,请回答下列问题:
(1)80°C干燥的加热方式:
(2)前驱体主要成分是NaF、FePO4、CH3COONa和蔗糖四种物质的混合物。此段操作的目的是
(3)加入的NaF、FePO4、CH3COONa物质的量之比为1:1:1的目的是
(4)350℃烧结主要是蔗糖碳化,产生的碳粒包裹在生成的纳米级Na2FePO4F的表面,碳层的作用是
(5)二次烧结中有NaF、FePO4、CH3COONa反应生成Na2FePO4F、CO、水及焦炭,试写出该反应的化学方程式:
(6)假定原料完全反应,最后称量黑色粉末Na2FePO4F/C共5.63g,则产品中Na2FePO4F含量为
您最近一年使用:0次



