为探究氯气与KI溶液的反应,某课外小组用如图装置进行实验(夹持仪器已略去,气密性已检验),装置A中发生反应的化学方程式为MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O。
MnCl2+Cl2↑+2H2O。
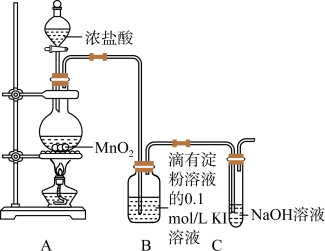
(1)装置A中生成氯气的离子反应方程式为_____ 。
(2)装置C中NaOH的作用是____ 。
(3)能证明氯气的氧化性强于碘的实验现象是____ 。
(4)为探究B中溶液颜色变化的原因,小组同学查阅资料并进行实验。
查阅资料:I2和I-在溶液中会发生反应:I2+I-= ,
, 显棕黄色且遇淀粉变蓝;I2可被氯气氧化为
显棕黄色且遇淀粉变蓝;I2可被氯气氧化为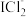 (红色)和
(红色)和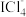 (黄色),两种离子可继续被氧化成
(黄色),两种离子可继续被氧化成 (无色)。
(无色)。
进行实验:
①操作I的实验目的是___ 。
②写出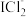 在水溶液中与氯气反应生成
在水溶液中与氯气反应生成 的离子方程式
的离子方程式____ 。
③由以上实验可推断B中溶液颜色变成浅棕色的原因是____ 。
 MnCl2+Cl2↑+2H2O。
MnCl2+Cl2↑+2H2O。
| 实验操作 | 实验现象 |
| 打开A中分液漏斗活塞,放下部分浓盐酸,加热 | 装置B中溶液变蓝色,随后蓝色褪去,溶液显浅棕色 |
(1)装置A中生成氯气的离子反应方程式为
(2)装置C中NaOH的作用是
(3)能证明氯气的氧化性强于碘的实验现象是
(4)为探究B中溶液颜色变化的原因,小组同学查阅资料并进行实验。
查阅资料:I2和I-在溶液中会发生反应:I2+I-=
 ,
, 显棕黄色且遇淀粉变蓝;I2可被氯气氧化为
显棕黄色且遇淀粉变蓝;I2可被氯气氧化为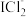 (红色)和
(红色)和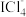 (黄色),两种离子可继续被氧化成
(黄色),两种离子可继续被氧化成 (无色)。
(无色)。进行实验:
| 实验操作 | 实验现象 |
| I.取反应后B中的溶液4mL分成两等份,第一份滴入1滴碘水;第二份滴入1滴淀粉溶液 | 第一份溶液变蓝色 第二份溶液颜色没有变化 |
| II.将I2溶于KI溶液中配制得碘总浓度为0.1mol/L的溶液,取上述溶液2mL,滴加1滴淀粉溶液,再通入氯气 | 加淀粉后溶液变蓝,通氯气后蓝色褪去,溶液显浅棕色 |
| III.向II所得溶液继续通入氯气 | 溶液几乎变为无色 |
②写出
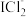 在水溶液中与氯气反应生成
在水溶液中与氯气反应生成 的离子方程式
的离子方程式③由以上实验可推断B中溶液颜色变成浅棕色的原因是
22-23高一上·全国·课时练习 查看更多[2]
(已下线)2.2.2 氯气与金属、非金属及还原性化合物的反应-2022-2023学年高一化学上学期课后培优分级练(人教版2019必修第一册)(已下线)专题05 氯及其化合物【考题猜想】(10大题型)-2023-2024学年高一化学上学期期中考点大串讲(人教版2019必修第一册)
更新时间:2022-09-10 22:01:06
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】无水四氯化锡(SnCl4)可用于制作导电玻璃,导电玻璃广泛用于液晶显示屏、薄膜太阳能电池基底等。可用如下装置制备四氯化锡(部分夹持装置已略去)。

有关信息如下表:
回答下列问题:
(1)对比分液漏斗,装置甲中恒压滴液漏斗的优点是___________________________ 。
仪器A中发生反应的离子方程式为_______________________________________ 。
(2)将装置如图连接好,检查气密性,慢慢滴入浓盐酸,待观察到__________ (填现象)后,开始加热丁装置。锡熔化后适当增大氯气流量并继续加热丁装置。继续加热丁装置的目的是促进氯气与锡反应和_________________________________ 。
(3)如果缺少乙装置可能产生的后果是_______________________________________ 。
(4)戊装置中球形冷凝管的冷水进口为______ (填“a”或“b”)。
(5)己装置中碱石灰的作用是_______________________________________________ 。
(6)碘氧化法滴定分析产品中Sn(II)的含量。准确称取m g产品于锥形瓶中,用适量浓盐酸溶解,淀粉溶液做指示剂,用c mol·L–1碘标准溶液滴定。滴入最后一滴标准溶液,出现__________ 时达到滴定终点,此时消耗碘标准溶液V mL,则产品中Sn(II)的质量分数为____________ (用字母表示)。

有关信息如下表:
化学式 | SnCl2 | SnCl4 |
熔点/℃ | 246 | −33 |
沸点/℃ | 652 | 144 |
其他性质 | 无色晶体,Sn(II)易被氧化为Sn(IV) | 无色液体,易水解 |
回答下列问题:
(1)对比分液漏斗,装置甲中恒压滴液漏斗的优点是
仪器A中发生反应的离子方程式为
(2)将装置如图连接好,检查气密性,慢慢滴入浓盐酸,待观察到
(3)如果缺少乙装置可能产生的后果是
(4)戊装置中球形冷凝管的冷水进口为
(5)己装置中碱石灰的作用是
(6)碘氧化法滴定分析产品中Sn(II)的含量。准确称取m g产品于锥形瓶中,用适量浓盐酸溶解,淀粉溶液做指示剂,用c mol·L–1碘标准溶液滴定。滴入最后一滴标准溶液,出现
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
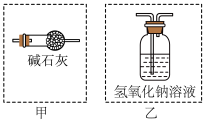
【推荐2】某兴趣小组用下图的装置制取ICl,并用ICl的冰醋酸溶液来测定某油脂的不饱和度。油脂的不饱和度是指一个油脂分子最多可加成的氢分子数。
已知:①ICl的熔点为13.9℃,沸点为97.4℃,化学性质与氯气相似易水解;
② ,ICl3的熔点为111℃。
,ICl3的熔点为111℃。
(1)写出第一个装置中发生反应的化学方程式:___________ 。
(2)虚线框内应选用的装置是___________ (填“甲”或“乙”)。___________ (用接口的字母表示)。
(4)下列有关说法正确的是___________。
(5)用ICl的冰醋酸溶液测定某油脂的不饱和度,进行如下实验,实验过程中有关反应为:
将含有0.05mol某油脂的样品溶于CCl4后形成100mL溶液;从中取出10mL,加入20mL含有IC1物质的量为n mol的冰醋酸溶液(过量);充分反应后,加入足量KI溶液;生成的碘单质用a 的
的 标准溶液滴定;重复上述实验两次,测得滴定所需Na2S2O3的平均值为V mL。
标准溶液滴定;重复上述实验两次,测得滴定所需Na2S2O3的平均值为V mL。
①滴定前,需要将装有标准液的滴定管中的气泡排尽,应选择图中___________ 。___________ (用含a、n、V的表达式表示)。
已知:①ICl的熔点为13.9℃,沸点为97.4℃,化学性质与氯气相似易水解;
②
 ,ICl3的熔点为111℃。
,ICl3的熔点为111℃。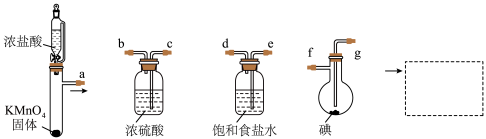
(1)写出第一个装置中发生反应的化学方程式:
(2)虚线框内应选用的装置是
(4)下列有关说法正确的是___________。
| A.上述实验装置中的KMnO4固体也可用MnO2代替 |
| B.恒压滴液漏斗使用时应打开上面的玻璃塞 |
C.ICl与NaOH溶液反应的方程式为: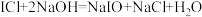 |
| D.若所制得的ICl中溶有少量ICl3杂质,可以采用蒸馏法进行提纯 |
(5)用ICl的冰醋酸溶液测定某油脂的不饱和度,进行如下实验,实验过程中有关反应为:
① ;②
;② ;③
;③
将含有0.05mol某油脂的样品溶于CCl4后形成100mL溶液;从中取出10mL,加入20mL含有IC1物质的量为n mol的冰醋酸溶液(过量);充分反应后,加入足量KI溶液;生成的碘单质用a
 的
的 标准溶液滴定;重复上述实验两次,测得滴定所需Na2S2O3的平均值为V mL。
标准溶液滴定;重复上述实验两次,测得滴定所需Na2S2O3的平均值为V mL。①滴定前,需要将装有标准液的滴定管中的气泡排尽,应选择图中
A. B.
B.  C.
C.  D.
D.
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】实验室用MnO2与浓盐酸制取和收集纯净干燥的氯气的实验装置如图所示:
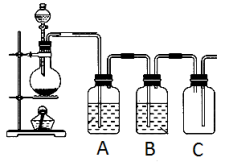
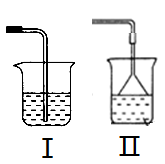
(1)实验室制取Cl2的化学方程式_____________ 。
(2)反应前,MnO2盛放______ 中(填写仪器名称)。
(3)装置A中所装试剂是_______ ,目的________ 。装置B中所装的试剂是______ 。
(4)该实验装置除缺少尾气吸收装置,明显有错误的装置是____ (选填“A”、“B”、“C”)。
(5)装置I、II中作为尾气吸收装置实验效果更好的是_______ ,发生反应的化学方程式为_________ 。


(1)实验室制取Cl2的化学方程式
(2)反应前,MnO2盛放
(3)装置A中所装试剂是
(4)该实验装置除缺少尾气吸收装置,明显有错误的装置是
(5)装置I、II中作为尾气吸收装置实验效果更好的是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】某化学小组利用如图装置制备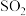 并探究其性质。
并探究其性质。
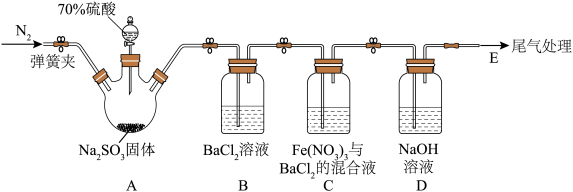
回答下列问题:
(1)盛放 固体的仪器名称为
固体的仪器名称为___________ 。
(2)实验前,检查装置气密性的方法为按图示连接好装置,___________ 。
(3)实验时,观察到装置B中无明显现象,装置C中有白色沉淀生成,据此推测装置C中白色沉淀的成分为___________ (填化学式)。该小组同学猜想产生该物质的原因可能有两种:
i. 氧化了
氧化了
ⅱ.___________
(4)为了验证猜想,小组同学进行了以下实验:
①为了验证猜想i,小组同学取少量装置B中反应后的溶液置于试管中,向其中滴加 溶液,产生了白色沉淀,写出该反应的离子方程式:
溶液,产生了白色沉淀,写出该反应的离子方程式:___________ 。
②为了验证猜想ⅱ,小组同学取少量装置B中反应后的溶液置于试管中,向其中滴加 溶液,也产生了白色沉淀,写出该反应的离子方程式:
溶液,也产生了白色沉淀,写出该反应的离子方程式:___________ 。
③据此小组同学认为猜想i和ⅱ均正确,为进一步检验装置中是否有猜想i的反应发生,还需要向反应后的装置C溶液中滴加___________ 进行验证。
 并探究其性质。
并探究其性质。
回答下列问题:
(1)盛放
 固体的仪器名称为
固体的仪器名称为(2)实验前,检查装置气密性的方法为按图示连接好装置,
(3)实验时,观察到装置B中无明显现象,装置C中有白色沉淀生成,据此推测装置C中白色沉淀的成分为
i.
 氧化了
氧化了
ⅱ.
(4)为了验证猜想,小组同学进行了以下实验:
①为了验证猜想i,小组同学取少量装置B中反应后的溶液置于试管中,向其中滴加
 溶液,产生了白色沉淀,写出该反应的离子方程式:
溶液,产生了白色沉淀,写出该反应的离子方程式:②为了验证猜想ⅱ,小组同学取少量装置B中反应后的溶液置于试管中,向其中滴加
 溶液,也产生了白色沉淀,写出该反应的离子方程式:
溶液,也产生了白色沉淀,写出该反应的离子方程式:③据此小组同学认为猜想i和ⅱ均正确,为进一步检验装置中是否有猜想i的反应发生,还需要向反应后的装置C溶液中滴加
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】某化学小组以铜为阳极、石墨为阴极,研究在不同的电解质溶液中铜被氧化的价态及产物。实验装置如图所示(电源装置略去)。

资料:i.Cu2O为砖红色,CuCl为白色,CuOH为黄色且易分解
ii.[Cu(NH3)2]+为无色,在空气中易被氧化为深蓝色[Cu(NH3)4]2+
iii.25 ℃时,Ksp(CuCl)=1.2×10-6,Ksp(CuOH)= 1.2×10-14
实验记录如下:
(1)I中铜电极的电极反应式是___________ 。
(2)II中沉淀由黄色变为砖红色的化学方程式是___________ 。
(3)将III中所得白色沉淀过滤,充分洗涤,进行下列实验,证实该沉淀为CuCl。

①证明III中所得白色沉淀中有Cu+的证据是___________ 。
②步骤iii的操作是___________ 。
(4)III中下端白色沉淀最终变为砖红色的原因是:白色沉淀为CuCl,___________ ,CuOH不稳定易分解为砖红色的Cu2O。
(5)IV中Cu未被氧化的原因是________ 。
(6)综上,铜被氧化的价态及产物与________ 有关。

资料:i.Cu2O为砖红色,CuCl为白色,CuOH为黄色且易分解
ii.[Cu(NH3)2]+为无色,在空气中易被氧化为深蓝色[Cu(NH3)4]2+
iii.25 ℃时,Ksp(CuCl)=1.2×10-6,Ksp(CuOH)= 1.2×10-14
实验记录如下:
| 实验 | 电解质溶液(3 mol/L) | 现象 | |
| 铜电极附近 | 石墨电极 | ||
| I | H2SO4 | 溶液变蓝 | 产生无色气泡,一段时间后有少量红色金属析出 |
| II | NaOH | 出现黄色浑浊,很快变为砖红色 | 产生无色气泡 |
| III | NaCl | 出现白色浑浊,浑浊向下扩散,一段时间后,下端白色沉淀变黄,最终为砖红色 | 产生无色气泡 |
| IV | KI | 迅速产生棕褐色的物质,滴入1 滴淀粉溶液, 立即变为蓝色;取出铜电极洗净检验,无变化 | 产生无色气泡 |
(2)II中沉淀由黄色变为砖红色的化学方程式是
(3)将III中所得白色沉淀过滤,充分洗涤,进行下列实验,证实该沉淀为CuCl。

①证明III中所得白色沉淀中有Cu+的证据是
②步骤iii的操作是
(4)III中下端白色沉淀最终变为砖红色的原因是:白色沉淀为CuCl,
(5)IV中Cu未被氧化的原因是
(6)综上,铜被氧化的价态及产物与
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】乙酰基二茂铁是橘红色固体,熔点为81℃,沸点为163℃,常用作火箭燃料的添加剂。由二茂铁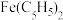 合成乙酰基二茂铁
合成乙酰基二茂铁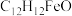 的原理如下图所示。已知乙酸酐
的原理如下图所示。已知乙酸酐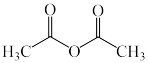 易水解。
易水解。
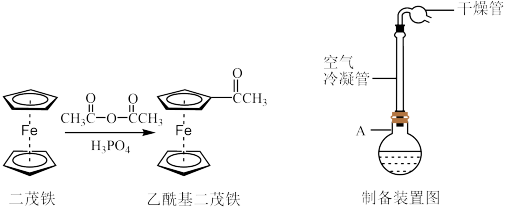
实验步骤如下:
步骤①:称取0.1g(0.00054mol)二茂铁,放入仪器A中,加入2mL(0.02mol)新蒸的乙酸酐,放入磁子,并装上空气冷凝管和干燥管,在60~75℃水浴中用磁力搅拌器搅拌溶解(见制备装置图,部分仪器已略去)后,迅速加入6~8滴浓磷酸,使反应液呈深红色,在室温下再搅拌60min。
步骤②:将反应液转入盛有约5g冰的烧杯中,用冷水刷洗反应瓶并将刷洗液并入烧杯中。滴加 氢氧化钠水溶液至pH为7~8.此时有大量橘红色固体析出。冷却后抽滤,并用少量冷水洗涤2次。在小于60°C红外灯下烘干后,刮下粗产物。
氢氧化钠水溶液至pH为7~8.此时有大量橘红色固体析出。冷却后抽滤,并用少量冷水洗涤2次。在小于60°C红外灯下烘干后,刮下粗产物。
(1)仪器A的名称为_____ ;
(2)装有无水氯化钙干燥管的作用是_____ ;
(3)步骤②中用pH试纸测定溶液的pH的操作是_____ ;用碳酸氢钠替换氢氧化钠中和产物时不需测定溶液的pH,观察到_____ ,可作为中和反应完成的判断标准;固体碳酸氢钠需分批加入,原因是_____ ;
(4)红外灯的温度不宜过高的原因是_____ ,提纯乙酰基二茂铁粗品的方法是_____ ,提纯后得到乙酰基二茂铁0.037g,本实验的产率是_____ (保留两位有效数字);
(5)二茂铁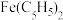 由两个环戊二烯负离子与亚铁离子结合而成,已知分子中的大
由两个环戊二烯负离子与亚铁离子结合而成,已知分子中的大 键可用符号
键可用符号 表示,其中m代表参与形成大
表示,其中m代表参与形成大 键的原子数,n代表参与形成大
键的原子数,n代表参与形成大 键的电子数(如苯分子中的大
键的电子数(如苯分子中的大 键可表示为
键可表示为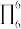 ),则
),则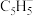 中的大
中的大 键应表示为
键应表示为_____ ,已知二乙酰基二茂铁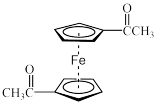 只有一种结构(由于乙酰基的致钝作用,使两个乙酰基不在一个环上),
只有一种结构(由于乙酰基的致钝作用,使两个乙酰基不在一个环上),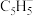 能否绕着与金属键合的轴转动?
能否绕着与金属键合的轴转动?_____ (填“能”或“否”)。
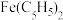 合成乙酰基二茂铁
合成乙酰基二茂铁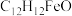 的原理如下图所示。已知乙酸酐
的原理如下图所示。已知乙酸酐 易水解。
易水解。
实验步骤如下:
步骤①:称取0.1g(0.00054mol)二茂铁,放入仪器A中,加入2mL(0.02mol)新蒸的乙酸酐,放入磁子,并装上空气冷凝管和干燥管,在60~75℃水浴中用磁力搅拌器搅拌溶解(见制备装置图,部分仪器已略去)后,迅速加入6~8滴浓磷酸,使反应液呈深红色,在室温下再搅拌60min。
步骤②:将反应液转入盛有约5g冰的烧杯中,用冷水刷洗反应瓶并将刷洗液并入烧杯中。滴加
 氢氧化钠水溶液至pH为7~8.此时有大量橘红色固体析出。冷却后抽滤,并用少量冷水洗涤2次。在小于60°C红外灯下烘干后,刮下粗产物。
氢氧化钠水溶液至pH为7~8.此时有大量橘红色固体析出。冷却后抽滤,并用少量冷水洗涤2次。在小于60°C红外灯下烘干后,刮下粗产物。(1)仪器A的名称为
(2)装有无水氯化钙干燥管的作用是
(3)步骤②中用pH试纸测定溶液的pH的操作是
(4)红外灯的温度不宜过高的原因是
(5)二茂铁
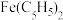 由两个环戊二烯负离子与亚铁离子结合而成,已知分子中的大
由两个环戊二烯负离子与亚铁离子结合而成,已知分子中的大 键可用符号
键可用符号 表示,其中m代表参与形成大
表示,其中m代表参与形成大 键的原子数,n代表参与形成大
键的原子数,n代表参与形成大 键的电子数(如苯分子中的大
键的电子数(如苯分子中的大 键可表示为
键可表示为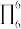 ),则
),则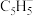 中的大
中的大 键应表示为
键应表示为 只有一种结构(由于乙酰基的致钝作用,使两个乙酰基不在一个环上),
只有一种结构(由于乙酰基的致钝作用,使两个乙酰基不在一个环上),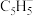 能否绕着与金属键合的轴转动?
能否绕着与金属键合的轴转动?
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】以Mg和不同盐溶液间的反应为实验对象,探究Mg与盐溶液反应的多样性。
(1)对实验Ⅰ进行研究:
①推测实验Ⅰ中黑色固体为Ag,则发生反应的离子方程式为___________ 。
②确认黑色固体为Ag的实验方案是___________ 。
(2)对实验Ⅱ进行研究:
①反应开始时产生H2的原因可能是:
ⅰ.___________ 。
ⅱ.Mg和NH 直接反应。
直接反应。
②“一段时间后”产生的气体一定含有___________ 。
③为进一步研究NH4Cl溶液的作用,设计如下实验:
结合实验Ⅱ、Ⅳ、Ⅴ可以得出的结论是___________ 。
(3)对实验Ⅲ进行研究:
①推测在pH=8.2的该溶液中,若无HCO ,则H+和Mg反应的程度很小。通过实验证实了该推测,其方案是
,则H+和Mg反应的程度很小。通过实验证实了该推测,其方案是___________ 。
②经检验,白色晶体为碱式碳酸镁[Mg2(OH)2CO3],结合化学用语并根据化学平衡移动原理,分析其产生的原因:___________ ;
(4)根据上述实验判断,影响Mg与盐溶液反应多样性的原因有:
ⅰ.盐溶液中阳离子氧化性的相对强弱;
ⅱ.盐溶液中阴离子的催化作用;
ⅲ:___________ 。
| 实验 | 向试管中加2mL溶液 | 实验现象 |
 | 实验Ⅰ:0.1 mol/L AgNO3溶液 | 镁条表面迅速覆盖一层疏松黑色固体,并有少量气泡产生 |
| 实验Ⅱ:2.0 mol/L NH4Cl溶液 | 反应开始时产生大量气体(经检验其中含有H2),一段时间后产生使湿润的红色石蕊试纸变蓝的气体 | |
| 实验Ⅲ:pH=8.2 NaHCO3溶液 | 产生大量气体(经检验其中含有H2和CO2)和白色晶体 |
①推测实验Ⅰ中黑色固体为Ag,则发生反应的离子方程式为
②确认黑色固体为Ag的实验方案是
(2)对实验Ⅱ进行研究:
①反应开始时产生H2的原因可能是:
ⅰ.
ⅱ.Mg和NH
 直接反应。
直接反应。②“一段时间后”产生的气体一定含有
③为进一步研究NH4Cl溶液的作用,设计如下实验:
| 实验 | 操作 | 现象 |
| 实验Ⅳ | 用1mol/L(NH4)2SO4溶液重复实验Ⅱ | 产生气体的速率慢于实验Ⅱ |
| 实验Ⅴ | 用2mol/L(NH4)2SO4溶液重复实验Ⅱ | 产生气体的速率与实验Ⅱ相当 |
(3)对实验Ⅲ进行研究:
①推测在pH=8.2的该溶液中,若无HCO
 ,则H+和Mg反应的程度很小。通过实验证实了该推测,其方案是
,则H+和Mg反应的程度很小。通过实验证实了该推测,其方案是②经检验,白色晶体为碱式碳酸镁[Mg2(OH)2CO3],结合化学用语并根据化学平衡移动原理,分析其产生的原因:
(4)根据上述实验判断,影响Mg与盐溶液反应多样性的原因有:
ⅰ.盐溶液中阳离子氧化性的相对强弱;
ⅱ.盐溶液中阴离子的催化作用;
ⅲ:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】两位同学各自设计了一个实验,检验试样中是否含有 。
。
甲同学的实验过程:

乙同学的实验过程:

(1)甲同学认为自己检验出 ,发生反应的离子方程式为
,发生反应的离子方程式为___________ ;结合学过的知识,你认为所得白色沉淀___________ (填“一定”、或“不一定”)是硫酸钡,判断理由是___________ ,可能发生反应的离子方程式___________ 。
(2)若你是乙同学,方案中选择试剂Ⅰ为___________ ,现象Ⅰ___________ ;试剂Ⅱ___________ ,现象Ⅱ___________ 。
 。
。甲同学的实验过程:

乙同学的实验过程:

(1)甲同学认为自己检验出
 ,发生反应的离子方程式为
,发生反应的离子方程式为(2)若你是乙同学,方案中选择试剂Ⅰ为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】向盛有10mL饱和氯化铁溶液的试管里投入足量铝片,观察到如下现象:
①黄色溶液很快变成红褐色,过一会儿溶液中有红褐色沉淀生成。
②铝片表面立刻有少量黑色物质析出,黑色物质能被磁铁吸起。
③混合液温度升高甚至发烫,产生无色气泡,且产生气泡速率明显加快,铝片上下翻滚。
(1)产生的红褐色沉淀是____________________ ,无色气泡的成分是____________________ 。
(2)产生无色气泡的原因是(用离子方程式表示)____________________ 。
(3)写出生成气泡速率明显加快的两个原因____________________ 、____________________ 。
①黄色溶液很快变成红褐色,过一会儿溶液中有红褐色沉淀生成。
②铝片表面立刻有少量黑色物质析出,黑色物质能被磁铁吸起。
③混合液温度升高甚至发烫,产生无色气泡,且产生气泡速率明显加快,铝片上下翻滚。
(1)产生的红褐色沉淀是
(2)产生无色气泡的原因是(用离子方程式表示)
(3)写出生成气泡速率明显加快的两个原因
您最近一年使用:0次



