N2O和CO可在催化剂 (Pt2O+)表面转化为无害气体,其反应原理为: 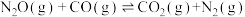 ,下列有关该反应说法正确的是
,下列有关该反应说法正确的是
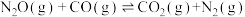 ,下列有关该反应说法正确的是
,下列有关该反应说法正确的是| A.催化剂能改变反应的∆H |
| B.通入过量CO,可使N2O转化率达100% |
| C.保持温度和容器体积不变,通入He增大压强,反应速率不变 |
| D.保持温度和压强不变,通入He反应速率不变 |
更新时间:2022-09-17 11:02:46
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】将除去氧化膜的镁条放入少量稀盐酸中进行实验,测得氢气的产生速率(v)随时间(t)的变化情况如图所示,下列说法中不正确的是
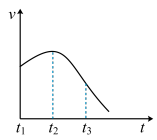
| A.镁条与稀盐酸反应的方程式:Mg + 2H+ = Mg2+ + H2↑ |
| B.t1→t2速率变化的主要原因是镁与酸的反应是放热反应,体系温度升高 |
| C.t2→t3速率变化的主要原因是随着反应的进行c(H+)下降 |
| D.t2→t3速率变化的主要原因是随着反应的进行温度逐渐降低 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列各项实验基本操作中,正确的是
| A.在做中和滴定实验时用蒸馏水清洗锥形瓶后,直接开始滴定实验 |
| B.为了加快锌和硫酸反应的速率,可将稀硫酸改为浓硫酸 |
| C.为了加快过滤速度,用玻璃棒搅拌漏斗中的液体 |
| D.蒸干AlCl3溶液制无水AlCl3固体 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】NO2与N2O4能相互转化,热化学方程式为
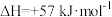 ,下列有关说法正确的是
,下列有关说法正确的是

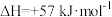 ,下列有关说法正确的是
,下列有关说法正确的是| A.降低体系温度逆反应速率减小,正反应速率增大 |
| B.若容器体积不变,气体颜色不变时说明该反应未建立化学平衡 |
C.其他条件不变,向平衡后的容器中再加入少量N2O4,新平衡 的值不变 的值不变 |
| D.减小体系的压强能降低N2O4的反应速率和转化率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
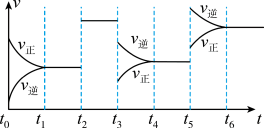
【推荐2】某密闭容器中发生如下反应:X(g)+3Y(g) 2Z(g);ΔH<0。下图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量。下列说法中错误的是
2Z(g);ΔH<0。下图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量。下列说法中错误的是
 2Z(g);ΔH<0。下图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量。下列说法中错误的是
2Z(g);ΔH<0。下图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量。下列说法中错误的是
| A.t2时加入了催化剂 |
| B.t3时减小反应物浓度 |
| C.t3时降低压强 |
| D.t5时升高温度 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】CO与 在铁催化剂表面进行如下两步反应:
在铁催化剂表面进行如下两步反应:
第一步: (慢)
(慢)
第二步: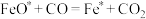 (快)
(快)
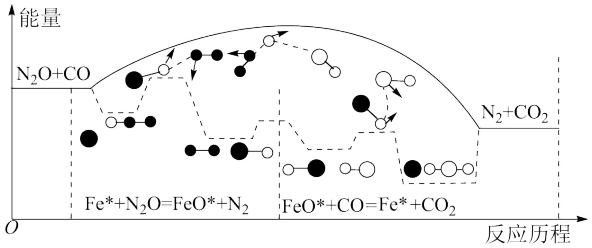
其相对能量与反应历程如下图所示,下列说法错误的是
 在铁催化剂表面进行如下两步反应:
在铁催化剂表面进行如下两步反应:第一步:
 (慢)
(慢) 第二步:
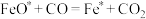 (快)
(快)其相对能量与反应历程如下图所示,下列说法错误的是

| A.在整个反应历程中,有极性键的断裂和生成 |
| B.总反应的反应速率由第一步反应决定 |
| C.两步反应均为放热反应 |
| D. FeO*和Fe *均为反应的催化剂 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】某小组拟用酸性 溶液与
溶液与 溶液的反应来探究“条件对化学反应速率的影响”(已知:
溶液的反应来探究“条件对化学反应速率的影响”(已知: ),设计了如下实验方案并记录实验结果。
),设计了如下实验方案并记录实验结果。
下列说法错误的是
 溶液与
溶液与 溶液的反应来探究“条件对化学反应速率的影响”(已知:
溶液的反应来探究“条件对化学反应速率的影响”(已知: ),设计了如下实验方案并记录实验结果。
),设计了如下实验方案并记录实验结果。| 编号 | V(0.20 mol·L  溶液)/mL 溶液)/mL | V(蒸馏水)/mL | V(0.01 mol·L 酸性 酸性 溶液)/mL 溶液)/mL | 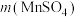 /g /g | T/℃ |
| ① | 2.0 | 0 | 4.0 | 0 | 50 |
| ② | 2.0 | 0 | 4.0 | 0 | 25 |
| ③ | 1.5 | a | 4.0 | 0 | 25 |
| ④ | 2.0 | 0 | 4.0 | 0.1 | 25 |
| A.实验①、②是探究温度对化学反应速率的影响 |
| B.实验②、④是探究催化剂对化学反应速率的影响 |
| C.若a为0.5,则实验①、③是探究浓度对化学反应速率的影响 |
| D.实验②中出现反应速率先增大后减小的现象,反应速率减小可能是反应物浓度降低造成的 |
您最近一年使用:0次

 CO(g)+H2(g)在一密闭容器中进行,下列条件的改变能加快反应速率是
CO(g)+H2(g)在一密闭容器中进行,下列条件的改变能加快反应速率是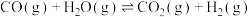 的历程如下图所示。吸附在催化剂表面上的物种用“*”表示。
的历程如下图所示。吸附在催化剂表面上的物种用“*”表示。
 、
、
 充分反应后转移电子的物质的量是2mol
充分反应后转移电子的物质的量是2mol

