废旧硬质合金刀具中含碳化钨(WC)、金属钴(Co)及少量杂质铁,利用电解法可回收WC和Co。工艺流程简图如下:
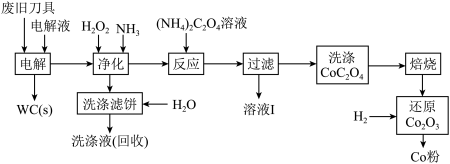
(1)电解时废旧刀具做阳极,不锈钢做阴极,HCl溶液为电解液。阴极主要的电极反应式为______ 。
(2)净化步骤所得滤饼的主要成分是______ 。回收的洗涤液代替水配制电解液,目的是回收利用其中的______ 。
(3)溶液I的主要成分是______ 。洗涤CoC2O4不充分对最终产品纯度并无明显影响,但焙烧时会造成环境污染,原因是______ 。
(4)将Co2O3还原成Co粉的化学反应方程式为______ 。

(1)电解时废旧刀具做阳极,不锈钢做阴极,HCl溶液为电解液。阴极主要的电极反应式为
(2)净化步骤所得滤饼的主要成分是
(3)溶液I的主要成分是
(4)将Co2O3还原成Co粉的化学反应方程式为
2013·山东·高考真题 查看更多[3]
四川省成都市石室天府中学2020-2021学年高二下学期5月月考化学试题(已下线)2014届高考化学二轮专题冲刺第17讲 化学与技术练习卷2013年全国普通高等学校招生统一考试理科综合能力测试化学(山东卷)
更新时间:2019-01-30 18:14:09
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】叠氮化钠( )不溶于乙醚,微溶于乙醇,易溶于水,常用于汽车安全防护袋的气源,汽车发生剧烈碰撞时,立即自动充气。实验室模拟尿素法制备水合肼(
)不溶于乙醚,微溶于乙醇,易溶于水,常用于汽车安全防护袋的气源,汽车发生剧烈碰撞时,立即自动充气。实验室模拟尿素法制备水合肼(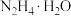 )并利用其进一步反应制取
)并利用其进一步反应制取 的流程如下:
的流程如下:
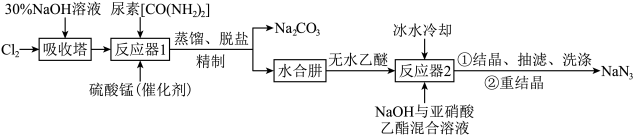
已知:①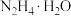 易溶于水,具有强还原性,易被氧化成N2;
易溶于水,具有强还原性,易被氧化成N2;
②一定条件下,碱性NaClO溶液与尿素溶液反应生成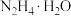

(1)写出反应器1中生成水合肼的化学方程式:___________ 。
(2)反应器2中加入无水乙醚的作用是___________ 。
(3)已知亚硝酸乙酯的结构简式为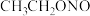 。写出反应器2中生成NaN3和
。写出反应器2中生成NaN3和 的化学方程式:
的化学方程式:________ 。若生成39gNaN3,则该反应中转移电子的物质的量为_______ 。
(4)反应器1要控制 NaClO溶液的用量,其主要目的是___________ 。
(5)某实验室设计了如图所示装置制备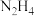 。双极膜是阴、阳复合膜,层间的
。双极膜是阴、阳复合膜,层间的 解离成OH-和H+并可分别通过阴、阳膜定向移动。
解离成OH-和H+并可分别通过阴、阳膜定向移动。
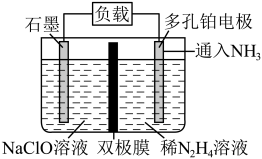
①双极膜中产生的___________ (填“H⁺”或“OH-”)移向多孔铂电极。
②石墨电极反应式为___________ 。
(6)对于反应中生成的碳酸钠,可以通过以下过程转化为亚硫酸钠。

 常用作还原性漂白剂。在测定某液体葡萄糖中
常用作还原性漂白剂。在测定某液体葡萄糖中 残留量时,取50.0mL样品,先通入足量 Cl2,再加入足量盐酸酸化的氯化钡溶液,充分反应,过滤,洗涤,干燥,称量固体质量为0.11g。通入足量Cl2发生反应的离子方程式为
残留量时,取50.0mL样品,先通入足量 Cl2,再加入足量盐酸酸化的氯化钡溶液,充分反应,过滤,洗涤,干燥,称量固体质量为0.11g。通入足量Cl2发生反应的离子方程式为___________ ,该样品中 残留量为
残留量为___________ g·L−1。(以SO2计,结果保留1位小数)
 )不溶于乙醚,微溶于乙醇,易溶于水,常用于汽车安全防护袋的气源,汽车发生剧烈碰撞时,立即自动充气。实验室模拟尿素法制备水合肼(
)不溶于乙醚,微溶于乙醇,易溶于水,常用于汽车安全防护袋的气源,汽车发生剧烈碰撞时,立即自动充气。实验室模拟尿素法制备水合肼(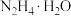 )并利用其进一步反应制取
)并利用其进一步反应制取 的流程如下:
的流程如下:
已知:①
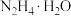 易溶于水,具有强还原性,易被氧化成N2;
易溶于水,具有强还原性,易被氧化成N2;②一定条件下,碱性NaClO溶液与尿素溶液反应生成
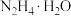

(1)写出反应器1中生成水合肼的化学方程式:
(2)反应器2中加入无水乙醚的作用是
(3)已知亚硝酸乙酯的结构简式为
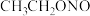 。写出反应器2中生成NaN3和
。写出反应器2中生成NaN3和 的化学方程式:
的化学方程式:(4)反应器1要控制 NaClO溶液的用量,其主要目的是
(5)某实验室设计了如图所示装置制备
 。双极膜是阴、阳复合膜,层间的
。双极膜是阴、阳复合膜,层间的 解离成OH-和H+并可分别通过阴、阳膜定向移动。
解离成OH-和H+并可分别通过阴、阳膜定向移动。
①双极膜中产生的
②石墨电极反应式为
(6)对于反应中生成的碳酸钠,可以通过以下过程转化为亚硫酸钠。

 常用作还原性漂白剂。在测定某液体葡萄糖中
常用作还原性漂白剂。在测定某液体葡萄糖中 残留量时,取50.0mL样品,先通入足量 Cl2,再加入足量盐酸酸化的氯化钡溶液,充分反应,过滤,洗涤,干燥,称量固体质量为0.11g。通入足量Cl2发生反应的离子方程式为
残留量时,取50.0mL样品,先通入足量 Cl2,再加入足量盐酸酸化的氯化钡溶液,充分反应,过滤,洗涤,干燥,称量固体质量为0.11g。通入足量Cl2发生反应的离子方程式为 残留量为
残留量为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】如图所示,A、B、C、D均为石墨电极,E、F分别为短周期相邻两种活泼金属元素中的一种单质,且E能与NaOH溶液反应,按图示接通电路,反应一段时间。
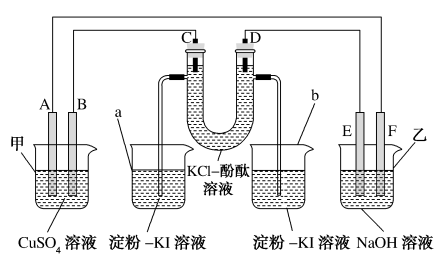
(1)电极A的名称是___________ 。
(2)C极电极反应式为___________ 。
(3)烧杯中溶液会变蓝的是___________ (填“a”或“b”)。
(4)F极的名称是___________ ,电极反应式为___________ 。
(5)甲池中总反应的离子方程式为___________ 。

(1)电极A的名称是
(2)C极电极反应式为
(3)烧杯中溶液会变蓝的是
(4)F极的名称是
(5)甲池中总反应的离子方程式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】某兴趣小组的同学用下图所示装置研究有关电化学的问题(甲、乙、丙三池中溶质足量), 当闭合该装置的电键 K 时,观察到电流计的指针发生了偏转。请回答下列问题:
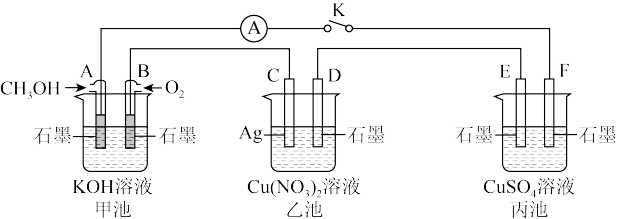
(1)乙池为_____ (填“原电池”、“电解池”或“电镀池”),B 电极的电极反应式为____ 。
(2)丙池中 E 电极为____ (填“正极”、“负极”、“阴极”或“阳极”),电极的电极反应式为____ 。该池总反应的化学方程式为____ 。
(3)当乙池中 C 极质量减轻 54 g 时,甲池中 B 电极理论上消耗 O2的为____ L(标准状况)。
(4)一段时间后,断开电键 K,下列物质能使丙池恢复到反应前浓度的是____ (填选项字母)。
A Cu B CuO C Cu(OH)2 D Cu2(OH)2CO3

(1)乙池为
(2)丙池中 E 电极为
(3)当乙池中 C 极质量减轻 54 g 时,甲池中 B 电极理论上消耗 O2的为
(4)一段时间后,断开电键 K,下列物质能使丙池恢复到反应前浓度的是
A Cu B CuO C Cu(OH)2 D Cu2(OH)2CO3
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】某种粗盐中含有泥沙、Ca2+、Mg2+、SO 等杂质。某同学在实验室中设计了用这种粗盐制备精盐的方案如图(用于沉淀的试剂稍过量)。
等杂质。某同学在实验室中设计了用这种粗盐制备精盐的方案如图(用于沉淀的试剂稍过量)。
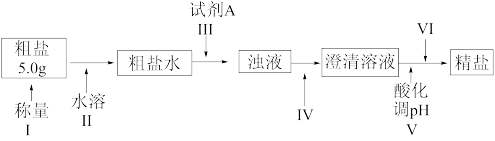
请回答以下问题:
(1)为操作IV选择所需仪器____ (填字母)。
a.烧杯 b.试管 c.玻璃棒 d.分液漏斗 e.漏斗 f.酒精灯 g.蒸发皿
(2)试剂A中常用①NaOH溶液、②Na2CO3溶液、③BaCl2溶液作为除杂试剂,则加入除杂试剂的顺序为____ 。
A.①②③ B.①③② C.②①③
(3)操作V调pH中应选择的酸是____ ,若将操作V与操作IV的先后顺序对调,将会对实验结果产生的影响是____ 。
 等杂质。某同学在实验室中设计了用这种粗盐制备精盐的方案如图(用于沉淀的试剂稍过量)。
等杂质。某同学在实验室中设计了用这种粗盐制备精盐的方案如图(用于沉淀的试剂稍过量)。
请回答以下问题:
(1)为操作IV选择所需仪器
a.烧杯 b.试管 c.玻璃棒 d.分液漏斗 e.漏斗 f.酒精灯 g.蒸发皿
(2)试剂A中常用①NaOH溶液、②Na2CO3溶液、③BaCl2溶液作为除杂试剂,则加入除杂试剂的顺序为
A.①②③ B.①③② C.②①③
(3)操作V调pH中应选择的酸是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】钴盐在生活和生产中有着重要应用。
(1)在活性炭的催化作用下,通过氧化CoCl2·6H2O制得到[Co(NH3)6]Cl3流程如下:
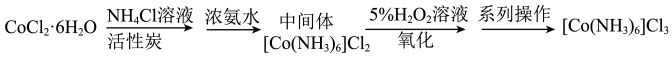
①在“氧化”过程,需水浴控温在50~60℃,温度不能过高,原因是:___________ 。“系列操作”是指在高浓度的盐酸中使[Co(NH3)6]Cl3结晶析出,过滤,醇洗,干燥。使用乙醇洗涤产品的具体操作是:___________ 。
②结束后废水中的Co2+,人们常用FeS沉淀剂来处理,原理是___________ (用离子方程式表示)。
(2)草酸钴是制备钴氧化物的重要原料,常用(NH4)2C2O4溶液和CoCl2溶液制取难溶于水的CoC2O4·2H2O晶体。
①常温下,(NH4)2C2O4溶液的pH___________ 7(填“>”、“=”或“<”)。(已知:常温下Kb(NH3·H2O)=1.8×10-5,H2C2O4:Ka1=5.6×10-2,Ka2=5.4×10-5)
②制取CoC2O4·2H2O晶体时,还需加入适量氨水,其作用是___________ 。
③在空气中加热10.98g二水合草酸钴(CoC2O4·2H2O),受热过程中在不同温度范围内分别得到一种固体物质。已知Co的两种常见化合价为+2价和+3价,M(CoC2O4·2H2O)=183g/mol。
i.温度在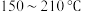 范围内,固体物质为
范围内,固体物质为___________ (填化学式);
ii.从 加热到
加热到 时生成一种钴的氧化物和CO2,此过程发生反应的化学方程式是
时生成一种钴的氧化物和CO2,此过程发生反应的化学方程式是______ 。
(1)在活性炭的催化作用下,通过氧化CoCl2·6H2O制得到[Co(NH3)6]Cl3流程如下:
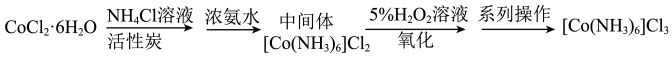
①在“氧化”过程,需水浴控温在50~60℃,温度不能过高,原因是:
②结束后废水中的Co2+,人们常用FeS沉淀剂来处理,原理是
(2)草酸钴是制备钴氧化物的重要原料,常用(NH4)2C2O4溶液和CoCl2溶液制取难溶于水的CoC2O4·2H2O晶体。
①常温下,(NH4)2C2O4溶液的pH
②制取CoC2O4·2H2O晶体时,还需加入适量氨水,其作用是
③在空气中加热10.98g二水合草酸钴(CoC2O4·2H2O),受热过程中在不同温度范围内分别得到一种固体物质。已知Co的两种常见化合价为+2价和+3价,M(CoC2O4·2H2O)=183g/mol。
| 温度范围/℃ | 150~210 | 290~320 |
| 固体质量/g | 8.82 | 4.82 |
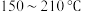 范围内,固体物质为
范围内,固体物质为ii.从
 加热到
加热到 时生成一种钴的氧化物和CO2,此过程发生反应的化学方程式是
时生成一种钴的氧化物和CO2,此过程发生反应的化学方程式是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】三氯化铁在印刷、医药、颜料、污水处理以及有机合成催化剂方面有重要的应用。以硫铁矿(主要成分为 ,杂质不与盐酸反应)为原料制备三氯化铁晶体
,杂质不与盐酸反应)为原料制备三氯化铁晶体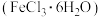 的工艺流程如图所示:
的工艺流程如图所示:
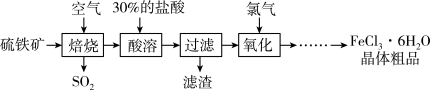
回答下列问题:
(1)“焙烧”过程中,理论上 ,被氧化转移
,被氧化转移 电子,则该反应的氧化产物为
电子,则该反应的氧化产物为_____________ 。
(2)现有试剂:①稀盐酸 ②稀硫酸 ③稀硝酸 ④氯气 ⑤硫氰化钾溶液 ⑥高锰酸钾溶液 ⑦氢氧化钠溶液。
为确认“酸溶”后的溶液中是否会含 ,另取“焙烧”后的烧渣少许,用
,另取“焙烧”后的烧渣少许,用________ (从上述试剂中选择,填标号)溶解,将所得溶液滴入______________ (从上述试剂中选择,填标号)中,若_________ ,则说明“酸溶”后的溶液中含 。
。
(3)从 溶液中得到
溶液中得到 的操作包括
的操作包括_______ 、冷却结晶、过滤,该过程需保持盐酸过量,结合必要的离子方程式说明原因:____________________ 。
(4)从 中得到无水
中得到无水 的操作方法为
的操作方法为____________________________ 。
(5)若以a吨硫铁矿为原料,最终制得b吨 ,不计生产过程中的损失,则该硫铁矿中
,不计生产过程中的损失,则该硫铁矿中 的含量为
的含量为_______________ (用含a、b的代数式表示)。
 ,杂质不与盐酸反应)为原料制备三氯化铁晶体
,杂质不与盐酸反应)为原料制备三氯化铁晶体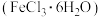 的工艺流程如图所示:
的工艺流程如图所示:
回答下列问题:
(1)“焙烧”过程中,理论上
 ,被氧化转移
,被氧化转移 电子,则该反应的氧化产物为
电子,则该反应的氧化产物为(2)现有试剂:①稀盐酸 ②稀硫酸 ③稀硝酸 ④氯气 ⑤硫氰化钾溶液 ⑥高锰酸钾溶液 ⑦氢氧化钠溶液。
为确认“酸溶”后的溶液中是否会含
 ,另取“焙烧”后的烧渣少许,用
,另取“焙烧”后的烧渣少许,用 。
。(3)从
 溶液中得到
溶液中得到 的操作包括
的操作包括(4)从
 中得到无水
中得到无水 的操作方法为
的操作方法为(5)若以a吨硫铁矿为原料,最终制得b吨
 ,不计生产过程中的损失,则该硫铁矿中
,不计生产过程中的损失,则该硫铁矿中 的含量为
的含量为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】软锰矿的主要成分是MnO2,还含有少量金属铁、镁、铝、锌、铜的化合物等杂质。黄铁矿的主要成分是FeS2,还含有硅、铝的氧化物等杂质。工业上用软锰矿制备碳酸锰并回收硫酸铵,其主要流程如下:
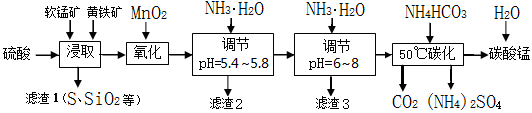
已知金属离子从开始形成氢氧化物沉淀,到沉淀时溶液的pH如下表:
(1)提高浸出率的可采取的措施有____ 。
a.适当升高温度 b.搅拌 c.加适量纯碱 d.加压
(2)浸取完成后,取浸取液少许,加入KSCN溶液无明显现象,则浸取时发生的主要反应的化学方程式是__________________________ 。
(3)调节pH为5.4~5.8的目的是______________ 。
(4)滤渣3的主要成分的化学式是_______ 。
(5)采用50℃碳化的原因是_________________________________ 。该过程发生反应的离子方程式是__________________ 。
(6)检验碳酸锰产品完全洗净的方法是_______________________________ 。

已知金属离子从开始形成氢氧化物沉淀,到沉淀时溶液的pH如下表:
| 金属离子 | Fe2+ | Fe3+ | Al3+ | Cu2+ | Mn2+ |
| 开始沉淀pH | 7.5 | 2.7 | 4.1 | 5.9 | 8.8 |
| 完全沉淀pH | 9.5 | 3.7 | 5.4 | 6.9 | 10.8 |
a.适当升高温度 b.搅拌 c.加适量纯碱 d.加压
(2)浸取完成后,取浸取液少许,加入KSCN溶液无明显现象,则浸取时发生的主要反应的化学方程式是
(3)调节pH为5.4~5.8的目的是
(4)滤渣3的主要成分的化学式是
(5)采用50℃碳化的原因是
(6)检验碳酸锰产品完全洗净的方法是
您最近一年使用:0次
【推荐2】某种电镀污泥主要含有碲化亚铜(Cu2Te)、三氧化二铬(Cr2O3)以及少量的金(Au),可以用于制取Na2Cr2O7溶液、金属铜和粗碲等,以实现有害废料的资源化利用,工艺流程如下:
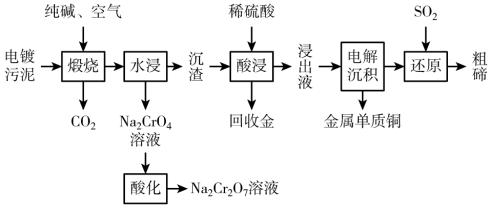
已知:煅烧时,Cu2Te发生的反应为Cu2Te+2O2 2CuO+TeO2。
2CuO+TeO2。
(1)煅烧时,Cr2O3发生反应的化学方程式为___________ 。
(2)为提高酸浸速率,可采用的措施是___________ (任写一条)。
(3)浸出液中除了含有TeOSO4(在电解过程中不反应)外,还可能含有___________ (写化学式)。
(4)在实际的含铬废水处理中,还可采用直接沉淀的方法,处理成本较低。
①已知含铬酸性废水中存在着Cr2O 和CrO
和CrO 相互转化的平衡,请用离子方程式表示它们之间的转化反应
相互转化的平衡,请用离子方程式表示它们之间的转化反应___________ 。
②在实际工业生产中,加入沉淀剂BaCl2溶液之前还要加入一定量的NaOH,这样有利于沉淀的生成,则生成的沉淀为___________ 。(写化学式)。
(5)测定产品中K2Cr2O7含量的方法如下:称取产品试样2.50g配成250mL溶液,用移液管取出25.00mL于锥形瓶中,加入足量稀硫酸酸化后,再加入几滴指示剂,用0.1000 mol·L-1硫酸亚铁铵(NH4)2Fe(SO4)2标准液进行滴定,重复进行二次实验。(已知Cr2O 被还原为Cr3+)
被还原为Cr3+)
①氧化还原滴定过程中的离子方程式为___________ 。
②若三次实验消耗(NH4)2Fe(SO4)2标准液的平均体积为25.00mL,则所得产品中K2Cr2O7的纯度为___________ %。[已知M(K2Cr2O7)=294g·mol-1,计算结果保留三位有效数字]
(6)上述流程中K2Cr2O7发生氧化还原反应后所得溶液中除含有Cr3+外,还含有一定浓度的Fe3+杂质,可通过加碱调pH的方法使两者转化为沉淀。已知c(Cr3+)=3×10-5 mol·L-1,则当溶液中开始析出Cr(OH)3沉淀时Fe3+是否沉淀完全?___________ (填“是”或“否”)。{已知:Ksp[Fe(OH)3]=4.0×10-38,Ksp[Cr(OH)3]=6.0×10-31}

已知:煅烧时,Cu2Te发生的反应为Cu2Te+2O2
 2CuO+TeO2。
2CuO+TeO2。(1)煅烧时,Cr2O3发生反应的化学方程式为
(2)为提高酸浸速率,可采用的措施是
(3)浸出液中除了含有TeOSO4(在电解过程中不反应)外,还可能含有
(4)在实际的含铬废水处理中,还可采用直接沉淀的方法,处理成本较低。
①已知含铬酸性废水中存在着Cr2O
 和CrO
和CrO 相互转化的平衡,请用离子方程式表示它们之间的转化反应
相互转化的平衡,请用离子方程式表示它们之间的转化反应②在实际工业生产中,加入沉淀剂BaCl2溶液之前还要加入一定量的NaOH,这样有利于沉淀的生成,则生成的沉淀为
(5)测定产品中K2Cr2O7含量的方法如下:称取产品试样2.50g配成250mL溶液,用移液管取出25.00mL于锥形瓶中,加入足量稀硫酸酸化后,再加入几滴指示剂,用0.1000 mol·L-1硫酸亚铁铵(NH4)2Fe(SO4)2标准液进行滴定,重复进行二次实验。(已知Cr2O
 被还原为Cr3+)
被还原为Cr3+)①氧化还原滴定过程中的离子方程式为
②若三次实验消耗(NH4)2Fe(SO4)2标准液的平均体积为25.00mL,则所得产品中K2Cr2O7的纯度为
(6)上述流程中K2Cr2O7发生氧化还原反应后所得溶液中除含有Cr3+外,还含有一定浓度的Fe3+杂质,可通过加碱调pH的方法使两者转化为沉淀。已知c(Cr3+)=3×10-5 mol·L-1,则当溶液中开始析出Cr(OH)3沉淀时Fe3+是否沉淀完全?
您最近一年使用:0次
【推荐3】醋酸亚铬[(CH3COO)2Cr·H2O]为砖红色晶体,难溶于冷水,易溶于酸,在气体分析中用作氧气吸收剂。一般制备方法是先在封闭体系中利用金属锌作还原剂,将三价铬还原为二价铬;二价铬再与醋酸钠溶液作用即可制得醋酸亚铬。实验装置如图所示,回答下列问题:

打开K3,关闭K1和K2.c中亮蓝色溶液流入d,其原因是___________ ;d中析出砖红色沉淀,为使沉淀充分析出并分离,需采用的操作是___________ 、___________ 、洗涤、干燥。

打开K3,关闭K1和K2.c中亮蓝色溶液流入d,其原因是
您最近一年使用:0次



