氯气是一种重要的化工原料,呈黄绿色,有毒,能与多种物质反应。用图所示装置Ⅰ可制取氯气,并对其性质进行一系列的实验探究。
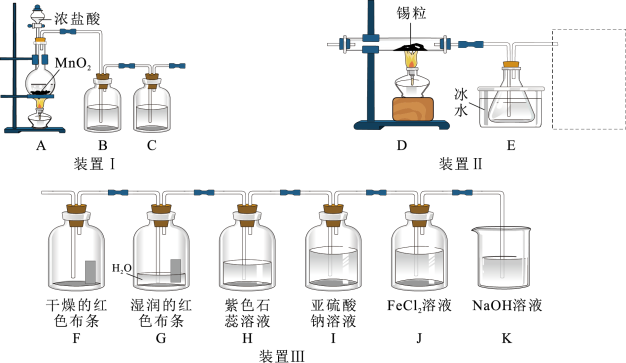
回答下列问题:
(1)①装置Ⅰ中盛装浓盐酸的仪器名称是_______ 。
②实验室利用装置A制氯气,反应的离子方程式是_______ 。
(2)利用纯净、干燥的氯气与熔融金属锡反应可制备 ,将装置Ⅰ与装置Ⅱ连接起来可制备
,将装置Ⅰ与装置Ⅱ连接起来可制备 。已知:金属锡熔点为231℃,活泼性与铁相似;
。已知:金属锡熔点为231℃,活泼性与铁相似; 的沸点为114℃;
的沸点为114℃; 易与水反应。
易与水反应。
①装置E的作用是_______ 。
②虚线框可选用下列装置中的_______ (填“甲”“乙”或“丙”)。
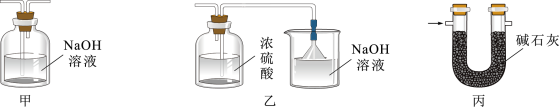
(3)将装置Ⅰ与装置Ⅱ连接起来探究氯气的漂白性及氧化性。
①F、G通入 后,观察到的现象是
后,观察到的现象是_________ ,根据现象可得出结论: 无漂白性,
无漂白性, 与水反应生成的
与水反应生成的 有漂白性。
有漂白性。
②实验开始后,观察到洗气瓶H中的现象是_______ 。
③请设计一个实验,证明洗气瓶Ⅰ中的亚硫酸钠已被氧化(简述实验操作):_______ 。
④装置K的作用是_______ 。

回答下列问题:
(1)①装置Ⅰ中盛装浓盐酸的仪器名称是
②实验室利用装置A制氯气,反应的离子方程式是
(2)利用纯净、干燥的氯气与熔融金属锡反应可制备
 ,将装置Ⅰ与装置Ⅱ连接起来可制备
,将装置Ⅰ与装置Ⅱ连接起来可制备 。已知:金属锡熔点为231℃,活泼性与铁相似;
。已知:金属锡熔点为231℃,活泼性与铁相似; 的沸点为114℃;
的沸点为114℃; 易与水反应。
易与水反应。①装置E的作用是
②虚线框可选用下列装置中的

(3)将装置Ⅰ与装置Ⅱ连接起来探究氯气的漂白性及氧化性。
①F、G通入
 后,观察到的现象是
后,观察到的现象是 无漂白性,
无漂白性, 与水反应生成的
与水反应生成的 有漂白性。
有漂白性。②实验开始后,观察到洗气瓶H中的现象是
③请设计一个实验,证明洗气瓶Ⅰ中的亚硫酸钠已被氧化(简述实验操作):
④装置K的作用是
更新时间:2022-09-15 08:49:14
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】氯气是一种重要的化工原料。
(1)标准状况下,22.4L Cl2的物质的量为________ mol。
(2)实验室制取Cl2的化学方程式为________________________ 。
(3)收集Cl2应使用_________ 法,要得到干燥的Cl2可选用 _______ 做干燥剂。
(4)写出实验室制取漂白液的反应的离子方程式______________________________ 。
(1)标准状况下,22.4L Cl2的物质的量为
(2)实验室制取Cl2的化学方程式为
(3)收集Cl2应使用
(4)写出实验室制取漂白液的反应的离子方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】已知在实验室浓盐酸和二氧化锰加热条件下可以反应生成氯化锰和Cl2等,某同学用此法制得标准状况下Cl2体积为22.4mL,据题意回答下列问题:
(1)写出其化学反应方程式并配平____________
(2)请计算共消耗MnO2多少克?_____________
(3)上述实验所用浓盐酸,其质量分数为36.5%,密度为1.19g/mL,为了使用方便,请计算该浓盐酸的物质的量浓度为多少?_______________
(1)写出其化学反应方程式并配平
(2)请计算共消耗MnO2多少克?
(3)上述实验所用浓盐酸,其质量分数为36.5%,密度为1.19g/mL,为了使用方便,请计算该浓盐酸的物质的量浓度为多少?
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】已知A和B两支试管所盛的溶液中共含有K+、Ag+、Mg2+、Cl-、OH-、NO3-六种离子,向试管A的溶液中滴入酚酞试液呈粉红色。请回答下列问题:
(1)试管A的溶液中所含上述离子共有___________ 种。
(2)若向某试管中滴入稀盐酸产生沉淀,则该试管为_______ (填“A”或“B”)。
(3)若向试管B的溶液中加入合适的药品,过滤后可以得到相应的金属和仅含一种溶质的溶液,则加入的药品是________________ (填化学式)。
(4)若将试管A和试管B中的溶液按一定体积比混合过滤后,蒸干滤液可得到一种纯净物,则混合过程中发生反应的离子方程式为_________________________ , _________________________ 。
(1)试管A的溶液中所含上述离子共有
(2)若向某试管中滴入稀盐酸产生沉淀,则该试管为
(3)若向试管B的溶液中加入合适的药品,过滤后可以得到相应的金属和仅含一种溶质的溶液,则加入的药品是
(4)若将试管A和试管B中的溶液按一定体积比混合过滤后,蒸干滤液可得到一种纯净物,则混合过程中发生反应的离子方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】工业上从海水中提溴,实验室中从海带中提碘的过程中发生反应的离子方程式有:



回答下列问题:
(1)根据所给出的反应,判断 、
、 、
、 、
、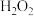 、
、 的氧化性强弱,可以明确得出的结论是
的氧化性强弱,可以明确得出的结论是____ 、___ 。
(2)将适量溴水加入氟化钠溶液中,__ (填“能”或“不能”)观察到明显现象。
(3)将适量碘水加入氯化钠溶液中,__ (填“能”或“不能”)观察到明显现象。



回答下列问题:
(1)根据所给出的反应,判断
 、
、 、
、 、
、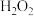 、
、 的氧化性强弱,可以明确得出的结论是
的氧化性强弱,可以明确得出的结论是(2)将适量溴水加入氟化钠溶液中,
(3)将适量碘水加入氯化钠溶液中,
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】回答下列问题:
(1)用金属钠制取氧化钠通常利用以下反应:2NaNO3+10Na 6Na2O+N2↑。试说明不用金属钠与氧气的反应而采用此反应的理由:
6Na2O+N2↑。试说明不用金属钠与氧气的反应而采用此反应的理由:______ 。此反应的氧化剂:______ ;氧化产物:______ 。
(2)利用图所示装置及药品制取氨气。
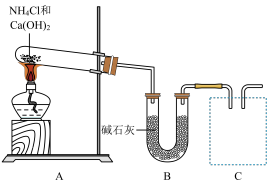
①A中制氨气的化学方程式是______ 。
②B中碱石灰的作用是______ 。
③C处是用集气瓶收集氨气的装置,请绘出装置图(在虚线内画出)______ 。
④证明氨气已集满的方法是______ 。
(1)用金属钠制取氧化钠通常利用以下反应:2NaNO3+10Na
 6Na2O+N2↑。试说明不用金属钠与氧气的反应而采用此反应的理由:
6Na2O+N2↑。试说明不用金属钠与氧气的反应而采用此反应的理由:(2)利用图所示装置及药品制取氨气。

①A中制氨气的化学方程式是
②B中碱石灰的作用是
③C处是用集气瓶收集氨气的装置,请绘出装置图(在虚线内画出)
④证明氨气已集满的方法是
您最近一年使用:0次
【推荐2】铁是人类较早使用的金属之一,铁合金也是用量最大的金属材料。请按要求完成下列问题。
(1)在自然界中,铁元素主要以___________ 填写“游离态”或“化合态”形式存在
(2)下列铁的化合物中,不能直接化合得到的是___________用字母代号填 。
。
(3)高铁酸钾 是一种新型、高效、多功能水处理剂,与水反应可生成透明的红褐色胶体,反应原理:
是一种新型、高效、多功能水处理剂,与水反应可生成透明的红褐色胶体,反应原理: 胶体
胶体 。
。
 胶体分散质粒子的直径范围是
胶体分散质粒子的直径范围是___________ 。
 该反应中
该反应中 是
是___________ 。
A.氧化剂 B.还原剂 C.被氧化 D.被还原
 高铁酸钾
高铁酸钾 能杀灭水中细菌的原因是
能杀灭水中细菌的原因是___________ 。
(4)电子工业常用 左右的
左右的 溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。为了从腐蚀废液中回收铜,并重新获得
溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。为了从腐蚀废液中回收铜,并重新获得 溶液,某同学设计下列方案:
溶液,某同学设计下列方案:

 实验室用无水氯化铁固体粗略配制
实验室用无水氯化铁固体粗略配制 的
的 溶液,需要的主要玻璃仪器除了量筒外还有
溶液,需要的主要玻璃仪器除了量筒外还有___________ 。
 写出
写出 溶液与铜箔发生反应的离子方程式
溶液与铜箔发生反应的离子方程式___________ 。
 现用500g 32.5% FeCl3溶液制造印刷电路板,生产后的腐蚀废液用该同学设计方案处理,最终获得氯化铁溶液中的
现用500g 32.5% FeCl3溶液制造印刷电路板,生产后的腐蚀废液用该同学设计方案处理,最终获得氯化铁溶液中的 物质的量至少为
物质的量至少为___________ mol。
(5)铝及其合金是金属材料界后起之秀。某研究性学习小组设计实验探究铝等金属的性质:将一置于空气中的铝片投入浓氯化铜溶液中,铝片表面出现一层海绵状暗红色物质,接下来铝片上产生大量气泡,溶液温度迅速上升。若用同样的铝片投入相同浓度的硫酸铜溶液中,在短时间内铝片无明显变化。造成不同现象的原因可能是___________  填序号
填序号 。
。
A.铝与氯化铜溶液反应,与硫酸铜溶液不反应
B.氯化铜溶液酸性比同浓度的硫酸铜溶液酸性强
C.生成物 溶于水,而
溶于水,而 不溶于水
不溶于水
D.氯离子能破坏氧化铝薄膜,而硫酸根离子不能
请设计一个简单实验验证你的选择:___________ 。
(1)在自然界中,铁元素主要以
(2)下列铁的化合物中,不能直接化合得到的是___________用字母代号填
 。
。A. | B. | C. | D. |
(3)高铁酸钾
 是一种新型、高效、多功能水处理剂,与水反应可生成透明的红褐色胶体,反应原理:
是一种新型、高效、多功能水处理剂,与水反应可生成透明的红褐色胶体,反应原理: 胶体
胶体 。
。 胶体分散质粒子的直径范围是
胶体分散质粒子的直径范围是 该反应中
该反应中 是
是A.氧化剂 B.还原剂 C.被氧化 D.被还原
 高铁酸钾
高铁酸钾 能杀灭水中细菌的原因是
能杀灭水中细菌的原因是(4)电子工业常用
 左右的
左右的 溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。为了从腐蚀废液中回收铜,并重新获得
溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。为了从腐蚀废液中回收铜,并重新获得 溶液,某同学设计下列方案:
溶液,某同学设计下列方案:
 实验室用无水氯化铁固体粗略配制
实验室用无水氯化铁固体粗略配制 的
的 溶液,需要的主要玻璃仪器除了量筒外还有
溶液,需要的主要玻璃仪器除了量筒外还有 写出
写出 溶液与铜箔发生反应的离子方程式
溶液与铜箔发生反应的离子方程式 现用500g 32.5% FeCl3溶液制造印刷电路板,生产后的腐蚀废液用该同学设计方案处理,最终获得氯化铁溶液中的
现用500g 32.5% FeCl3溶液制造印刷电路板,生产后的腐蚀废液用该同学设计方案处理,最终获得氯化铁溶液中的 物质的量至少为
物质的量至少为(5)铝及其合金是金属材料界后起之秀。某研究性学习小组设计实验探究铝等金属的性质:将一置于空气中的铝片投入浓氯化铜溶液中,铝片表面出现一层海绵状暗红色物质,接下来铝片上产生大量气泡,溶液温度迅速上升。若用同样的铝片投入相同浓度的硫酸铜溶液中,在短时间内铝片无明显变化。造成不同现象的原因可能是
 填序号
填序号 。
。A.铝与氯化铜溶液反应,与硫酸铜溶液不反应
B.氯化铜溶液酸性比同浓度的硫酸铜溶液酸性强
C.生成物
 溶于水,而
溶于水,而 不溶于水
不溶于水 D.氯离子能破坏氧化铝薄膜,而硫酸根离子不能
请设计一个简单实验验证你的选择:
您最近一年使用:0次

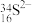 微粒中的中子数为
微粒中的中子数为


