下列图示中,A为一种常见的单质,B、C、D、E是含A元素的常见化合物,它们的焰色试验均为黄色。
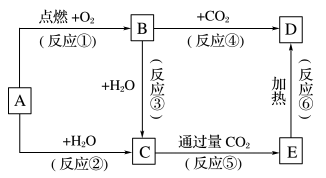
请填写下列空白:
(1)写出下列化学式:B____ ,C____ ,E____ 。
(2)反应②③⑤⑥中____ (填序号)属于氧化还原反应。
(3)完成下列方程式。
①写出反应①的化学方程式:____ 。
②写出反应③的离子方程式:____ 。

请填写下列空白:
(1)写出下列化学式:B
(2)反应②③⑤⑥中
(3)完成下列方程式。
①写出反应①的化学方程式:
②写出反应③的离子方程式:
更新时间:2022-09-15 22:46:43
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】已知A、B、C、D是中学化学的常见物质,且A、B、C均含有同一种元素。在一定条件下它们之间的相互转化关系如图所示(部分反应中的H2O已略去)。
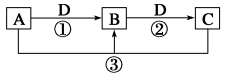
请回答下列问题:
(1)若A是黄绿色的气体,D是铁单质。则B是____________ (填化学式),反应③的离子方程式为__________________ 。
(2)若A是一种有刺激性气味的气体,其水溶液呈碱性;B和C是常见的氧化物且C是红棕色气体。则反应①的化学方程式为____________ ,A的用途有____________ (任写一种)。
(3)若A、C、D都是气体,B是一种(淡)黄色的固体单质,C是形成酸雨的主要物质。在标准状况下,反应③中消耗6.72L的A,则转移的电子数为____________ 。
(4)若A是钠盐,B俗称小苏打,则反应②的离子方程式为____________ ;配制250mL0.1mol·L-1Na2CO3溶液,需要用托盘天平称量Na2CO3•10H2O晶体的质量为____________ 克。

请回答下列问题:
(1)若A是黄绿色的气体,D是铁单质。则B是
(2)若A是一种有刺激性气味的气体,其水溶液呈碱性;B和C是常见的氧化物且C是红棕色气体。则反应①的化学方程式为
(3)若A、C、D都是气体,B是一种(淡)黄色的固体单质,C是形成酸雨的主要物质。在标准状况下,反应③中消耗6.72L的A,则转移的电子数为
(4)若A是钠盐,B俗称小苏打,则反应②的离子方程式为
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】A、B、C、D、E、F是六种短周期主族元素,它们的原子序数依次增大,其中C、F分别是同一主族元素,A、F两种元素的原子核中质子数之和比C、D两种元素原子核中质子数之和少2,F元素的最外层电子数是次外层电子数的0.75倍。又知B元素的最外层电子数是内层电子数的2倍,E元素的最外层电子数等于其电子层数。请回答:
(1)1 mol由E、F二种元素组成的化合物跟由A、C、D三种元素组成的化合物反应生成两种盐和水,完全反应后消耗后者的物质的量为___________ 。
(2)A、C、F间可以形成甲、乙两种负一价双原子阴离子,甲有18个电子,乙有10个电子,则甲与乙反应的离子方程式为___________ ;
(3)科学研究证明:化学反应热只与始终态有关,与过程无关。单质B的燃烧热为a kJ/mol。由B、C二种元素组成的化合物BC l4 g完全燃烧放出热量b kJ,写出单质B和单质C反应生成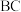 的热化学方程式:
的热化学方程式:___________ ;
(4)用B元素的单质与E元素的单质可以制成电极浸入由A、C、D三种元素组成化合物的溶液中构成电池,则电池负极反应式为___________ 。
(5)C、D、E、F四种元素的离子半径由大到小的顺序___________ (用离子符号表示)
(6)过量B元素的最高价氧化物与D元素的最高价氧化物的水化物反应的离子方程式为___________ 。
(1)1 mol由E、F二种元素组成的化合物跟由A、C、D三种元素组成的化合物反应生成两种盐和水,完全反应后消耗后者的物质的量为
(2)A、C、F间可以形成甲、乙两种负一价双原子阴离子,甲有18个电子,乙有10个电子,则甲与乙反应的离子方程式为
(3)科学研究证明:化学反应热只与始终态有关,与过程无关。单质B的燃烧热为a kJ/mol。由B、C二种元素组成的化合物BC l4 g完全燃烧放出热量b kJ,写出单质B和单质C反应生成
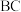 的热化学方程式:
的热化学方程式:(4)用B元素的单质与E元素的单质可以制成电极浸入由A、C、D三种元素组成化合物的溶液中构成电池,则电池负极反应式为
(5)C、D、E、F四种元素的离子半径由大到小的顺序
(6)过量B元素的最高价氧化物与D元素的最高价氧化物的水化物反应的离子方程式为
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】A经图所示的过程转化为含氧酸D,已知D为强酸,请回答下列问题:
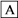
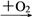
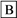

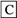
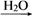
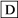
(1)若A在常温下为非金属单质固体,B是能使品红溶液褪色的有刺激性气味的无色气体。
①D的化学式是_________ 。
②在工业生产中,大量排放的B气体被雨水吸收后形成了_________ 而污染环境。
(2)若A在常温下为气态化合物,C是红棕色气体。
①A、C的化学式分别是:A_________ 、C_________ 。
②写出A与O2反应的化学方程式:_________________________________ 。
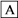
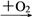
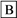

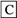
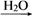
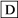
(1)若A在常温下为非金属单质固体,B是能使品红溶液褪色的有刺激性气味的无色气体。
①D的化学式是
②在工业生产中,大量排放的B气体被雨水吸收后形成了
(2)若A在常温下为气态化合物,C是红棕色气体。
①A、C的化学式分别是:A
②写出A与O2反应的化学方程式:
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】已知甲和乙为中学化学常见金属单质,丙和丁为常见气体单质,A~E为常见化合物;A为淡黄色固体,常温下B为液体,C的焰色反应为黄色。试回答下列问题:
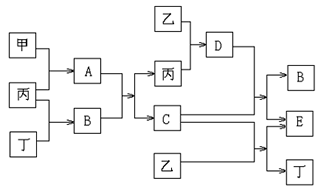
(1)A和E的化学式分别为_____________ 、____________ ;
(2)A+B→C+丙的化学方程式:__________________________________________ ;
(3)D+C→B+E的化学方程式:__________________________________________ ;
(4)1mol甲和1mol乙混合投入到足量的B中,在标准状况下,最多能产生丁气体______ L。

(1)A和E的化学式分别为
(2)A+B→C+丙的化学方程式:
(3)D+C→B+E的化学方程式:
(4)1mol甲和1mol乙混合投入到足量的B中,在标准状况下,最多能产生丁气体
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】下表是元素周期表的一部分,表中所列的字母分别代表某一化学元素。

回答下列问题(填元素符号或化学式):
(1)D简单离子的结构示意图为___________ ,D、E中金属性较强的元素是_______ 。
D单质在空气中燃烧可生成淡黄色粉末X,X常用作呼吸面具和潜水艇中的供氧剂,可选用合适的化学试剂和下图所示实验装置证明X有提供氧气的作用。
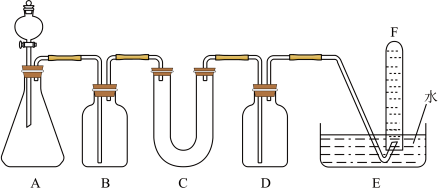
(2)装置A使用石灰石与盐酸反应制取 ,装置B中饱和
,装置B中饱和 溶液的作用是除去
溶液的作用是除去___________ 。
(3)装置C中 与
与 反应的化学方程式是
反应的化学方程式是___________ ,装置D盛放 溶液的作用是除去
溶液的作用是除去___________ 。
(4)为检验试管F收集的气体,进行___________ 操作,出现___________ 现象,即证明X可作供氧剂。

回答下列问题(填元素符号或化学式):
(1)D简单离子的结构示意图为
D单质在空气中燃烧可生成淡黄色粉末X,X常用作呼吸面具和潜水艇中的供氧剂,可选用合适的化学试剂和下图所示实验装置证明X有提供氧气的作用。

(2)装置A使用石灰石与盐酸反应制取
 ,装置B中饱和
,装置B中饱和 溶液的作用是除去
溶液的作用是除去(3)装置C中
 与
与 反应的化学方程式是
反应的化学方程式是 溶液的作用是除去
溶液的作用是除去(4)为检验试管F收集的气体,进行
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】选考(15)化学与技术
侯氏制碱法的生产流程可表示如下,请回答下列问题:
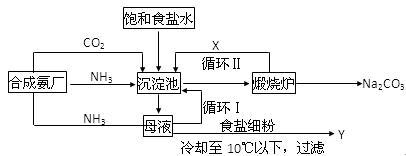
(1)沉淀池中加入(或通入)有关物质的顺序为_____________ →___________ →___________
(2)写出上述流程中X、Y的化学式:X____________ Y___________
(3)写出沉淀池中发生的化学反应方程式__________________________________________
(4)侯氏制碱法的生产流程中可以循环使用的物质主要为____________ 、______________
(5)从沉淀池中取出沉淀的操作是___________ ,为了进一步提纯NaHCO3晶体,可采用_______ 法
(6)若在煅烧炉中燃烧的时间较短,NaHCO3将分解不完全。现若取10.5g NaHCO3固体,加热一定时间后,剩余固体的质量为7.1g,如果把此剩余固体全部加入到200mL 1mol/L的盐酸中,充分反应后溶液中H+的物质的量浓度为___________ mol/L(溶液体积变化忽略不计)
侯氏制碱法的生产流程可表示如下,请回答下列问题:

(1)沉淀池中加入(或通入)有关物质的顺序为
(2)写出上述流程中X、Y的化学式:X
(3)写出沉淀池中发生的化学反应方程式
(4)侯氏制碱法的生产流程中可以循环使用的物质主要为
(5)从沉淀池中取出沉淀的操作是
(6)若在煅烧炉中燃烧的时间较短,NaHCO3将分解不完全。现若取10.5g NaHCO3固体,加热一定时间后,剩余固体的质量为7.1g,如果把此剩余固体全部加入到200mL 1mol/L的盐酸中,充分反应后溶液中H+的物质的量浓度为
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】下列图示中,A为一种常见的单质,B、C、D、E是含A元素的常见化合物,它们的焰色实验均为黄色。请填写下列空白:
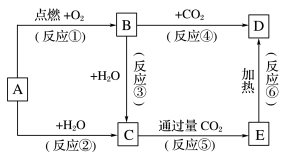
(1)写出下列化学式: D_______ ,E_______ 。
(2)以上反应中,不属于氧化还原反应的有_______ (填序号)。
(3)完成方程式:
①A→C反应的离子方程式:_______ ;
②B→D反应的化学方程式:_______ 。

(1)写出下列化学式: D
(2)以上反应中,不属于氧化还原反应的有
(3)完成方程式:
①A→C反应的离子方程式:
②B→D反应的化学方程式:
您最近半年使用:0次
【推荐3】钠的化合物在日常生活中的应用非常广泛。回答下列问题:
Ⅰ.为了测定Na2CO3和NaHCO3的混合物中Na2CO3的质量分数,某同学用如下实验装置完成实验。
(1)实验前首先要进行的操作是_______ 。
(2)某同学称取65.4 g混合物于锥形瓶中,打开止水夹,通入N2,一段时间后,关闭止水夹,打开旋塞,当锥形瓶中没有气泡生成时,关闭旋塞,再次打开止水夹,通入一段时间N2。停止通N2,装置C的质量增加30.8 g。
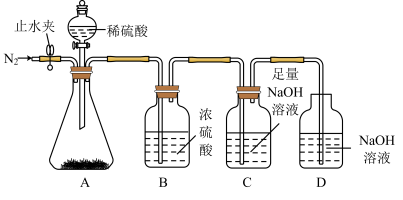
①两次通入N2的目的分别是_______ 、_______ 。
②混合物中Na2CO3的物质的量为_______ mol。
Ⅱ.侯德榜“联合制碱法”将制碱技术发展到一个新的水平。该工艺以氯化钠为原料制取纯碱,主要流程如图所示(部分物质已略去)。
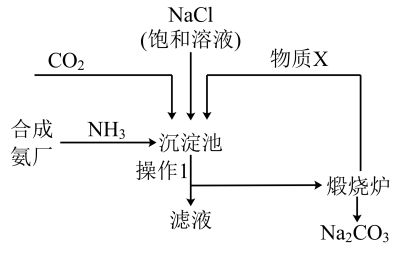
资料:沉淀池中的反应为NaCl+CO2+NH3+H2O=NaHCO3↓+NH4Cl。
(3)操作1的名称为_______ ;煅烧炉中反应的化学方程式为_______ 。
(4)物质X可循环利用,其化学式为_______ 。
(5)工业可用纯碱代替烧碱生产某些化工产品,如用饱和纯碱溶液与Cl2反应可制得一种在生产、生活中常用于漂白、消毒的物质,同时有NaHCO3生成,该反应的化学方程式是_______ 。
(6)某同学提出制得的纯碱中可能含有氯化钠,请设计实验鉴别:_______ (写出步骤、现象和结论)。
Ⅰ.为了测定Na2CO3和NaHCO3的混合物中Na2CO3的质量分数,某同学用如下实验装置完成实验。
(1)实验前首先要进行的操作是
(2)某同学称取65.4 g混合物于锥形瓶中,打开止水夹,通入N2,一段时间后,关闭止水夹,打开旋塞,当锥形瓶中没有气泡生成时,关闭旋塞,再次打开止水夹,通入一段时间N2。停止通N2,装置C的质量增加30.8 g。

①两次通入N2的目的分别是
②混合物中Na2CO3的物质的量为
Ⅱ.侯德榜“联合制碱法”将制碱技术发展到一个新的水平。该工艺以氯化钠为原料制取纯碱,主要流程如图所示(部分物质已略去)。

资料:沉淀池中的反应为NaCl+CO2+NH3+H2O=NaHCO3↓+NH4Cl。
(3)操作1的名称为
(4)物质X可循环利用,其化学式为
(5)工业可用纯碱代替烧碱生产某些化工产品,如用饱和纯碱溶液与Cl2反应可制得一种在生产、生活中常用于漂白、消毒的物质,同时有NaHCO3生成,该反应的化学方程式是
(6)某同学提出制得的纯碱中可能含有氯化钠,请设计实验鉴别:
您最近半年使用:0次




