有关CO2(g)+CH4(g) = 2CO(g)+2H2(g) ΔH1=+247 kJ·mol-1的说法正确的是
| A.该反应在任何温度下都可自发进行 |
| B.反应CO2(s)+CH4(g) = 2CO(g)+2H2(g) ΔH2<+247 kJ·mol-1 |
| C.选择高效催化剂可以降低反应的活化能,提高化学反应速率 |
| D.反应中每生成1 mol H2,转移电子的数目为2×6.02×1023 |
更新时间:2022-09-14 00:49:31
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】下列有关热化学方程式的叙述正确的是
| A.2NaOH(aq)+H2SO4(aq)═Na2SO4(aq)+2H2O(l)△H=﹣akJmol﹣1,则中和热为a/2kJ/mol |
| B.2H2(g)+O2(g)═2H2O(l);△H1=﹣akJmol﹣1,则氢气燃烧热为akJmol﹣1 |
| C.反应物的总能量低于生成物的总能量时,该反应必须加热才能发生 |
| D.N2(g)+3H2(g)⇌2NH3(g);△H=﹣akJmol﹣1,则将14gN2(g)和足量H2置于一密闭容器中,充分反应后放出0.5akJ的热量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】燃烧热是指101kPa时,1mol纯物质完全燃烧生成稳定的氧化物时所放出的热量,单位为kJ·mol-1。以下几个热化学方程式能表示相应物质的燃烧热的是
A.  |
B.  |
C.  |
D.  |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】下列关于热化学反应的描述中正确的是
| A.HCl和NaOH反应的中和热ΔH=-57.3kJ/mol,则H2SO4和Ca(OH)2反应的中和热ΔH=2×(-57.3)kJ/mol |
| B.CO(g)的燃烧热是283.0kJ/mol,则2CO2(g) =2CO(g)+O2(g)反应的ΔH=+2×283.0kJ/mol |
| C.需要加热才能发生的反应一定是吸热反应 |
| D.1mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】Ni可活化 制得
制得 ,其反应历程如下:
,其反应历程如下:

下列关于该活化历程的说法错误的是
 制得
制得 ,其反应历程如下:
,其反应历程如下:
下列关于该活化历程的说法错误的是
A.  |
| B.可以用焓判据来判断该反应是否自发进行 |
| C.中间体2→中间体3的活化能大于中间体1→中间体2的活化能 |
| D.Ni在该反应中作催化剂 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列实验方案设计、现象和结论都正确的是
| 编号 | 目的 | 方案设计 | 现象和结论 |
| A | 探究NaClO溶液的酸碱性 | 把NaClO溶液滴到pH试纸上 | pH=10,则NaClO溶液水解显碱性 |
| B | 探究反应速率与温度的关系 | 分别在20℃、30℃下,取0.1mol•L-1KI溶液,向其中先加入0.1mol•L-1的硫酸,再加入淀粉溶液 | 30℃下出现蓝色的时间短,则温度越高反应速率越快 |
| C | 探究MnSO4有催化作用 | 向酸性KMnO4和H2C2O4的混合液中加入一小块MnSO4 | 若生成气体的速率加快,溶液迅速褪色,则MnSO4是该反应的催化剂 |
| D | 探究反应速率与浓度的关系 | 两支试管各盛0.1mol/L4mL酸性高锰酸钾溶液,分别加入0.1mol/L2mL草酸溶液和0.2mol/L2mL草酸溶液 | 加入0.2mol/L草酸溶液试管中,高锰酸钾溶液褪色更快,则反应物浓度越大,反应速率越快 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】热催化合成氨面临的两难问题是:采用高温增大反应速率的同时会因平衡限制导致NH3产率降低。我国科研人员研制了Ti・H・Fe双温区催化剂(Ti-H区域和Fe区域的温度差可超过100℃)。Ti-H-Fe双温区催化合成氨的反应历程如图所示,其中吸附在催化剂表面上的物种用*标注。下列说法正确的是()


| A.①为氮氮三键的断裂过程 |
| B.①②③在低温区发生,④⑤在高温区发生 |
| C.使用Ti-H-Fe双温区催化剂使合成氨反应转变为吸热反应 |
| D.④为N原子由Fe区域向Ti-H区域的传递过程 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列叙述正确的是
A.某溶液的 ,则该溶液一定为中性溶液 ,则该溶液一定为中性溶液 |
B.在 溶液中: 溶液中: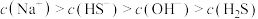 |
C. 氨水加水稀释后,溶液中 氨水加水稀释后,溶液中 的值减小 的值减小 |
D.常温下,反应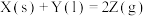 不能自发进行,则该反应的 不能自发进行,则该反应的 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】分析下列反应,在任何温度下均能自发进行的是
A.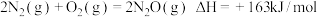 |
B.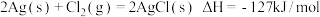 |
C.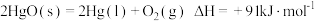 |
D.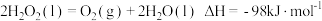 |
您最近一年使用:0次



