 的刚性密闭容器中,发生如下反应:
的刚性密闭容器中,发生如下反应: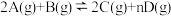 ,反应进行到
,反应进行到 末,测得A的物质的量为
末,测得A的物质的量为 ,C的物质的量为
,C的物质的量为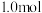 ,
, 内D的反应速率为
内D的反应速率为 ,则:
,则:(1)用C表示
 内反应的平均反应速率为
内反应的平均反应速率为 。
。(2)生成物D的化学计量数n为
(3)
 末反应物A的转化率为
末反应物A的转化率为(4)能说明该反应已达到平衡状态的是
a.v(A)=2v(B)
b.容器内压强保持不变
c.2v逆(A)=v正(B)
d.容器内混合气体的密度保持不变
e.c(A)∶c(B)∶c(C)=2∶1∶2
f.混合气体的平均相对分子质量保持不变
(5)反应进程中,正反应速率随时间的变化曲线如图所示:
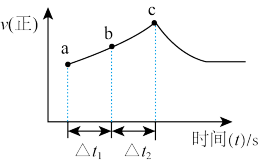
①该反应为
②反应在c点处v(正)
③若
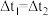 ,反应物B的转化率:
,反应物B的转化率: 段
段 段(填“>”或“=”或“<”)。
段(填“>”或“=”或“<”)。
相似题推荐

(1)该反应的化学方程式为
(2)2min内以气体X表示的平均反应速率为
(3)下列描述中能说明反应达到平衡状态的是
a.Y的体积分数在混合气体中保持不变
b.X、Y的反应速率比为1:1
c.容器内气体压强保持不变
d.容器内气体的总质量保持不变
e.生成1molY的同时消耗2molZ
Ⅰ.在某一容积为4L的密闭容器中,A、B、C、D四种物质的物质的量随时间的变化曲线如图所示,完成下列问题:
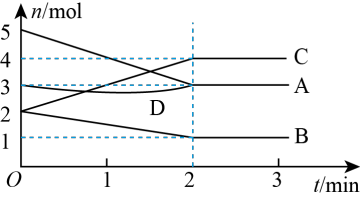
(1)该反应的化学方程式为
(2)前
 用A的浓度变化表示的化学反应速率为
用A的浓度变化表示的化学反应速率为Ⅱ.
 是一种常用的还原剂。一定条件下,反应
是一种常用的还原剂。一定条件下,反应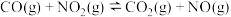 的速率方程为
的速率方程为 (k为速率常数,只与温度、催化剂有关。与浓度无关)。某温度下,该反应在不同浓度下反应速率如下表所示:
(k为速率常数,只与温度、催化剂有关。与浓度无关)。某温度下,该反应在不同浓度下反应速率如下表所示: |  | 反应速率 | |
| ① | 0.10 | 0.10 |  |
| ② | 0.20 | 0.10 | 2 |
| ③ | 0.20 | 0.20 | 4 |
(4)改变下列反应条件,反应速率增大的是___________(填字母)。
| A.降温 | B.缩小体积 | C.加入催化剂 | D.减压 |
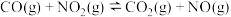 已经达到平衡状态的是
已经达到平衡状态的是A.
 的物质的量分数保持不变
的物质的量分数保持不变B.体系中气体颜色不变
C.等温等容,体系中气体密度保持不变
D.等温等压,体系压强不再发生变化
E.

 消耗的同时
消耗的同时
 生成
生成F.若反应在绝热体系中进行,体系温度不再变化
 2SO3 , 如果2min内SO2的浓度由6 mol/L下降为2 mol/L,那么,用SO2浓度变化来表示的化学反应速率为
2SO3 , 如果2min内SO2的浓度由6 mol/L下降为2 mol/L,那么,用SO2浓度变化来表示的化学反应速率为(2)反应N2+3H2
 2NH3 ΔH<0 ,达平衡后,不同时刻改变外界条件时正逆反应速率变化如图,请判断某时刻所改变的条件。
2NH3 ΔH<0 ,达平衡后,不同时刻改变外界条件时正逆反应速率变化如图,请判断某时刻所改变的条件。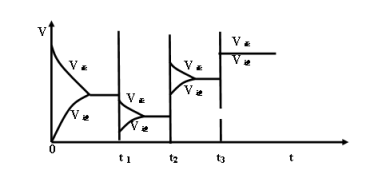
可能改变的外界条件:t1
 、
、 、CO等气体的处理对治理大气污染、建设生态文明具有重要意义。
、CO等气体的处理对治理大气污染、建设生态文明具有重要意义。(1)已知:


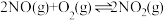
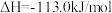
则
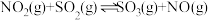 的
的
(2)在一定条件下,将
 与
与 以体积比1:2置于密闭容器中发生上述反应。下列能说明反应达到平衡状态的是
以体积比1:2置于密闭容器中发生上述反应。下列能说明反应达到平衡状态的是a.体系压强保持不变
b.混合气体的颜色保持不变
c.
 和NO的体积比保持不变
和NO的体积比保持不变d.每生成1mol
 的同时消耗1mol
的同时消耗1mol
【推荐2】已知反应:2SO2(g)+O2(g) 2SO3(g) ΔH=-Q kJ·mol-1。将2 molSO2和1 molO2通入体积为5 L的密闭容器中进行反应。反应在不同催化条件下进行,反应体系总压强随时间的变化如图所示。
2SO3(g) ΔH=-Q kJ·mol-1。将2 molSO2和1 molO2通入体积为5 L的密闭容器中进行反应。反应在不同催化条件下进行,反应体系总压强随时间的变化如图所示。
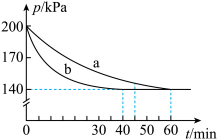
(1)由图可知,催化效率更佳的是曲线
A.SO2的转化率不再变化 B.体系温度不再变化
C.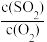 不再变化 D.混合气体平均分子量不再变化
不再变化 D.混合气体平均分子量不再变化
(2)观察曲线a,通过计算回答下列问题:
①60min内,用浓度变化表示O2的平均反应速率为
②平衡时,SO3的百分含量为
(3)反应2SO2(g)+O2(g) 2SO3(g)中,V2O5是催化剂的活性成分,有人提出:V2O5在对反应Ⅰ的催化循环过程中,经历了Ⅱ、Ⅲ两个反应阶段,如图所示:
2SO3(g)中,V2O5是催化剂的活性成分,有人提出:V2O5在对反应Ⅰ的催化循环过程中,经历了Ⅱ、Ⅲ两个反应阶段,如图所示:
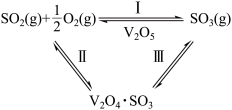
已知反应Ⅱ为SO2+V2O5 V2O4·SO3,则反应Ⅲ的化学方程式为
V2O4·SO3,则反应Ⅲ的化学方程式为
 Fe2O3+CO(g)⇌
Fe2O3+CO(g)⇌ Fe(s)+CO2(g),已知该反应在不同温度下的平衡常数如下:
Fe(s)+CO2(g),已知该反应在不同温度下的平衡常数如下:温度/℃ | 1000 | 1150 | 1300 |
平衡常数 | 4.0 | 3.7 | 3.5 |
请回答下列问题:
(1)该反应正反应是
(2)欲提高反应中CO的平衡转化率,可采取的措施是
A.减少Fe的量 B.增加Fe2O3的量 C.移出部分CO2 D.加入合适的催化剂 E.增大容器的容积
(3)在一个容积为1L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各2.0mol,反应经过5min后达到平衡.求该时间范围内反应的平均反应速率:v(CO2)=
(4)在恒温恒容下,下列各项可作为该反应达到平衡状态的标志的是
A.压强不再变化
B.气体密度不再变化
C.CO的消耗速率与CO2的消耗速率之比为1:1
D.气体平均摩尔质量不再变化
E.CO与CO2的浓度相等
 CH3OH(g)的起始浓度分别为:c(CO)=1mol·L-1,c(H2)=2.4mol·L-1,5min后达到平衡,CO的转化率为50%;若反应物的起始浓度分别为:c(CO)=4mol·L-1,c(H2)=amol·L-1,达到平衡后,c(CH3OH)=2mol·L-1,则a=
CH3OH(g)的起始浓度分别为:c(CO)=1mol·L-1,c(H2)=2.4mol·L-1,5min后达到平衡,CO的转化率为50%;若反应物的起始浓度分别为:c(CO)=4mol·L-1,c(H2)=amol·L-1,达到平衡后,c(CH3OH)=2mol·L-1,则a= 平衡常数与温度关系如表所示:
平衡常数与温度关系如表所示:| 温度(℃) | 360 | 440 | 520 |
| K | 0.036 | 0.010 | 0.0038 |
(2)为了增大X的转化率,宜采用的措施是_______(填写序号)
| A.升高温度 | B.增大压强 | C.使用高效催化剂 | D.分离Z |
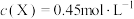 ,此时,反应是否达到平衡状态
,此时,反应是否达到平衡状态(4)在某容积固定的容器中进行上述反应,当X、Y起始物质的量一定时,仅改变一个外界条件对Z体积分数的影响如图所示(曲线Ⅰ为标准):
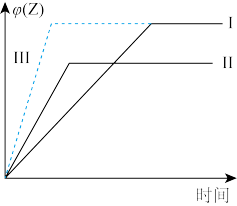
①曲线Ⅱ改变的条件是
②曲线Ⅲ改变的条件是
(1)达到平衡时, A2的转化率为
(2)达到平衡后,若向原容器中通入少量的氩气,A2的转化率将
(3)恒压的密闭容器中发生可逆反应2A2(g)+B2(g)⇌2C3(g) △H=-Q1 kJ/mol(Q1>0),在一定条件下达到化学平衡状态的标志是
A.v(A2):v(C3)=3:2
B.反应混合气体的密度不再变化
C.反应混合气体的平均摩尔质量不再变化
D.A2、B2两种反应物的转化率不再变化
E. A2、B2、C3三种物质的浓度相等
F.密闭容器内的压强不再变化
(4)改变某一条件,得到如图的变化规律(图中T表示温度,n表示物质的量),可得出的结论正确的是
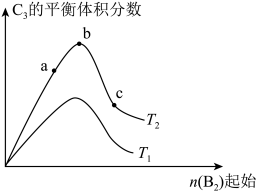
a.反应速率c>b>a
b.达到平衡时A2的转化率大小为:b>a>c
c.T2>T1
d.b点A2和B2的物质的量之比为2:1
(5)若将上述容器改为恒压容器,起始时加入2 molA2和1 molB2,500℃时充分反应达平衡后,放出热量Q4 kJ,则Q2



