减弱温室效应的方法之一是将CO2回收利用,科学家研究利用回收的CO2制取甲醛,反应的热化学方程式为CO2(g)+2H2(g HCHO(g)+H2O(g) ΔH。实验室在2L密闭容器中进行模拟上述合成HCHO的实验。T1℃时,将体积比为1∶2的CO2和H2混合气体充入容器中,每隔一定时间测得容器内气体压强如表所示:
HCHO(g)+H2O(g) ΔH。实验室在2L密闭容器中进行模拟上述合成HCHO的实验。T1℃时,将体积比为1∶2的CO2和H2混合气体充入容器中,每隔一定时间测得容器内气体压强如表所示:
已知:v(B)=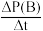 ,则反应开始10min内,用H2的压强变化表示该反应的平均反应速率为
,则反应开始10min内,用H2的压强变化表示该反应的平均反应速率为_____ kPa•min-1。
 HCHO(g)+H2O(g) ΔH。实验室在2L密闭容器中进行模拟上述合成HCHO的实验。T1℃时,将体积比为1∶2的CO2和H2混合气体充入容器中,每隔一定时间测得容器内气体压强如表所示:
HCHO(g)+H2O(g) ΔH。实验室在2L密闭容器中进行模拟上述合成HCHO的实验。T1℃时,将体积比为1∶2的CO2和H2混合气体充入容器中,每隔一定时间测得容器内气体压强如表所示:| 时间/min | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 压强/kPa | 1.08 | 0.96 | 0.88 | 0.82 | 0.80 | 0.80 | 0.80 |
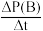 ,则反应开始10min内,用H2的压强变化表示该反应的平均反应速率为
,则反应开始10min内,用H2的压强变化表示该反应的平均反应速率为
2022高三·全国·专题练习 查看更多[1]
(已下线)专题14 速率计算专练
更新时间:2022-09-29 14:33:18
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】将等物质的量的A、B混合于5L的密闭容器中,发生反应: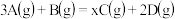 ,经5min后,测得D的浓度为
,经5min后,测得D的浓度为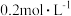 ,
, ,C的平均反应速率是
,C的平均反应速率是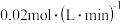 。
。 请写出计算过程
请写出计算过程 求:
求:
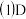 的平均反应速率
的平均反应速率_____ ;
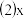 的值
的值_____ ;
 反应开始前放入容器中的A、B的物质的量
反应开始前放入容器中的A、B的物质的量_____ ;
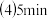 时B的物质的量浓度
时B的物质的量浓度_____ 。
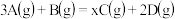 ,经5min后,测得D的浓度为
,经5min后,测得D的浓度为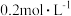 ,
, ,C的平均反应速率是
,C的平均反应速率是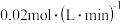 。
。 请写出计算过程
请写出计算过程 求:
求: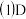 的平均反应速率
的平均反应速率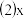 的值
的值 反应开始前放入容器中的A、B的物质的量
反应开始前放入容器中的A、B的物质的量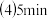 时B的物质的量浓度
时B的物质的量浓度
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】在温度保持不变的情况下,将一定量的NO2充入注射器中后封口,图乙是在拉伸或压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小且整个操作过程物质均为气态)。(已知:2NO2(g) N2O4(g)+Q)
N2O4(g)+Q)

在100℃时,将0.40mol的NO2气体充入2L的密闭容器中,每隔一定时间就对该容器内的物质进行分析,得到表中数据。
20~40s内,NO2的平均反应速率为_____ 。
 N2O4(g)+Q)
N2O4(g)+Q)
在100℃时,将0.40mol的NO2气体充入2L的密闭容器中,每隔一定时间就对该容器内的物质进行分析,得到表中数据。
| 时间/s | 0 | 20 | 40 | 60 | 80 | 100 |
| n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 | n5 |
| n(N2O4)/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 | 0.08 |
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
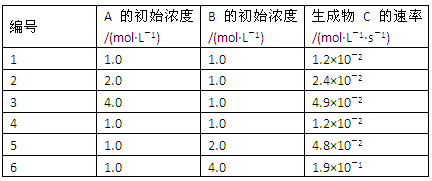
【推荐1】有一化学反应aA+bB=C,根据影响化学反应速率的因素可得v(C)=kcm(A)cn(B)。其中k是与温度有关的常数,为测k、m、n的值,在298 K时,将A、B溶液按不同的浓度混合,得到下列实验数据:
(1)根据上表可求得:m=_______ ,n=______ ,k=________ 。
(2) 当c(A)=c(B)=2.0mol/L时,用B表示的初始反应速率为___________________ 。
(1)根据上表可求得:m=
(2) 当c(A)=c(B)=2.0mol/L时,用B表示的初始反应速率为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
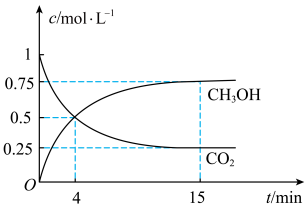
【推荐2】C、N、S的氧化物常会造成一些环境问题,科研工作者正在研究用各种化学方法来消除这些物质对环境的不利影响。在500℃下合成甲醇的反应原理为:CO2(g)+3H2(g) CH3OH(g)+H2O(g),在1 L 的密闭容器中,充入1 mol CO2和3 mol H2,压强为p0 ,测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示。(可逆反应的平衡常数可以用平衡浓度计算,也可以用平衡分压Kp代替平衡浓度,计算分压=总压×物质的量分数)
CH3OH(g)+H2O(g),在1 L 的密闭容器中,充入1 mol CO2和3 mol H2,压强为p0 ,测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示。(可逆反应的平衡常数可以用平衡浓度计算,也可以用平衡分压Kp代替平衡浓度,计算分压=总压×物质的量分数)
①反应进行到4 min 时,υ(正)__ (填“>”“<”或“=”)υ(逆)。0~4 min,H2的平均反应速率υ(H2)=__ mol·L-1·min-1。
②CO2平衡时的体积分数为_____ ,该温度下Kp为_____ (用含有p0的式子表示)。
 CH3OH(g)+H2O(g),在1 L 的密闭容器中,充入1 mol CO2和3 mol H2,压强为p0 ,测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示。(可逆反应的平衡常数可以用平衡浓度计算,也可以用平衡分压Kp代替平衡浓度,计算分压=总压×物质的量分数)
CH3OH(g)+H2O(g),在1 L 的密闭容器中,充入1 mol CO2和3 mol H2,压强为p0 ,测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示。(可逆反应的平衡常数可以用平衡浓度计算,也可以用平衡分压Kp代替平衡浓度,计算分压=总压×物质的量分数)①反应进行到4 min 时,υ(正)
②CO2平衡时的体积分数为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】(1)反应A+3B=2C+2D在四种不同情况下的反应速率分别为:
①v(A)=0.15 mol/(L·s); ②v(B)=0.6 mol/(L·s);
③v(C)=0.4 mol/(L·s); ④v(D)=0.45 mol/(L·s)。
该反应进行的快慢顺序为________________ 。
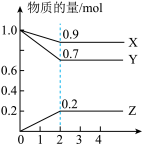
(2)某温度时,在2L容器中X、Y、Z三种物质的量随时间的变化曲线如图所示。由图中数据分析,该反应的化学方程式为_______________________ 。反应开始至2min,Z的平均反应速率为_______________________ 。
①v(A)=0.15 mol/(L·s); ②v(B)=0.6 mol/(L·s);
③v(C)=0.4 mol/(L·s); ④v(D)=0.45 mol/(L·s)。
该反应进行的快慢顺序为
(2)某温度时,在2L容器中X、Y、Z三种物质的量随时间的变化曲线如图所示。由图中数据分析,该反应的化学方程式为

您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】一定温度下,将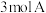 气体和
气体和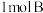 气体通入一容积固定为2L的密闭容器中,发生如下反应:
气体通入一容积固定为2L的密闭容器中,发生如下反应: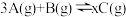 ,请回答下列问题:
,请回答下列问题:
(1)反应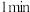 时测得剩余
时测得剩余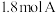 ,C的浓度为
,C的浓度为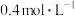 ,则
,则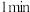 内,B的平均反应速率为
内,B的平均反应速率为________ ; 为
为________ 。
(2)若反应经 达到平衡,平衡时C的浓度
达到平衡,平衡时C的浓度________ (填“大于”“小于”或“等于”)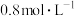 。
。
(3)若已知达到平衡时,该容器内混合气体总压强为p,混合气体起始压强为 ,请用
,请用 、
、 来表示达到平衡时反应物A的转化率
来表示达到平衡时反应物A的转化率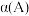 为
为________ 。
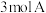 气体和
气体和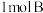 气体通入一容积固定为2L的密闭容器中,发生如下反应:
气体通入一容积固定为2L的密闭容器中,发生如下反应: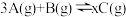 ,请回答下列问题:
,请回答下列问题:(1)反应
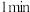 时测得剩余
时测得剩余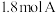 ,C的浓度为
,C的浓度为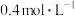 ,则
,则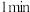 内,B的平均反应速率为
内,B的平均反应速率为 为
为(2)若反应经
 达到平衡,平衡时C的浓度
达到平衡,平衡时C的浓度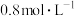 。
。(3)若已知达到平衡时,该容器内混合气体总压强为p,混合气体起始压强为
 ,请用
,请用 、
、 来表示达到平衡时反应物A的转化率
来表示达到平衡时反应物A的转化率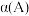 为
为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐3】某温度下,在容积为2 L的密闭容器中进行如下反应:
A(g)+2B(g) 3C(g)+nD(g),开始时A为4 mol,B为6 mol。5 min时测得生成C 3 mol,用D表示的化学反应速率v(D)为0.2 mol·L−1·min−1。已知该温度下,反应的平衡常数K=1。试回答下列问题:
3C(g)+nD(g),开始时A为4 mol,B为6 mol。5 min时测得生成C 3 mol,用D表示的化学反应速率v(D)为0.2 mol·L−1·min−1。已知该温度下,反应的平衡常数K=1。试回答下列问题:
(1)5 min时B的物质的量浓度为_______________ 。
(2)5 min内用A表示的化学反应速率v(A)为_______________ 。
(3)化学方程式中n为_______________ 。
(4)5 min时该反应是否达到平衡?请计算说明。_______________
A(g)+2B(g)
 3C(g)+nD(g),开始时A为4 mol,B为6 mol。5 min时测得生成C 3 mol,用D表示的化学反应速率v(D)为0.2 mol·L−1·min−1。已知该温度下,反应的平衡常数K=1。试回答下列问题:
3C(g)+nD(g),开始时A为4 mol,B为6 mol。5 min时测得生成C 3 mol,用D表示的化学反应速率v(D)为0.2 mol·L−1·min−1。已知该温度下,反应的平衡常数K=1。试回答下列问题:(1)5 min时B的物质的量浓度为
(2)5 min内用A表示的化学反应速率v(A)为
(3)化学方程式中n为
(4)5 min时该反应是否达到平衡?请计算说明。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】将等物质的量的A、B混合于2 L的密闭容器中,发生反应: 3A(g)+B(g)  3C(g)+2D(g),经5 min后,测得D的浓度为0.5 mol·L-1,n(A)∶n(B)=3∶5.求:
3C(g)+2D(g),经5 min后,测得D的浓度为0.5 mol·L-1,n(A)∶n(B)=3∶5.求:
(1)5 min 末C的浓度是多少_______ ?
(2)这5 min 内B的平均反应速率是多少_______ ?
(3)反应开始前容器中的A的物质的量是多少_______ ?
 3C(g)+2D(g),经5 min后,测得D的浓度为0.5 mol·L-1,n(A)∶n(B)=3∶5.求:
3C(g)+2D(g),经5 min后,测得D的浓度为0.5 mol·L-1,n(A)∶n(B)=3∶5.求:(1)5 min 末C的浓度是多少
(2)这5 min 内B的平均反应速率是多少
(3)反应开始前容器中的A的物质的量是多少
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】把1mol X气体和0.5mol Y气体混合于2L密闭容器中,发生如下反应:3X(g)+Y(g)⇌nZ(g)+2W(g),2min末生成0.2mol W,若测得以Z的物质的量浓度变化表示的平均反应速率为0.1mol/(L·min),试计算:
(1)前2min内,用X表示的平均反应速率为__________
(2)2min末时Y的转化率为__________ ,Z的浓度为__________
(3)化学方程式中Z的化学计量数n为__________
(1)前2min内,用X表示的平均反应速率为
(2)2min末时Y的转化率为
(3)化学方程式中Z的化学计量数n为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】按要求回答问题:
(1)已知氢气燃烧生成2mol液态水时放出的热量为572kJ。请回答下列问题:
①生成物能量总和________ (填“大于”“小于”或“等于”)反应物能量总和。
②反应2H2(g)+O2(g)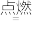 2H2O(L)的能量变化如图(图中各微粒前的系数表示物质的量)所示。已知拆开1mol H2、1mol O2和1mol H—O中的化学键分别需要消耗436kJ、496kJ和463kJ的能量。则反应过程(Ⅱ)
2H2O(L)的能量变化如图(图中各微粒前的系数表示物质的量)所示。已知拆开1mol H2、1mol O2和1mol H—O中的化学键分别需要消耗436kJ、496kJ和463kJ的能量。则反应过程(Ⅱ)________ (填“吸收”或“放出”)________ kJ。

(2)一定温度下,在容积为2L的密闭容器中进行反应:aN(g)⇌bM(g)+cP(g),M、N、P的物质的量随时间变化的曲线如图所示:

①反应化学方程式中各物质的系数比为a∶b∶c=_________ 。
②1min到3min这段时刻,以M的浓度变化表示的平均反应速率为:__________ 。
③下列叙述中能说明上述反应达到平衡状态的是_____________ 。
A 反应中当M与N的物质的量相等时
B P的质量不随时间变化而变化
C 混合气体的总物质的量不随时间变化而变化
D 单位时间内每消耗a mol N,同时消耗b mol M
E 混合气体的压强不随时间的变化而变化
F M的物质的量浓度保持不变
④达到平衡时,在相同温度下容器内混合气体的压强与反应前的压强之比为________
(1)已知氢气燃烧生成2mol液态水时放出的热量为572kJ。请回答下列问题:
①生成物能量总和
②反应2H2(g)+O2(g)
 2H2O(L)的能量变化如图(图中各微粒前的系数表示物质的量)所示。已知拆开1mol H2、1mol O2和1mol H—O中的化学键分别需要消耗436kJ、496kJ和463kJ的能量。则反应过程(Ⅱ)
2H2O(L)的能量变化如图(图中各微粒前的系数表示物质的量)所示。已知拆开1mol H2、1mol O2和1mol H—O中的化学键分别需要消耗436kJ、496kJ和463kJ的能量。则反应过程(Ⅱ)
(2)一定温度下,在容积为2L的密闭容器中进行反应:aN(g)⇌bM(g)+cP(g),M、N、P的物质的量随时间变化的曲线如图所示:

①反应化学方程式中各物质的系数比为a∶b∶c=
②1min到3min这段时刻,以M的浓度变化表示的平均反应速率为:
③下列叙述中能说明上述反应达到平衡状态的是
A 反应中当M与N的物质的量相等时
B P的质量不随时间变化而变化
C 混合气体的总物质的量不随时间变化而变化
D 单位时间内每消耗a mol N,同时消耗b mol M
E 混合气体的压强不随时间的变化而变化
F M的物质的量浓度保持不变
④达到平衡时,在相同温度下容器内混合气体的压强与反应前的压强之比为
您最近一年使用:0次

 xC(g)+2D(g),经过5分钟后,测得D的浓度为0.5mol/L,C的平均反应速率是0.1mol/(L·min),且c(A):c(B)=3:5求:
xC(g)+2D(g),经过5分钟后,测得D的浓度为0.5mol/L,C的平均反应速率是0.1mol/(L·min),且c(A):c(B)=3:5求:  xC(g)。2min时反应达到平衡状态(温度不变),剩余了0.8molB,并测得C的浓度为0.4mol/L,请填写下列空白:
xC(g)。2min时反应达到平衡状态(温度不变),剩余了0.8molB,并测得C的浓度为0.4mol/L,请填写下列空白:

