某化学兴趣小组为探究 SO2的性质,按如图所示装置进行实验。

请回答下列问题:
(1)装置 A 中盛放浓硫酸的仪器名称是_______ ,A 中化学方程式为_______ 。
(2)反应后,装置 B 中发生反应的离子方程式_______ , 装置 C 中的现象是_______ ,表现了SO2具有_______ 性;装置D 中现象是_______ ,发生反应的化学方程式_______ 。
(3)装置E中的现象是_______ ,表现了 SO2具有_______ 性,F装置的作用是_______ ,漏斗的作用是_______ 。

请回答下列问题:
(1)装置 A 中盛放浓硫酸的仪器名称是
(2)反应后,装置 B 中发生反应的离子方程式
(3)装置E中的现象是
更新时间:2022-10-01 08:34:47
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】某化学研究小组利用如图所示装置探究SO2与FeCl3溶液的反应。

(1)实验过程中需要配制100mL 1mol•L-1 FeCl3溶液,所需要的玻璃仪器:烧杯、量筒、玻璃棒、_______ 。
(2)制备二氧化硫的化学方程式_______ ,使用70%硫酸而不用稀硫酸的原因_______ 。
(3)该小组同学向5mL1mol•L-1 FeCl3溶液中通入足量的SO2,溶液最终呈浅绿色,写出发生反应的离子方程式式_______ ;
(4)打开分液漏斗活塞,逐滴加入NaOH稀溶液,则试管中产生的实验现象是_______
(5)若用NaOH溶液吸收尾气,请写出反应的离子方程式_______

(1)实验过程中需要配制100mL 1mol•L-1 FeCl3溶液,所需要的玻璃仪器:烧杯、量筒、玻璃棒、
(2)制备二氧化硫的化学方程式
(3)该小组同学向5mL1mol•L-1 FeCl3溶液中通入足量的SO2,溶液最终呈浅绿色,写出发生反应的离子方程式式
(4)打开分液漏斗活塞,逐滴加入NaOH稀溶液,则试管中产生的实验现象是
(5)若用NaOH溶液吸收尾气,请写出反应的离子方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】根据要求完成下列实验过程(a、b为弹簧夹,加热及固定装置已略去)。
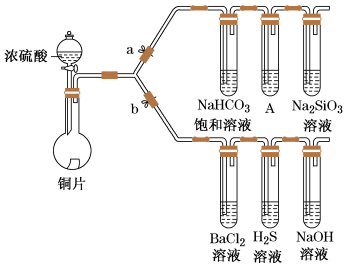
(1)验证碳、硅非金属性的相对强弱(已知酸性:亚硫酸>碳酸)。
①连接仪器、________ 、加药品后,打开a、关闭b,然后滴入浓硫酸,加热。
②铜与浓硫酸反应的化学方程式是________ ,装置A中试剂是_______ 。
③能说明碳的非金属性比硅强的实验现象是________ 。
(2)验证SO2的氧化性、还原性和酸性氧化物的通性。
①在(1)①操作后打开b,关闭a。
②H2S溶液中有浅黄色浑浊出现,化学方程式是______ 。
③BaCl2溶液中无明显现象,将其分成两份,分别滴加氯水和氨水均产生沉淀。则沉淀的化学式分别为___________ 、__________ 。

(1)验证碳、硅非金属性的相对强弱(已知酸性:亚硫酸>碳酸)。
①连接仪器、
②铜与浓硫酸反应的化学方程式是
③能说明碳的非金属性比硅强的实验现象是
(2)验证SO2的氧化性、还原性和酸性氧化物的通性。
①在(1)①操作后打开b,关闭a。
②H2S溶液中有浅黄色浑浊出现,化学方程式是
③BaCl2溶液中无明显现象,将其分成两份,分别滴加氯水和氨水均产生沉淀。则沉淀的化学式分别为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】某化学兴趣小组同学利用如图所示装置(夹持及加热装置已略去,装置气密性良好)探究SO2的性质(实验前已事先除去装置中的空气)。请回答下列问题:
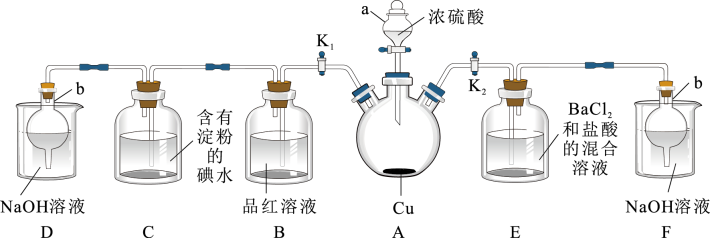
查阅资料得知浓硫酸的沸点为338 ℃,酒精灯火焰的温度为400~500 ℃。
(1)仪器a的名称____ 。
(2)装置D和F的作用是_____ 。
(3)加热时,装置A中反应的化学方程式____ 。
(4)打开K1,关闭K2,加热装置A一段时间后,装置B中的现象是____ ,若要证明其过程是可逆的,还需要的操作是____ ;装置C中溶液由蓝色变为无色,为了证实该过程中SO2已被氧化,具体的实验操作及现象是____ 。
(5)关闭K1,打开K2,用酒精灯加热装置A,观察到装置E中的现象是有白色沉淀产生,白色沉淀的成分是____ ,生成白色沉淀的原因可能是____ (填序号)。
a.SO2与BaCl2溶液反应生成了白色沉淀
b.BaCl2溶液与硫酸蒸气反应生成了白色沉淀
(6)将装置A中产生的SO2气体通入足量双氧水中,然后加入足量BaCl2溶液,经过滤。洗涤。干燥得到4.66 g沉淀。据此推知SO2气体的体积为____ mL(标准状况)。

查阅资料得知浓硫酸的沸点为338 ℃,酒精灯火焰的温度为400~500 ℃。
(1)仪器a的名称
(2)装置D和F的作用是
(3)加热时,装置A中反应的化学方程式
(4)打开K1,关闭K2,加热装置A一段时间后,装置B中的现象是
(5)关闭K1,打开K2,用酒精灯加热装置A,观察到装置E中的现象是有白色沉淀产生,白色沉淀的成分是
a.SO2与BaCl2溶液反应生成了白色沉淀
b.BaCl2溶液与硫酸蒸气反应生成了白色沉淀
(6)将装置A中产生的SO2气体通入足量双氧水中,然后加入足量BaCl2溶液,经过滤。洗涤。干燥得到4.66 g沉淀。据此推知SO2气体的体积为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】下图是实验室制取SO2并验证SO2的某些性质的装置,请回答:
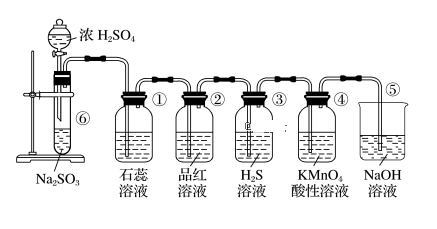
(1)在⑥中发生反应的化学方程式为_____________________ 。
(2)①中的实验现象为石蕊溶液____________ ,此实验证明SO2具有____________ 的性质。
(3)②中的品红溶液________ ,证明SO2具有____________ 性。。
(4)③中的实验现象是_______________________ ,证明SO2有____________ 性。
(5)④中的实验现象是______________________ ,证明SO2有_____________ 性。
(6)⑤装置的作用是___________________________ ,该反应的离子方程式为________ 。

(1)在⑥中发生反应的化学方程式为
(2)①中的实验现象为石蕊溶液
(3)②中的品红溶液
(4)③中的实验现象是
(5)④中的实验现象是
(6)⑤装置的作用是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】硫酸亚铁可用于治疗缺铁性贫血症。某兴趣小组为探究硫酸亚铁的分解产物,设计实验方案如下:
①先按要求搭配好装置再检查装置的气密性;
②打开弹簧夹K1和K2,向装置中缓缓通入N2一段时间后,加热装有 的硬质玻璃管;
的硬质玻璃管;
③观察到的实验现象:A装置中有红棕色固体出现,B中有白色沉淀生成,C中品红溶液褪色;
④冷却后A装置中剩余固体的质量为10.88g。

(1)根据B、C装置中的实验现象可推测分解产物中含有___________ 和___________ 。
(2)将装置B、C顺序颠倒能否达到原来的实验目的___________ (填“能”或“不能”),原因是___________ 。
(3)D装置中发生的主要反应的离子方程式是___________ 。
(4)通过计算确定已分解的FeSO4物质的量(写出计算过程)___________ 。
①先按要求搭配好装置再检查装置的气密性;
②打开弹簧夹K1和K2,向装置中缓缓通入N2一段时间后,加热装有
 的硬质玻璃管;
的硬质玻璃管;③观察到的实验现象:A装置中有红棕色固体出现,B中有白色沉淀生成,C中品红溶液褪色;
④冷却后A装置中剩余固体的质量为10.88g。

(1)根据B、C装置中的实验现象可推测分解产物中含有
(2)将装置B、C顺序颠倒能否达到原来的实验目的
(3)D装置中发生的主要反应的离子方程式是
(4)通过计算确定已分解的FeSO4物质的量(写出计算过程)
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】二氧化硫具有漂白性,工业上常用二氧化硫来漂白纸浆、毛、丝、草帽等。此外二氧化硫还具有还原性,可用作防腐剂,甲组同学拟利用Mg粉与浓硫酸反应制取22.4L (标准状况下)SO2。实验方案设计如下:取24g镁粉与100Ml98%的浓硫酸(含2.204molH2SO4)混合,加热充分反应,待Mg粉全部溶解后,干燥并收集气体。
(1)写出Mg粉与浓硫酸反应制备SO2的化学方程式:_______ ;
(2)乙组同学认为:按甲组同学实验方案无法达到实验目的,并且制得气体应该含有杂质,该杂质为_______ (填化学式);
(3)为了检验甲组同学所制气体的成分,乙组同学按甲组同学的实验方案制备气体,并设计了如图所示的实验装置进行检验(已知酸性高锰酸钾溶液及B中试剂均过量),其中C是CuO固体,D是无水CuSO4。

①A中试剂是品红溶液,作用是_______ ;
②B中所装试剂为_______ ;
③证明气体中混有杂质气体的实验现象是:_______ ;
(4)将二氧化硫气体通入FeCl3溶液中反应一段时间后,取少量生成的溶液,分成两份,一份滴加KSCN溶液,溶液未变红色,另一份滴加稀盐酸酸化的BaCl2溶液,生成了白色沉淀,请写出二氧化硫气体通入FeCl3溶液时发生的离子反应方程式_______ 。
(1)写出Mg粉与浓硫酸反应制备SO2的化学方程式:
(2)乙组同学认为:按甲组同学实验方案无法达到实验目的,并且制得气体应该含有杂质,该杂质为
(3)为了检验甲组同学所制气体的成分,乙组同学按甲组同学的实验方案制备气体,并设计了如图所示的实验装置进行检验(已知酸性高锰酸钾溶液及B中试剂均过量),其中C是CuO固体,D是无水CuSO4。

①A中试剂是品红溶液,作用是
②B中所装试剂为
③证明气体中混有杂质气体的实验现象是:
(4)将二氧化硫气体通入FeCl3溶液中反应一段时间后,取少量生成的溶液,分成两份,一份滴加KSCN溶液,溶液未变红色,另一份滴加稀盐酸酸化的BaCl2溶液,生成了白色沉淀,请写出二氧化硫气体通入FeCl3溶液时发生的离子反应方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】实验室可用图中装置(略去部分夹持仪器)制取 并验证其性质。
并验证其性质。___________ ,装置A中发生反应的化学方程式为___________ 。
(2)仪器组装完成后,关闭两端活塞,向装置B的长颈漏斗内注入液体至形成一段液柱,若___________ ,则整个装置气密性良好。
(3)装置B的作用之一是通过观察产生气泡的多少判断 生成的快慢,其中的液体最好选择
生成的快慢,其中的液体最好选择___________ (填序号)。
a.蒸馏水 b.饱和 溶液 c.饱和
溶液 c.饱和 溶液 d.饱和
溶液 d.饱和 溶液
溶液
(4)C试管中的试剂可以验证二氧化硫的氧化性,现象为___________ 。
(5)为验证二氧化硫的还原性,充分反应后,取试管D中的溶液分成三份,分别进行实验:
方案I:向第一份溶液中加入 溶液,有白色沉淀生成;
溶液,有白色沉淀生成;
方案II:向第二份溶液中加入 溶液,有白色沉淀生成;
溶液,有白色沉淀生成;
方案III:向第三份溶液中加入 溶液,有产生白色沉淀。
溶液,有产生白色沉淀。
上述方案中合理的是方案___________ (填“I”“II”或“III”)。
 并验证其性质。
并验证其性质。
(2)仪器组装完成后,关闭两端活塞,向装置B的长颈漏斗内注入液体至形成一段液柱,若
(3)装置B的作用之一是通过观察产生气泡的多少判断
 生成的快慢,其中的液体最好选择
生成的快慢,其中的液体最好选择a.蒸馏水 b.饱和
 溶液 c.饱和
溶液 c.饱和 溶液 d.饱和
溶液 d.饱和 溶液
溶液(4)C试管中的试剂可以验证二氧化硫的氧化性,现象为
(5)为验证二氧化硫的还原性,充分反应后,取试管D中的溶液分成三份,分别进行实验:
方案I:向第一份溶液中加入
 溶液,有白色沉淀生成;
溶液,有白色沉淀生成;方案II:向第二份溶液中加入
 溶液,有白色沉淀生成;
溶液,有白色沉淀生成;方案III:向第三份溶液中加入
 溶液,有产生白色沉淀。
溶液,有产生白色沉淀。上述方案中合理的是方案
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】z物质的类别和核心元素的化合价是研究物质性质的两个重要角度。如图所示是硫及其部分化合物的“价类二维图”,回答下列问题:

(1)D的化学式为______ ; 属于
属于______ (填“共价”或“离子”)化合物。
(2)足量B通入溴水中的现象是__________________ 。
(3)C(C为钠盐)和D的浓溶液可以少量制取B,写出该反应的化学方程式:__________________ 。
(4)欲制备 ,从氧化还原角度分析,下列选项中合理的是______(填字母)。
,从氧化还原角度分析,下列选项中合理的是______(填字母)。
(5)将A的溶液与B混合,可生成淡黄色固体,写出该反应的化学方程式并用双线桥表示该过程中转移的电子数:__________________ 。
(6)某地收集的雨水样品在不同时间测得pH如表所示,根据价类二维图分析该雨水样品随时间变化酸性逐渐增强的原因:__________________ 。

(1)D的化学式为
 属于
属于(2)足量B通入溴水中的现象是
(3)C(C为钠盐)和D的浓溶液可以少量制取B,写出该反应的化学方程式:
(4)欲制备
 ,从氧化还原角度分析,下列选项中合理的是______(填字母)。
,从氧化还原角度分析,下列选项中合理的是______(填字母)。A. | B. |
C. | D. |
(6)某地收集的雨水样品在不同时间测得pH如表所示,根据价类二维图分析该雨水样品随时间变化酸性逐渐增强的原因:
| 时间/h | 0 | 2 | 4 | 6 | 8 | 10 |
| pH | 5.0 | 4.8 | 4.5 | 4.3 | 4.2 | 4.0 |
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】海洋资源的综合利用是21世纪海洋开发利用的重点发展领域之一、从海水中可以制取氯、溴、镁等多种化工产品。在元素周期表中,溴(Br)位于第四周期,与Cl同主族。氯气可用于海水提溴,其工艺流程如下:

(1)进入吹出塔前海水中的 与
与 发生反应的离子方程式为
发生反应的离子方程式为_______ 。
(2)已知: 具有较强的氧化性,可氧化
具有较强的氧化性,可氧化 ,从吸收塔流出的溶液主要含
,从吸收塔流出的溶液主要含____ (填离子符号)。
(3)两次通入 的目的是富集浓缩溴,最终每获得
的目的是富集浓缩溴,最终每获得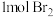 ,理论上需消耗
,理论上需消耗_______ 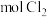 。
。
(4)某同学利用如图所示装置模拟吹出塔、吸收塔的实验,请回答下列问题:

①进行吹出塔中实验时,应关闭活塞_______ ,打开活塞_______ 。
②可根据_______ (填现象),简单判断热空气的流速,通入热空气能吹出 的原因是
的原因是_______ 。
③装置B中要先通入 ,反应完全后再通入
,反应完全后再通入 ,简单判断通入的
,简单判断通入的 已反应完全的依据:
已反应完全的依据:____ 。
(5)下列实验或事实能说明得电子能力Cl强于Br的是_______ (填标号)。
A.将 通入KBr溶液中可制得
通入KBr溶液中可制得
B.常温常压下, 为气态,
为气态, 为液态
为液态
C.HBr约500℃开始分解,HCl约1000℃开始缓慢分解

(1)进入吹出塔前海水中的
 与
与 发生反应的离子方程式为
发生反应的离子方程式为(2)已知:
 具有较强的氧化性,可氧化
具有较强的氧化性,可氧化 ,从吸收塔流出的溶液主要含
,从吸收塔流出的溶液主要含(3)两次通入
 的目的是富集浓缩溴,最终每获得
的目的是富集浓缩溴,最终每获得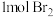 ,理论上需消耗
,理论上需消耗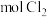 。
。(4)某同学利用如图所示装置模拟吹出塔、吸收塔的实验,请回答下列问题:

①进行吹出塔中实验时,应关闭活塞
②可根据
 的原因是
的原因是③装置B中要先通入
 ,反应完全后再通入
,反应完全后再通入 ,简单判断通入的
,简单判断通入的 已反应完全的依据:
已反应完全的依据:(5)下列实验或事实能说明得电子能力Cl强于Br的是
A.将
 通入KBr溶液中可制得
通入KBr溶液中可制得
B.常温常压下,
 为气态,
为气态, 为液态
为液态C.HBr约500℃开始分解,HCl约1000℃开始缓慢分解
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】硫元素是动植物生长不可缺少的元素,广泛存在于自然界中。实验室常用下列装置来进行铜跟浓硫酸反应等一系列实验。 生成所依据的现象是
生成所依据的现象是__________ ,甲装置中发生的主要反应的化学方程式是__________ ,在此反应中,浓硫酸所体现的性质是__________ 、________________ ;该反应中若有 参加反应,则被还原的
参加反应,则被还原的 的物质的量为
的物质的量为_______  ;
;
(2)若铜片还有剩余,硫酸________ (填“有”或“没有”)消耗完毕.其理由是________________ ;
(3)浸有碱液的棉花的作用是__________ ;
(4)写出 转化为
转化为 的化学方程式,
的化学方程式,__________ 、__________ 。

 生成所依据的现象是
生成所依据的现象是 参加反应,则被还原的
参加反应,则被还原的 的物质的量为
的物质的量为 ;
;(2)若铜片还有剩余,硫酸
(3)浸有碱液的棉花的作用是
(4)写出
 转化为
转化为 的化学方程式,
的化学方程式,
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】为探究氯气的性质,某兴趣小组设计如下实验:

(1)在A中圆底烧瓶内发生反应的化学方程式:___________ 。装置B中饱和食盐水的作用是___________ , 装置C中添加的试剂为: ___________ 。
(2)点燃A处酒精灯, 一段时间后,取出装置D,将烧红的铁丝伸入D中,可观察到___________ ,反应的化学方程式:___________ 。
(3)有同学提出可用饱和Na2SO3溶液代替NaOH溶液吸收多余的氯气, 其原因是____________ (用离子方程式表示)。
(4)实验室里迅速制备少量氯气可利用以下反应,该反应中浓盐酸体现___________ 性和酸性。2KMnO4+ 16HCl(浓) =2KCl+2MnCl2+5Cl2↑+8H2O用双线桥标出该反应中电子转移的方向和数目___________ 。

(1)在A中圆底烧瓶内发生反应的化学方程式:
(2)点燃A处酒精灯, 一段时间后,取出装置D,将烧红的铁丝伸入D中,可观察到
(3)有同学提出可用饱和Na2SO3溶液代替NaOH溶液吸收多余的氯气, 其原因是
(4)实验室里迅速制备少量氯气可利用以下反应,该反应中浓盐酸体现
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】二氧化氯(ClO2)是一种黄绿色有刺激性气味的气体。与Cl2的氧化性相近,可用于自来水消毒。为检测二氧化氯能否与KI溶液反应,某兴趣小组设计了下述实验(实验装置如图所示,且气密性良好,D中稳定剂不能与Cl2反应)。回答下列问题:

(1)盛放稀盐酸仪器的名称为_______ 。
(2)打开B的活塞,A中发生反应,且产物有ClO2、Cl2等,该反应的化学方程式为_______ 。
(3)关闭B的活塞,ClO2在D中被稳定剂完全吸收生成NaClO,此时观察到F中溶液的颜色不变,则装置C的作用是_______ 。
(4)已知在酸性条件下NaClO2可发生反应生成NaCl并放出ClO2,反应的离子方程式为_______ 。
(5)自来水厂用碘量法检测水中ClO2的浓度,其实验操作如下:取300.0 mL的水样,酸化,加入足量的碘化钾反应,再用0.2000 mol/L Na2S2O3溶液和生成的碘单质反应(反应的化学方程式为:2ClO2+10I-+8H+=5I2+2Cl- +4H2O、I2+2S2O =2I- +S4O
=2I- +S4O ),恰好完全反应时用去25.00 mL Na2S2O3溶液,测得该水样中的ClO2含量为
),恰好完全反应时用去25.00 mL Na2S2O3溶液,测得该水样中的ClO2含量为_______ mg/L。
(6)该小组同学还制得了ClO2的水溶液,以探究FeI2的还原性。他们进行了如下实验:取一定量的FeI2溶液,向其中滴加ClO2的水溶液。某同学对FeI2反应后的产物的成分(不考虑Cl- )提出了如下假设:
假设1:I2和Fe2+;
假设2:Fe3+、I-;
假设3:Fe3+、I2;
假设4:Fe2+、Fe3+、I2
其中假设_______ (填“1”“2”“3”或“4”)错误,理由是_______ 。

(1)盛放稀盐酸仪器的名称为
(2)打开B的活塞,A中发生反应,且产物有ClO2、Cl2等,该反应的化学方程式为
(3)关闭B的活塞,ClO2在D中被稳定剂完全吸收生成NaClO,此时观察到F中溶液的颜色不变,则装置C的作用是
(4)已知在酸性条件下NaClO2可发生反应生成NaCl并放出ClO2,反应的离子方程式为
(5)自来水厂用碘量法检测水中ClO2的浓度,其实验操作如下:取300.0 mL的水样,酸化,加入足量的碘化钾反应,再用0.2000 mol/L Na2S2O3溶液和生成的碘单质反应(反应的化学方程式为:2ClO2+10I-+8H+=5I2+2Cl- +4H2O、I2+2S2O
 =2I- +S4O
=2I- +S4O ),恰好完全反应时用去25.00 mL Na2S2O3溶液,测得该水样中的ClO2含量为
),恰好完全反应时用去25.00 mL Na2S2O3溶液,测得该水样中的ClO2含量为(6)该小组同学还制得了ClO2的水溶液,以探究FeI2的还原性。他们进行了如下实验:取一定量的FeI2溶液,向其中滴加ClO2的水溶液。某同学对FeI2反应后的产物的成分(不考虑Cl- )提出了如下假设:
假设1:I2和Fe2+;
假设2:Fe3+、I-;
假设3:Fe3+、I2;
假设4:Fe2+、Fe3+、I2
其中假设
您最近一年使用:0次



