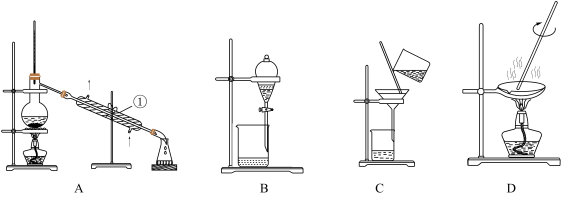
《肘后备急方•治寒热诸疟方》中记载“青蒿一握,以水二升渍,绞取汁,尽服之”。我国科学家屠呦呦受此启发,成功提取了青蒿素,获得了2015年诺贝尔生理学或医学奖。
已知:①青蒿素可溶于乙醇(分子式为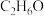 )、乙醚,难溶于水,受热不稳定;
)、乙醚,难溶于水,受热不稳定;
②不同物质的沸点:
(1)上述水、乙醇、乙醚三种物质中,属于电解质是_______ ,属于非电解质的是_______ 。
(2)实验室酒精灯燃烧时发生反应的化学方程式:_______ 。
(3)选择萃取青蒿素的试剂是_______ ﹐你选择的理由是_______ 。
(4)为了加快青蒿素的浸出速率,可采取的措施_______ 。
(5)根据青蒿素的性质,请以黄花蒿(黄花蒿是一种含有青蒿素的植物)为原料,设计一个合理提取青蒿素的实验方案___________ 。
已知:①青蒿素可溶于乙醇(分子式为
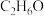 )、乙醚,难溶于水,受热不稳定;
)、乙醚,难溶于水,受热不稳定;②不同物质的沸点:
| 物质 | 水 | 乙醇 | 乙醚 |
| 沸点/℃ | 100 | 78.3 | 34.6 |
(2)实验室酒精灯燃烧时发生反应的化学方程式:
(3)选择萃取青蒿素的试剂是
(4)为了加快青蒿素的浸出速率,可采取的措施
(5)根据青蒿素的性质,请以黄花蒿(黄花蒿是一种含有青蒿素的植物)为原料,设计一个合理提取青蒿素的实验方案
更新时间:2022/10/10 17:44:47
|
相似题推荐
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐1】现有下列电解质:①稀硫酸②冰醋酸③Ba(OH)2④石炭酸⑤氨水⑥NaHSO4⑦盐酸⑧明矾⑨钾钠合金。
(1)(用序号填空)其中可以导电的有___ ,属于弱电解质的是____ ,属于盐的有___ 。
(2)写出⑥在融化状态下的电离方程式:______ 。
(3)写出将③的水溶液逐滴加入到一定量的⑧溶液中至沉淀质量最大时的离子方程式:___ 。
(1)(用序号填空)其中可以导电的有
(2)写出⑥在融化状态下的电离方程式:
(3)写出将③的水溶液逐滴加入到一定量的⑧溶液中至沉淀质量最大时的离子方程式:
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐2】Ⅰ以下是实验室及生活中常见的一些物质:①液氯、②稀H2SO4、③CO2、④石灰水、⑤氯水、⑥氢氧化钠溶液、⑦CaO、⑧酒精、⑨Cu,请根据要求填空:
(1)属于酸性氧化物的是______ ;属于电解质的是________ 。(填序号)
(2)②在水中的电离方程式为_________ 。
(3)写出①与⑥溶液反应的离子方程式:______ 。
Ⅱ、过氧化钠常用作漂白剂、杀菌剂、消毒剂,能与水和二氧化碳等物质发生反应,保存不当时容易变质。某实验小组以过氧化钠为研究对象进行了如下实验,请回答以下问题:
(4)纯净的Na2O2是________ 色固体,其中氧元素的化合价为_________ 价。
该实验小组为了粗略测定过氧化钠的质量分数,称取了20.0 g样品,并设计用如图装置通过排水法测定E中收集到的O2的体积,来测定过氧化钠的质量分数。
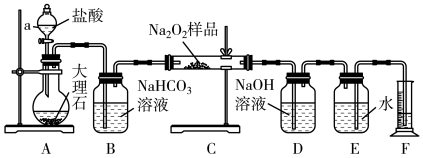
(5)将仪器连接好以后、加药品之前必须进行的一步操作_____ ,A中主要反应的离子方程式:_____ ;
(6)装置B的作用是除去二氧化碳气体中的______ 气体,写出相应的化学方程式_____ 。读出量筒内水的体积后,将其折算成标准状况下氧气的体积为2.24L,则样品中过氧化钠的质量分数为_____ 。
(1)属于酸性氧化物的是
(2)②在水中的电离方程式为
(3)写出①与⑥溶液反应的离子方程式:
Ⅱ、过氧化钠常用作漂白剂、杀菌剂、消毒剂,能与水和二氧化碳等物质发生反应,保存不当时容易变质。某实验小组以过氧化钠为研究对象进行了如下实验,请回答以下问题:
(4)纯净的Na2O2是
该实验小组为了粗略测定过氧化钠的质量分数,称取了20.0 g样品,并设计用如图装置通过排水法测定E中收集到的O2的体积,来测定过氧化钠的质量分数。

(5)将仪器连接好以后、加药品之前必须进行的一步操作
(6)装置B的作用是除去二氧化碳气体中的
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐3】按要求回答下列问题。
(1)现有以下物质:a.NaOH溶液b.液氨c.Ba(OH)2固体d.NaHSO4e.Fe(OH)3胶体f.铜g.CO2h.盐酸
①以上物质中属于非电解质的是_______ (填序号,下同),属于电解质的有_______ 。
②在足量d溶液中加入少量c溶液,发生反应的离子方程式为_______ 。
(2)银首饰在空气中容易发黄变黑,原因是发生反应:4Ag+O2+2H2S=2Ag2S+2H2O,当消耗了108gAg时,该反应消耗标准状况下的O2的体积为_______ 。
(3)“84消毒液”是家居常用的消毒用品,某小组同学查看包装说明,得到如图信息:

现取适量该“84清毒液”原液进行稀释,配制980mLc(NaClO)=0.05mol/L的溶液。
①稀释过程中,需要用到的玻璃仪器有烧杯,玻璃棒、量筒、胶头滴管、_______ 。
②稀释时,需要用量筒量取该“84消毒液”的体积为_______ mL。
③下列操作会使配制溶液中NaClO浓度偏高的是_______ (填标号)。
A.取用久置的“84消毒液”原液进行稀释
B.量取“84消毒液”原液时,仰视读数
C.容量瓶未干燥直接使用
D.定容时,仰视刻度线
E.定容摇匀后,液面低于刻度线,再加水至刻度线
(1)现有以下物质:a.NaOH溶液b.液氨c.Ba(OH)2固体d.NaHSO4e.Fe(OH)3胶体f.铜g.CO2h.盐酸
①以上物质中属于非电解质的是
②在足量d溶液中加入少量c溶液,发生反应的离子方程式为
(2)银首饰在空气中容易发黄变黑,原因是发生反应:4Ag+O2+2H2S=2Ag2S+2H2O,当消耗了108gAg时,该反应消耗标准状况下的O2的体积为
(3)“84消毒液”是家居常用的消毒用品,某小组同学查看包装说明,得到如图信息:

现取适量该“84清毒液”原液进行稀释,配制980mLc(NaClO)=0.05mol/L的溶液。
①稀释过程中,需要用到的玻璃仪器有烧杯,玻璃棒、量筒、胶头滴管、
②稀释时,需要用量筒量取该“84消毒液”的体积为
③下列操作会使配制溶液中NaClO浓度偏高的是
A.取用久置的“84消毒液”原液进行稀释
B.量取“84消毒液”原液时,仰视读数
C.容量瓶未干燥直接使用
D.定容时,仰视刻度线
E.定容摇匀后,液面低于刻度线,再加水至刻度线
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
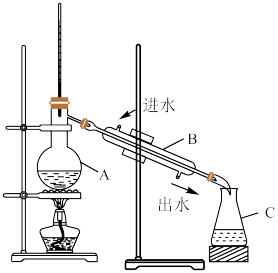
【推荐1】蒸馏是实验室制备蒸馏水的常用方法。
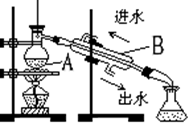
(1)如图是实验室制取蒸馏水的常用装置,图中明显的一个错误是__________________________ 。
(2)仪器A的名称是____________________ ,仪器B的名称是____________________________ 。
(3)实验时A中除加入少量自来水外,还需加入几粒______________ ,其作用是防止液体暴沸。
(4)从锥形瓶取少量收集到的液体于试管中,然后滴入___________________ 和 _______________ (填试剂的化学式),检验是否存在Cl-。
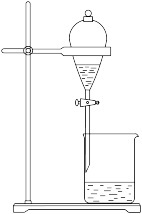
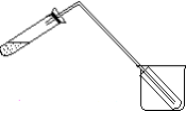
(5)如图装置也可用于少量蒸馏水的制取(加热及固定仪器略),其原理与上图完全相同。该装置中使用的玻璃导管较长,其作用是______________________________ ;为了提高冷凝效果,烧杯中最好盛有的物质是 ___________ (填名称)。

(1)如图是实验室制取蒸馏水的常用装置,图中明显的一个错误是
(2)仪器A的名称是
(3)实验时A中除加入少量自来水外,还需加入几粒
(4)从锥形瓶取少量收集到的液体于试管中,然后滴入
(5)如图装置也可用于少量蒸馏水的制取(加热及固定仪器略),其原理与上图完全相同。该装置中使用的玻璃导管较长,其作用是

您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐2】氢溴酸是无色、易挥发的液体,在化工领域用途广泛。实验室模拟一种工业制备氢溴酸的主要流程如图:

完成下列填空:
(1)写出反应①的离子方程式___ 。该反应需要在冰水浴中进行,可能的原因是___ 。
(2)操作I用到的玻璃仪器有蒸馏烧瓶、___ 、接液管和锥形瓶。
(3)反应②中Na2SO3的目的是___ 。
(4)反应③中的Ba(OH)2溶液能否用BaCl2或者Ba(NO3)2溶液代替?说明理由___ 。
(5)工业氢溴酸往往呈淡黄色。
①工业氢溴酸呈黄色可能是因为像工业盐酸一样含Fe3+,如何证明含Fe3+?___ 。
②工业氢溴酸呈黄色还可能是因为含___ ,如何证明?___ 。

完成下列填空:
(1)写出反应①的离子方程式
(2)操作I用到的玻璃仪器有蒸馏烧瓶、
(3)反应②中Na2SO3的目的是
(4)反应③中的Ba(OH)2溶液能否用BaCl2或者Ba(NO3)2溶液代替?说明理由
(5)工业氢溴酸往往呈淡黄色。
①工业氢溴酸呈黄色可能是因为像工业盐酸一样含Fe3+,如何证明含Fe3+?
②工业氢溴酸呈黄色还可能是因为含
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】Ⅰ、实验室有如下仪器:①试管 ②烧杯 ③量筒 ④蒸发皿 ⑤锥形瓶 ⑥温度计 ⑦蒸馏烧瓶
⑧分液漏斗。
回答下列问题:
(1)可以直接加热的有____________ (填序号,下同);
(2)加热时必须垫上石棉网的有______________ ;
(3)使用前必须查漏的有______________ ;
Ⅱ、选取下列实验方法分离物质,将分离方法的序号填在横线上。
A.萃取分液法 B.结晶法
C.分液法 D.蒸馏法
E.过滤法 F.升华法
(1)________ 分离饱和食盐水与沙子的混合物。
(2)________ 分离水和汽油的混合物。
(3)________ 分离四氯化碳(沸点为76.75 ℃)和甲苯(沸点为110.6 ℃)的混合物。
(4)________ 分离NaCl和I2的固体混合物。
⑧分液漏斗。
回答下列问题:
(1)可以直接加热的有
(2)加热时必须垫上石棉网的有
(3)使用前必须查漏的有
Ⅱ、选取下列实验方法分离物质,将分离方法的序号填在横线上。
A.萃取分液法 B.结晶法
C.分液法 D.蒸馏法
E.过滤法 F.升华法
(1)
(2)
(3)
(4)
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐2】(1)某同学采用萃取—分液的方法从碘水中提取碘,主要操作步骤如下图:
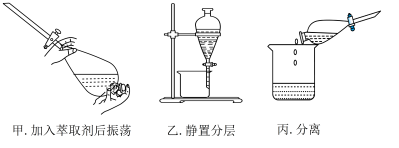
①该同学所采用的萃取剂可能是______________ (填序号)。
A 酒精 B 苯 C 四氯化碳 D 汽油
②甲、乙、丙3步实验操作中,不正确的是_______________ (填“甲”、“乙”或“丙”)。
(2)实验室制取、净化并收集氯气涉及以下几个主要阶段:
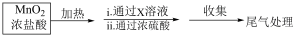
现有以下2种试剂:A 饱和食盐水 B NaOH溶液
请在以上实际中选择填空(填“A”或“B”):
①X溶液应选用________________ 。
②尾气处理过程中,多余的氯气可用________________ 吸收。

①该同学所采用的萃取剂可能是
A 酒精 B 苯 C 四氯化碳 D 汽油
②甲、乙、丙3步实验操作中,不正确的是
(2)实验室制取、净化并收集氯气涉及以下几个主要阶段:
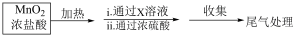
现有以下2种试剂:A 饱和食盐水 B NaOH溶液
请在以上实际中选择填空(填“A”或“B”):
①X溶液应选用
②尾气处理过程中,多余的氯气可用
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐1】在医药工业中,2-氯乙醇(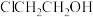 )可用于生产磷酸哌嗪、呋喃唑酮、四咪唑、驱蛔灵和普鲁卡因等。制备2-氯乙醇的装置如图所示。
)可用于生产磷酸哌嗪、呋喃唑酮、四咪唑、驱蛔灵和普鲁卡因等。制备2-氯乙醇的装置如图所示。
已知: ,
,
在制备乙烯过程中会产生 和
和 气体。
气体。
(1)仪器 的名称是
的名称是___________ ,装置A中碎瓷片的作用是___________ 。
(2)装置 中
中 溶液的作用是
溶液的作用是___________ 。
(3)装置D中发生反应的化学方程式为___________ 。
(4)装置C中发生反应的化学方程式为___________ 。
(5)如图装置中的导管 与装置
与装置 中的导管
中的导管 相连用来处理尾气,则装置
相连用来处理尾气,则装置 用来处理尾气
用来处理尾气___________ (填化学式),装置 中的现象是
中的现象是___________ 。
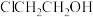 )可用于生产磷酸哌嗪、呋喃唑酮、四咪唑、驱蛔灵和普鲁卡因等。制备2-氯乙醇的装置如图所示。
)可用于生产磷酸哌嗪、呋喃唑酮、四咪唑、驱蛔灵和普鲁卡因等。制备2-氯乙醇的装置如图所示。已知:
 ,
,在制备乙烯过程中会产生
 和
和 气体。
气体。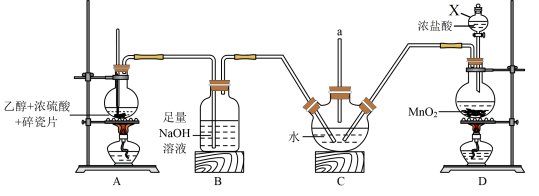
(1)仪器
 的名称是
的名称是(2)装置
 中
中 溶液的作用是
溶液的作用是(3)装置D中发生反应的化学方程式为
(4)装置C中发生反应的化学方程式为
(5)如图装置中的导管
 与装置
与装置 中的导管
中的导管 相连用来处理尾气,则装置
相连用来处理尾气,则装置 用来处理尾气
用来处理尾气 中的现象是
中的现象是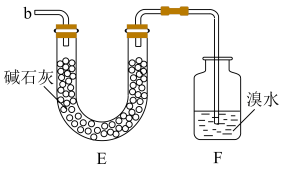
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐2】亚硝酸钠常用作防腐剂,某化学兴趣小组设计如图装置制备亚硝酸钠(部分夹持装置略,气密性已检验)。
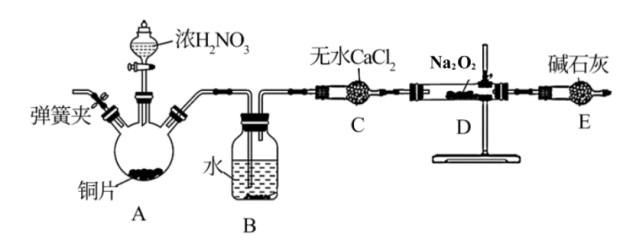
已知:ⅰ.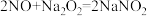 ,亚硝酸钠是白色固体,易潮解,易溶于水。
,亚硝酸钠是白色固体,易潮解,易溶于水。
ⅱ.
ⅲ.酸性条件下, 或
或 都能与
都能与 反应生成
反应生成 和
和 。
。
实验操作及现象:
回答下列问题:
(1)A装置中盛有铜片的仪器名称为_______ 。
(2)装置E中碱石灰的作用是_______ 。
(3)上述装置存在一处缺陷,不符合绿色化学的理念,改进的方法是_______ 。
(4)分析反应后D中白色固体的组成。
①从D中取白色固体,滴加酸性 溶液,现象为
溶液,现象为_______ ,证明固体中存在 。
。
②甲同学认为固体中可能存在硝酸钠,理由是装置中空气参与反应。请从实验现象中找出该同学判断的依据为_______ ,该同学设计方案解决该问题,进行的操作为:a.……;b.关闭弹簧夹,打开分液漏斗活塞,滴加适量浓硝酸;c.……。则操作a是_______ 。

已知:ⅰ.
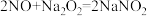 ,亚硝酸钠是白色固体,易潮解,易溶于水。
,亚硝酸钠是白色固体,易潮解,易溶于水。ⅱ.

ⅲ.酸性条件下,
 或
或 都能与
都能与 反应生成
反应生成 和
和 。
。实验操作及现象:
| 操作 | 现象 |
| ⅰ.关闭弹簧夹,打开分液漏斗活塞,滴加适量浓硝酸。 | A中铜片表面产生红棕色气泡,逐渐充满容器; B中刚开始时液面上方略显浅棕色并逐渐消失; D中淡黄色固体变为白色。 |
ⅱ.打开弹簧夹,通入 一段时间。 一段时间。 |
(1)A装置中盛有铜片的仪器名称为
(2)装置E中碱石灰的作用是
(3)上述装置存在一处缺陷,不符合绿色化学的理念,改进的方法是
(4)分析反应后D中白色固体的组成。
①从D中取白色固体,滴加酸性
 溶液,现象为
溶液,现象为 。
。②甲同学认为固体中可能存在硝酸钠,理由是装置中空气参与反应。请从实验现象中找出该同学判断的依据为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐3】实验室可用环己醇(沸点:160.84℃,微溶于水)制备环己酮(沸点:155.6℃,微溶于水),使用的氧化剂可以是次氯酸钠、重铬酸钾等。
下列装置分别是产品的合成装置和精制装置示意图:
向装有搅拌器、滴液漏斗和温度计的三颈烧瓶中依次加入5.2 mL环己醇和25 mL冰醋酸。开动搅拌器,将40 mL次氯酸钠溶液逐渐加入到反应瓶中,并使瓶内温度维持在30~35℃,用磁性搅拌器搅拌5 min。然后,在室温下继续搅拌30 min后,在合成装置中再加入30 mL水、3g氯化铝和几粒沸石,加热蒸馏至馏出液无油珠滴出为止。回答下列问题:
(1)在合成装置中,甲装置的名称是___________ 。
(2)三颈烧瓶的容量为___________ (填“50 mL”、“100 mL”或“250 mL”)。
(3)滴液漏斗具有特殊的结构,主要目的是___________ 。
(4)蒸馏完成后,向馏出液中分批加入无水碳酸钠至反应液呈中性为止,其目的是___________ 。然后加入精制食盐使之变成饱和溶液,再将混合液倒入___________ 中,分离得到有机层。
(5)有机层先加无水MgSO4,用如图装置对粗产品进行精制,加入无水MgSO4的作用是___________ ,对粗产品进行精制,蒸馏收集___________ ℃的馏分。检验精制后的环己酮是否纯净,可使用的试剂为___________ 。
A.重铬酸钾溶液 B.金属钠 C.酚酞溶液 D.新制的氢氧化铜悬浊液

下列装置分别是产品的合成装置和精制装置示意图:

向装有搅拌器、滴液漏斗和温度计的三颈烧瓶中依次加入5.2 mL环己醇和25 mL冰醋酸。开动搅拌器,将40 mL次氯酸钠溶液逐渐加入到反应瓶中,并使瓶内温度维持在30~35℃,用磁性搅拌器搅拌5 min。然后,在室温下继续搅拌30 min后,在合成装置中再加入30 mL水、3g氯化铝和几粒沸石,加热蒸馏至馏出液无油珠滴出为止。回答下列问题:
(1)在合成装置中,甲装置的名称是
(2)三颈烧瓶的容量为
(3)滴液漏斗具有特殊的结构,主要目的是
(4)蒸馏完成后,向馏出液中分批加入无水碳酸钠至反应液呈中性为止,其目的是
(5)有机层先加无水MgSO4,用如图装置对粗产品进行精制,加入无水MgSO4的作用是
A.重铬酸钾溶液 B.金属钠 C.酚酞溶液 D.新制的氢氧化铜悬浊液
您最近一年使用:0次