氧化还原反应在工农业生产、日常生活中具有广泛的用途。
(1)服用维生素C,可以使食物中的Fe3+转化为Fe2+,说明维生素C具有____ (填“氧化”或“还原”)性。
(2)我国古代四大发明之一的黑火药爆炸时的反应为:S+2KNO3+3C=K2S+N2↑+3CO2↑。在该反应中,氧化剂是____ (填化学式)。
(3)H2O2在实验、医疗、化工等方面有广泛的应用。酸性高锰酸钾溶液(用硫酸酸化)可与H2O2反应,其化学方程式是:H2O2+KMnO4+H2SO4——X+MnSO4+O2↑+H2O(未配平)。
已知:稀MnSO4溶液几乎无色。
①X的化学式是____ 。
②被氧化的元素是____ (填元素符号)。
③请配平上述反应,写出离子方程式并用单桥法标出上述反应中电子转移的方向和数目____ 。
④向酸性KMnO4溶液中滴入双氧水,观察到的现象是____ 。
(1)服用维生素C,可以使食物中的Fe3+转化为Fe2+,说明维生素C具有
(2)我国古代四大发明之一的黑火药爆炸时的反应为:S+2KNO3+3C=K2S+N2↑+3CO2↑。在该反应中,氧化剂是
(3)H2O2在实验、医疗、化工等方面有广泛的应用。酸性高锰酸钾溶液(用硫酸酸化)可与H2O2反应,其化学方程式是:H2O2+KMnO4+H2SO4——X+MnSO4+O2↑+H2O(未配平)。
已知:稀MnSO4溶液几乎无色。
①X的化学式是
②被氧化的元素是
③请配平上述反应,写出离子方程式并用单桥法标出上述反应中电子转移的方向和数目
④向酸性KMnO4溶液中滴入双氧水,观察到的现象是
更新时间:2022-10-12 13:45:49
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】某一反应体系中,有反应物和生成物共五种物质,这五种物质是:Cl2、KMnO4、MnCl2、H2O、HCl(浓)、KCl,其中Cl2、H2O均为生成物。
(1)该反应中的氧化剂是______________ ,氧化产物为_____________ 。
(2)该反应中,氧化产物与还原产物的物质的量之比为_______________ 。
(3)若产生的气体在标准状况下体积为2.24 L,则反应过程中转移电子的数目为______ NA(NA表示阿伏加德罗常数的值),发生反应的KMnO4的质量为___________ g。
(1)该反应中的氧化剂是
(2)该反应中,氧化产物与还原产物的物质的量之比为
(3)若产生的气体在标准状况下体积为2.24 L,则反应过程中转移电子的数目为
您最近一年使用:0次
【推荐2】现有下列反应:
①2H2O+Cl2+SO2=H2SO4+2HCl
②2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
针对上述两个反应回答:
(1)氧化剂的氧化性强弱顺序为____ ,还原剂的还原性强弱顺序为____ 。
(2)反应①中氧化剂是_____ 氧化产物是________ 。氧化产物和还原产物质量之比为____ 。
(3)反应②中氯化氢表现出的性质是____ 。
A.还原性 B.酸性
C.氧化性
(4)用单线桥法表示反应①的电子转移情况___
(5)用双线桥法表示反应②的电子转移情况___
①2H2O+Cl2+SO2=H2SO4+2HCl
②2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
针对上述两个反应回答:
(1)氧化剂的氧化性强弱顺序为
(2)反应①中氧化剂是
(3)反应②中氯化氢表现出的性质是
A.还原性 B.酸性
C.氧化性
(4)用单线桥法表示反应①的电子转移情况
(5)用双线桥法表示反应②的电子转移情况
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】氧化还原反应在日常生活、工农业生产和科学技术中应用广泛。
(1)氧化还原反应的实质是___________ 。
(2)废钒催化剂回收工艺中涉及的反应为 。
。
已知氯气与亚硫酸根离子会发生反应: ;根据上述两个反应,可推出
;根据上述两个反应,可推出 、
、 、
、 的还原性由强到弱的顺序为
的还原性由强到弱的顺序为___________ 。
(3)某实验兴趣小组根据氧化还原反应相关知识。探究 、
、 、
、 三者的氧化性强弱,设计实验装置如图:
三者的氧化性强弱,设计实验装置如图:

①实验Ⅰ的现象是___________ ;实验Ⅱ的现象是___________ 。
②实验Ⅱ发生反应的离子方程式为___________ 。
③综合实验Ⅰ和实验Ⅱ的现象及氧化还原反应的理论知识,可推测出 、
、 、
、 三者的氧化性由强到弱的顺序为
三者的氧化性由强到弱的顺序为___________ 。
④当两实验过程中发生的氧化还原反应转移的电子数相同时,铁丝与铜丝增重的质量之比为___________ 。(已知:实验起始时,铁丝与铜丝的质量相同且均足量)
(1)氧化还原反应的实质是
(2)废钒催化剂回收工艺中涉及的反应为
 。
。已知氯气与亚硫酸根离子会发生反应:
 ;根据上述两个反应,可推出
;根据上述两个反应,可推出 、
、 、
、 的还原性由强到弱的顺序为
的还原性由强到弱的顺序为(3)某实验兴趣小组根据氧化还原反应相关知识。探究
 、
、 、
、 三者的氧化性强弱,设计实验装置如图:
三者的氧化性强弱,设计实验装置如图:
①实验Ⅰ的现象是
②实验Ⅱ发生反应的离子方程式为
③综合实验Ⅰ和实验Ⅱ的现象及氧化还原反应的理论知识,可推测出
 、
、 、
、 三者的氧化性由强到弱的顺序为
三者的氧化性由强到弱的顺序为④当两实验过程中发生的氧化还原反应转移的电子数相同时,铁丝与铜丝增重的质量之比为
您最近一年使用:0次
【推荐2】回答下列问题:
(1)人体血红蛋白分子中含有Fe2+,正是这些Fe2+使血红蛋白分子具有载氧功能。亚硝酸钠(NaNO2)可将人体血红蛋白中的Fe2+转化为Fe3+,生成高铁血红蛋白而丧失与氧气的结合能力,反应过程中Fe2+发生___________ 反应,说明亚硝酸钠具有___________ 性;误食亚硝酸钠中毒,可服维生素C缓解,说明维生素C具有___________ 性。
(2)稀土氟化物是金属热还原法制取单一稀土金属的重要原料。微波法合成CeF3的化学方程式为6CeO2+18NH4F=CeF3+16NH3↑+12H2O+N2↑,该反应中还原剂是___________ ,反应中被氧化的氮原子与未被氧化的氮原子个数比为___________ 。
(3)过氧化氢溶液可作为采矿业废液消毒剂,如消除废液中剧毒的氰化钾(KCN,其中氮元素为-3价),反应方程式为KCN+H2O2+H2O=A+NH3↑(已配平)。
①该反应是否属于氧化还原反应?___________ (填“是”或“否”),理由是___________ 。若是,则被还原的元素是___________ 。
②生成物A的化学式是___________ 。
③该反应中发生氧化反应的物质是___________ ,理由是___________ 。
④若生成4个NH3分子,转移电子数为___________ 。
⑤用双线桥法表示反应中电子转移的方向和数目:___________ 。
(1)人体血红蛋白分子中含有Fe2+,正是这些Fe2+使血红蛋白分子具有载氧功能。亚硝酸钠(NaNO2)可将人体血红蛋白中的Fe2+转化为Fe3+,生成高铁血红蛋白而丧失与氧气的结合能力,反应过程中Fe2+发生
(2)稀土氟化物是金属热还原法制取单一稀土金属的重要原料。微波法合成CeF3的化学方程式为6CeO2+18NH4F=CeF3+16NH3↑+12H2O+N2↑,该反应中还原剂是
(3)过氧化氢溶液可作为采矿业废液消毒剂,如消除废液中剧毒的氰化钾(KCN,其中氮元素为-3价),反应方程式为KCN+H2O2+H2O=A+NH3↑(已配平)。
①该反应是否属于氧化还原反应?
②生成物A的化学式是
③该反应中发生氧化反应的物质是
④若生成4个NH3分子,转移电子数为
⑤用双线桥法表示反应中电子转移的方向和数目:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】央视《每周质量报告》曝光了河北省一些明胶企业将皮革废料熬制成工业明胶,出售给浙江绍兴某些制药企业,最终变成药用胶囊。由工业明胶制成的胶囊往往含有超标的重金属铬,会对人体造成伤害。
(1)已知Fe(CrO2)2中铁元素是+2价,则其中铬元素是_____ 价。
(2)①上述转化中,属于氧化还原反应的是_____ (填编号)。

②请配平下列离子方程式并标出电子转移方向和数目:_____ 。
1Cr2O +6I-+_____H+=2Cr3++3I2+7H2O。
+6I-+_____H+=2Cr3++3I2+7H2O。
每生成1摩尔氧化产物转移电子_____ 个。
(1)已知Fe(CrO2)2中铁元素是+2价,则其中铬元素是
(2)①上述转化中,属于氧化还原反应的是

②请配平下列离子方程式并标出电子转移方向和数目:
1Cr2O
 +6I-+_____H+=2Cr3++3I2+7H2O。
+6I-+_____H+=2Cr3++3I2+7H2O。每生成1摩尔氧化产物转移电子
您最近一年使用:0次
【推荐1】(1)请把符合要求的化学方程式的字母填在下列空白处:
①既属于分解反应又是氧化还原反应的是________ 。
②属于分解反应,但不是氧化还原反应的是________ 。
③既属于化合反应,又是氧化还原反应的是________ 。
④属于化合反应,但不是氧化还原反应的是________ 。
⑤不属于四种基本反应类型的氧化还原反应的是________ 。
A.(NH4)2SO3 2NH3↑+H2O+SO2↑
2NH3↑+H2O+SO2↑
B.2CO+O2 2CO2
2CO2
C.2C+SiO2 Si+2CO↑
Si+2CO↑
D.NH4NO3 N2O+ 2H2O
N2O+ 2H2O
E.CaCO3+ CO2+ H2O=Ca(HCO3)2
F.MnO2+ 4HCl(浓) MnCl2+ Cl2↑+ 2H2O
MnCl2+ Cl2↑+ 2H2O
(2)根据反应Al+4HNO3(稀)=Al(NO3)3+NO↑+2H2O,回答下列问题:
①还原剂是________ ,还原产物是________ 。
②被还原的硝酸与未被还原的硝酸的物质的量比是________ 。
③用单线桥表示此反应转移的电子数目及方向___________________________ 。
①既属于分解反应又是氧化还原反应的是
②属于分解反应,但不是氧化还原反应的是
③既属于化合反应,又是氧化还原反应的是
④属于化合反应,但不是氧化还原反应的是
⑤不属于四种基本反应类型的氧化还原反应的是
A.(NH4)2SO3
 2NH3↑+H2O+SO2↑
2NH3↑+H2O+SO2↑B.2CO+O2
 2CO2
2CO2C.2C+SiO2
 Si+2CO↑
Si+2CO↑D.NH4NO3
 N2O+ 2H2O
N2O+ 2H2OE.CaCO3+ CO2+ H2O=Ca(HCO3)2
F.MnO2+ 4HCl(浓)
 MnCl2+ Cl2↑+ 2H2O
MnCl2+ Cl2↑+ 2H2O(2)根据反应Al+4HNO3(稀)=Al(NO3)3+NO↑+2H2O,回答下列问题:
①还原剂是
②被还原的硝酸与未被还原的硝酸的物质的量比是
③用单线桥表示此反应转移的电子数目及方向
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】(1)配平下列方程式
①_____ Na+_____ H2O =_____ NaOH+_____ H2↑
②_____ Na2O2 +_____ CO2=_____ NaCO3 +_____ O2↑
③_____ KMnO4 +_____ HCl(浓) =_____ KCl +_____ MnCl2 +_____ H2O + _____ Cl2↑
④_____ Al+_____ H2O +_____ NaOH =_____ Na AlO2 +_____ H2↑
(2)用双线桥法表示电子转移的数目和方向____________ 、__________
①2Na2O2 + 2H2O = 4NaOH + O2↑
②2FeCl2 + Cl2 = 2FeCl3
①
②
③
④
(2)用双线桥法表示电子转移的数目和方向
①2Na2O2 + 2H2O = 4NaOH + O2↑
②2FeCl2 + Cl2 = 2FeCl3
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】(1)已知下列反应:Fe + S == FeS 2Fe + 3Cl2 ==2FeCl3 3Fe + 2O2 ==Fe3O4 则 S,Cl2,O2 的氧化性:______ >_____ >______
(2)用双线桥标出下列反应中电子转移的方向和数目:______
MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
该反应中的氧化剂是________ ,HCl体现的性质是_______________ ,若有4molHCl参加反应,则被氧化的HCl的物质的量是______ mol,如反应中转移了0.4mol电子,则产生的Cl2在标准状况下体积为_________ L。
(2)用双线桥标出下列反应中电子转移的方向和数目:
MnO2+4HCl(浓)
 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O该反应中的氧化剂是
您最近一年使用:0次
填空题
|
适中
(0.64)
【推荐1】(1)按要求写出下列反应的离子方程式
①少量二氧化碳通入澄清石灰水_______________
②硫酸氢钠与过量氢氧化钡溶液混合_____________
③熔融状态下NaHSO4电离方程式______________
(2)①用双线桥表示下列氧化还原反应电子转移
2KMnO4 + 16HCl(浓)=2KCl + 2MnCl2 + 5Cl2↑+ 8H2O
________________________
②配平下列氧化还原反应方程式:
___ KMnO4+___ H2O2+__ H2SO4 —__ K2SO4+__ MnSO4+__ O2↑+__ H2O
①少量二氧化碳通入澄清石灰水
②硫酸氢钠与过量氢氧化钡溶液混合
③熔融状态下NaHSO4电离方程式
(2)①用双线桥表示下列氧化还原反应电子转移
2KMnO4 + 16HCl(浓)=2KCl + 2MnCl2 + 5Cl2↑+ 8H2O
②配平下列氧化还原反应方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】氮元素的常见化合价及其化合价对应的常见物质的化学式如下表,试回答下列问题:
(1)从化合价上看,N2O5具有_______ (填“氧化”或“还原”)性。
(2)下列试剂不能用于干燥NH3的是_______(填标号)。
(3)NO与NO2中氮元素的价态均处于中间价态,则NO与NO2均既有氧化性又有还原性。
①NO极易与氧气反应,NO表现_______ 性;在一定条件下NO与氨气发生归中反应生成N2,其化学方程式为_______ 。
②NO2可与H2O发生自身歧化反应,反应中氧化剂和还原剂的物质的量之比为_______ ;NO2与NaOH溶液反应可生成两种盐,其中一种是NaNO2,写出NO2与NaOH溶液反应的化学方程式:_______ 。
③汽车排气管上装有催化转化器,可减少尾气对环境的污染,将汽车尾气中的有害气体CO和NO转化为无害气体排放,写出相关反应的化学方程式:_______ 。
④工业生产中利用氨水吸收SO2和NO2,原理如图所示:
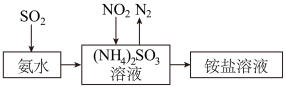
写出NO2被吸收过程中的离子方程式:_______ 。
| 化合价 | -3 | +1 | +2 | +3 | +4 | +5 |
| 化学式 | NH3 | N2O | NO | N2O3 | NO2 | N2O5 |
(1)从化合价上看,N2O5具有
(2)下列试剂不能用于干燥NH3的是_______(填标号)。
| A.浓硫酸 | B.碱石灰 | C.NaOH固体 | D.CaCl2固体 |
①NO极易与氧气反应,NO表现
②NO2可与H2O发生自身歧化反应,反应中氧化剂和还原剂的物质的量之比为
③汽车排气管上装有催化转化器,可减少尾气对环境的污染,将汽车尾气中的有害气体CO和NO转化为无害气体排放,写出相关反应的化学方程式:
④工业生产中利用氨水吸收SO2和NO2,原理如图所示:

写出NO2被吸收过程中的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】NaNO2是一种白色易溶于水的固体,溶液呈碱性,其外观与氯化钠相似,有咸味,俗称工业盐;是一 种重要的化学试剂、漂白剂和食品添加剂。已知亚硝酸盐能被溴水氧化,在酸性条件下能氧化亚铁离子; 亚硝酸银是可溶于稀硝酸的白色沉淀。
请完成以下填空:
(1)N原子最外层电子的轨道排布式为_______ ;用一个事实说明氮和氧非金属强弱_______ 。
(2)酸性条件下,NaNO2溶液只能将I-氧化为I2,同时生成NO。写出此反应①的离子方程式并标出电子转移的方向和数目______ 。
(3)氯气、浓硝酸、酸性高锰酸钾等都是常用的强氧化剂,工业上氧化卤水中的I-提取单质I2选择了价格并不便宜的亚硝酸钠,可能的原因是_______ 。
(4)在盐酸溶液中加入亚硝酸钠溶液至中性,则c(Cl-)_____ c(HNO2)(填“<”、“>”或“=”)。
(5)设计一种鉴别亚硝酸钠和氯化钠的实验方案。_______
请完成以下填空:
(1)N原子最外层电子的轨道排布式为
(2)酸性条件下,NaNO2溶液只能将I-氧化为I2,同时生成NO。写出此反应①的离子方程式并标出电子转移的方向和数目
(3)氯气、浓硝酸、酸性高锰酸钾等都是常用的强氧化剂,工业上氧化卤水中的I-提取单质I2选择了价格并不便宜的亚硝酸钠,可能的原因是
(4)在盐酸溶液中加入亚硝酸钠溶液至中性,则c(Cl-)
(5)设计一种鉴别亚硝酸钠和氯化钠的实验方案。
您最近一年使用:0次

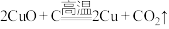 ②
② 完成以下问题:
完成以下问题: 失氧发生
失氧发生

