按要求书写化学方程式
(1)过氧化钠作为潜艇供氧剂的原理:_______
(2)钠在空气中加热:_______
(3)漂白粉生效原理:_______
(4)制备84消毒液:_______
(5)把钠放入硫酸铜溶液中:_______
(1)过氧化钠作为潜艇供氧剂的原理:
(2)钠在空气中加热:
(3)漂白粉生效原理:
(4)制备84消毒液:
(5)把钠放入硫酸铜溶液中:
更新时间:2022/10/24 08:01:54
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】有X、Y、Z三种元素
(1)X、Y、Z的三种单质在常温下均为气体
(2)X单质可在Z单质中燃烧,生成物XZ,其火焰为苍白色;
(3)XZ极易溶于水,电离出X+和Z-离子,水溶液可使湿润的蓝色石蕊试纸变红;
(4)2moLX可与1molY化合生成2molX2Y,X2Y常温下为液态
(5)Z单质黄绿色,溶于X2Y中,溶液有漂白作用,
则三种元素符号依次是X_____________ Y__________ Z__________ ,
它们化合物的化学式XZ__________ X2Y______________ 。
(1)X、Y、Z的三种单质在常温下均为气体
(2)X单质可在Z单质中燃烧,生成物XZ,其火焰为苍白色;
(3)XZ极易溶于水,电离出X+和Z-离子,水溶液可使湿润的蓝色石蕊试纸变红;
(4)2moLX可与1molY化合生成2molX2Y,X2Y常温下为液态
(5)Z单质黄绿色,溶于X2Y中,溶液有漂白作用,
则三种元素符号依次是X
它们化合物的化学式XZ
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】生产生活中常涉及到含氯的物质。下图(1)、(2)是验证次氯酸光照分解的数字化实验中pH和氯离子浓度变化与时间的关系。
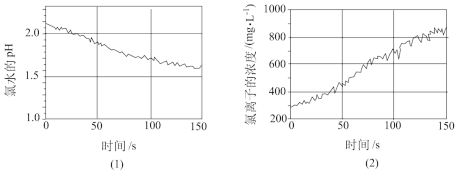
(1)从上图中相关曲线变化可知在光照过程中溶液的导电能力_______ (填“增强”、“不变”或“减弱”),主要原因是_______ (用化学 反应方程式表示)。
(2)检验一瓶氯水是否已经完全变质可选用的试剂是 (填字母)。
(3)有一种“地康法”制取氯气的反应原理如下图(3)所示:
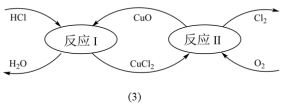
(提示:箭头进去的为反应物,出来的为生成物)
①写出实验室用MnO2与浓盐酸反应制取氯气的离子方程式为_______ 。
②整个过程的总反应化学方程式为_______ 。

(1)从上图中相关曲线变化可知在光照过程中溶液的导电能力
(2)检验一瓶氯水是否已经完全变质可选用的试剂是 (填字母)。
| A.硝酸银溶液 | B.酚酞溶液 | C.碳酸钠溶液 | D.紫色石蕊溶液 |

(提示:箭头进去的为反应物,出来的为生成物)
①写出实验室用MnO2与浓盐酸反应制取氯气的离子方程式为
②整个过程的总反应化学方程式为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】化学工业为疫情防控提供了强有力的物质支撑。氯的许多化合物既是重要化工原料,又是高效、广谱的灭菌消毒剂。回答下列问题:
(1)氯气是一种___________ 色的气体;氯气与水反应的化学方程式为___________ ;氯水中滴加少量紫色石蕊试液的现象是___________ 。
(2)氯气和石灰乳反应可以制备漂白粉,漂白粉的有效成分是___________ ;次氯酸盐与空气中的二氧化碳和水蒸气反应可生成次氯酸,从而发挥漂白和消毒作用,用化学方程式表示漂白粉的漂白和消毒原理___________ 。
(3)二氧化氯(ClO2)是目前国际上公认的新一代的高效、广谱、安全的杀菌、保鲜剂。一种制备ClO2的方法是用SO2通入硫酸酸化的NaClO3溶液中,反应的离子方程式为___________ ;ClO2在杀菌消毒过程中会产生副产物亚氯酸盐(ClO ),需将其转化为Cl-除去。下列试剂中,可将ClO
),需将其转化为Cl-除去。下列试剂中,可将ClO 转化为Cl-的是
转化为Cl-的是___________ (填字母序号)。
a.FeSO4 b.O3 c.KMnO4 d.SO2
(4)84消毒液与氯气相比具有贮运方便等优点,用氯气与烧碱溶液反应制备84消毒液的离子方程式为___________ ;工业上是将氯气通入到30%的NaOH溶液中来制备NaClO溶液,若NaClO溶液中NaOH的质量分数为1%,则生产100kg该溶液需消耗氯气的质量为___________ kg(保留整数)。
(1)氯气是一种
(2)氯气和石灰乳反应可以制备漂白粉,漂白粉的有效成分是
(3)二氧化氯(ClO2)是目前国际上公认的新一代的高效、广谱、安全的杀菌、保鲜剂。一种制备ClO2的方法是用SO2通入硫酸酸化的NaClO3溶液中,反应的离子方程式为
 ),需将其转化为Cl-除去。下列试剂中,可将ClO
),需将其转化为Cl-除去。下列试剂中,可将ClO 转化为Cl-的是
转化为Cl-的是a.FeSO4 b.O3 c.KMnO4 d.SO2
(4)84消毒液与氯气相比具有贮运方便等优点,用氯气与烧碱溶液反应制备84消毒液的离子方程式为
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐1】(1)氯气是最早用于饮用水消毒的物质,其消毒作用主要是氯气溶于水后生成了次氯酸,该反应的化学方程式为___________________________________________
(2)写出次氯酸光照后化学反应方程式:_____________________________________
(3)写出氯气工业制法方程式:_______________________________________
(2)写出次氯酸光照后化学反应方程式:
(3)写出氯气工业制法方程式:
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】利用氯元素的价类二维图可以从不同角度研究含氯物质的性质及其转化关系。图中①~⑩均含氯元素。回答下列问题:

(1)④的化学式为___________ ,⑦的电离方程式为___________ 。
(2)工业制漂白粉是将①通入___________ 中制成的,反应的离子方程式为___________ 。
(3)工业上常用 制备
制备 ,该反应的化学方程式为
,该反应的化学方程式为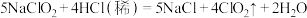 ,
,___________ (用双线桥标明电子转移方向和数目),氧化产物与还原产物物质的量之比为___________ 。
(4)比较⑥和⑦溶液的酸性强弱___________ (填可以或不可以)用pH试纸分别测定。
(5)含⑨的溶液可作为水处理剂除去水中的杂质离子。例如它可使酸性废水中的 转化为
转化为 ,整个过程对环境无污染,反应的离子方程式为
,整个过程对环境无污染,反应的离子方程式为___________ 。

(1)④的化学式为
(2)工业制漂白粉是将①通入
(3)工业上常用
 制备
制备 ,该反应的化学方程式为
,该反应的化学方程式为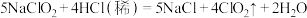 ,
,(4)比较⑥和⑦溶液的酸性强弱
(5)含⑨的溶液可作为水处理剂除去水中的杂质离子。例如它可使酸性废水中的
 转化为
转化为 ,整个过程对环境无污染,反应的离子方程式为
,整个过程对环境无污染,反应的离子方程式为
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】2010年4月14日7时49分在青海省玉树地区发生7.1级地震,造成了重大的人员伤亡和财产损失。为了保证震区的卫生环境,常使用漂白液和漂白粉对环境和饮用水进行杀菌、消毒,以抑制大规模传染病爆发。
回答下列问题:
(1)漂白液的有效成分是(填化学式)____________________ ;
(2)某研究性学习小组对漂白液进行了如下实验探究:取漂白液少量,滴入3~5滴紫色石蕊试液,发现溶液先变蓝色后褪色,可以证明漂白液具有的性质____________ (填序号)。
(3)工业上用氯气通入石灰乳[Ca(OH)2]制取漂白粉的化学方程式:
_____________________________________________________________________________ 。
(4)已知二氧化硫和亚硫酸盐具有较强的还原性。若将少量的SO2通入漂白粉溶液中,有同学认为发生的反应为:Ca(ClO)2+SO2+H2O=CaSO3↓+2HClO。你认为该同学的说法是否正确?
(填“正确”或“不正确”),请说明理由______________________________________________ 。
(5)二氧化氯是世卫组织确认的A级新型高效安全的消毒剂,其安全性远高于氯气。制备方法之一是:2NaClO3+4HCl =2ClO2↑+ Cl2↑+ 2NaCl + 2H2O,当转移0.2mol电子时,参加反应的还原剂的物质的量为___________ 。
回答下列问题:
(1)漂白液的有效成分是(填化学式)
(2)某研究性学习小组对漂白液进行了如下实验探究:取漂白液少量,滴入3~5滴紫色石蕊试液,发现溶液先变蓝色后褪色,可以证明漂白液具有的性质
| A.酸性 | B.碱性 | C.强氧化性 | D.还原性 |
(3)工业上用氯气通入石灰乳[Ca(OH)2]制取漂白粉的化学方程式:
(4)已知二氧化硫和亚硫酸盐具有较强的还原性。若将少量的SO2通入漂白粉溶液中,有同学认为发生的反应为:Ca(ClO)2+SO2+H2O=CaSO3↓+2HClO。你认为该同学的说法是否正确?
(填“正确”或“不正确”),请说明理由
(5)二氧化氯是世卫组织确认的A级新型高效安全的消毒剂,其安全性远高于氯气。制备方法之一是:2NaClO3+4HCl =2ClO2↑+ Cl2↑+ 2NaCl + 2H2O,当转移0.2mol电子时,参加反应的还原剂的物质的量为
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐1】填空:
(1)将一小块钠投入到硫酸铜溶液中,观察到与钠跟水反应相同的 现象是___________ ;还可以观察到的现象是___________ 。写出有关的化学方程式:___________ 、___________ 。
(2)灼烧后的铜丝立即插入充满氯气的集气瓶中观察到的现象是___________ ,集气瓶中注入少量水看到的现象是___________ 。
(3)将点燃的氢气伸入盛有氯气的集气瓶中观察到的现象是___________ 。
(1)将一小块钠投入到硫酸铜溶液中,观察到与钠跟水反应
(2)灼烧后的铜丝立即插入充满氯气的集气瓶中观察到的现象是
(3)将点燃的氢气伸入盛有氯气的集气瓶中观察到的现象是
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】写出下列反应的离子方程式
(1)胃舒平[Al(OH)3]治疗胃酸过多的原理_______
(2)已知氮化镁与水反应生成氢氧化镁和氨气,则氮化镁和盐酸反应的离子方程式为_______
(3)完成并配平: +
+ +_____=Mn2++CO2↑+______,
+_____=Mn2++CO2↑+______,_______ 。
(4)明矾净水原理_______
(5)钠与氯化铁溶液反应_______ (用总反应式表示)
(1)胃舒平[Al(OH)3]治疗胃酸过多的原理
(2)已知氮化镁与水反应生成氢氧化镁和氨气,则氮化镁和盐酸反应的离子方程式为
(3)完成并配平:
 +
+ +_____=Mn2++CO2↑+______,
+_____=Mn2++CO2↑+______,(4)明矾净水原理
(5)钠与氯化铁溶液反应
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】Ⅰ.今有11种物质:①铝线;②石墨;③氯气;④BaSO4晶体;⑤纯硫酸;⑥盐酸;⑦石灰水;⑧乙醇;⑨熔融的KNO3;⑩NH3。其中:属于电解质的是___ ;
Ⅱ.已知0.1 mol/L的NaHSO4溶液中H+的物质的量浓度为0.1 mol/L,请回答下列问题:
(1)写出NaHSO4在水溶液中电离的方程式:____ 。
(2)写出NaHSO4与氢氧化钠溶液反应的离子方程式___ 。
(3)向NaHSO4溶液中逐滴加入Ba(OH)2溶液至溶液恰好显中性,则该反应的离子方程式是:____ 。
Ⅲ.钠是一种还原性很强的金属,甚至能和冷水发生剧烈反应,写出钠加入到水中反生反应的离子反应方程式___ ;把钠加入到饱和的石灰水中的现象是___ ,产生这种现象的原因是_____ ;把钠加入到硫酸铜溶液中的现象是___ ,写出该过程中产生沉淀的离子反应方程式____ ;写出少量的钠加入到足量硫酸氢钠溶液中反应的离子方程式____ 。
Ⅳ.将一定体积的CuSO4溶液、NaCl溶液和Na2SO3混合,充分反应后有白色沉淀生成。经分析可知白色沉淀中只含有铜元素和氯元素,且该化合物的摩尔质量为99.5g/mol。试回答下列问题:
(1)白色沉淀的化学式为____ 。
(2)题述过程发生的反应____ (填“属于”或“不属于”)氧化还原反应。
(3)题述反应的离子方程式为Cu2++Cl-+SO32-+H2O→白色沉淀+( )+H+(离子方程式没有配平),则括号内的离子为___ 。
Ⅱ.已知0.1 mol/L的NaHSO4溶液中H+的物质的量浓度为0.1 mol/L,请回答下列问题:
(1)写出NaHSO4在水溶液中电离的方程式:
(2)写出NaHSO4与氢氧化钠溶液反应的离子方程式
(3)向NaHSO4溶液中逐滴加入Ba(OH)2溶液至溶液恰好显中性,则该反应的离子方程式是:
Ⅲ.钠是一种还原性很强的金属,甚至能和冷水发生剧烈反应,写出钠加入到水中反生反应的离子反应方程式
Ⅳ.将一定体积的CuSO4溶液、NaCl溶液和Na2SO3混合,充分反应后有白色沉淀生成。经分析可知白色沉淀中只含有铜元素和氯元素,且该化合物的摩尔质量为99.5g/mol。试回答下列问题:
(1)白色沉淀的化学式为
(2)题述过程发生的反应
(3)题述反应的离子方程式为Cu2++Cl-+SO32-+H2O→白色沉淀+( )+H+(离子方程式没有配平),则括号内的离子为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】在呼吸面具和潜水艇中可用过氧化钠作为供氧剂。请选用适当的化学试剂和实验用品、用图中的实验装置进行实验,证明过氧化钠可作供氧剂。
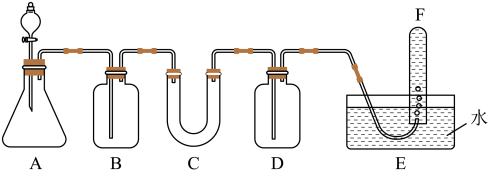
(1)填写表中空格:
(2)试管F中收集满气体后,下一步实验操作的目的 是:___ 。

(1)填写表中空格:
| 仪器 | 加入试剂 | 加入该试剂的目的 |
| A | 石灰石和稀盐酸 | 制取CO2气体 |
| B | 饱和NaHCO3溶液 | |
| C | 过氧化钠 | 与CO2和水蒸气反应,产生O2 |
| D |
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】钠及其化合物是具有广泛应用的材料。
(1)金属钠很活泼,通常保存在_______ 里,以隔绝空气。
(2) 是
是_______ 色固体,飞船内安装盛有 的装置,它的用途是产生氧气。与人体呼出的
的装置,它的用途是产生氧气。与人体呼出的 反应的化学方程式
反应的化学方程式_______ 。
(3)汽车安全气囊的气体发生剂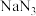 可由金属钠生产,某汽车安全气囊内含
可由金属钠生产,某汽车安全气囊内含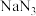 、
、 和
和 等物质。
等物质。
①当气体发生较严重的碰撞时,引发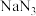 分解的反应为
分解的反应为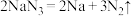 ,从而为气囊充气,用单线桥法标出该反应的电子转移方向和数目
,从而为气囊充气,用单线桥法标出该反应的电子转移方向和数目_______ 。
②产生的 立即与
立即与 发生置换反应生成
发生置换反应生成 ,化学方程式是
,化学方程式是_______ 。
③ 是冷却剂,能吸收上述过程释放的热量,并使自身分解。
是冷却剂,能吸收上述过程释放的热量,并使自身分解。 起冷却作用时,发生分解反应的化学方程式为
起冷却作用时,发生分解反应的化学方程式为_______ 。
④假设一个安全气囊装有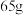
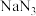 ,完全分解所释放的N2为
,完全分解所释放的N2为_______  。
。
(1)金属钠很活泼,通常保存在
(2)
 是
是 的装置,它的用途是产生氧气。与人体呼出的
的装置,它的用途是产生氧气。与人体呼出的 反应的化学方程式
反应的化学方程式(3)汽车安全气囊的气体发生剂
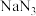 可由金属钠生产,某汽车安全气囊内含
可由金属钠生产,某汽车安全气囊内含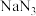 、
、 和
和 等物质。
等物质。①当气体发生较严重的碰撞时,引发
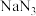 分解的反应为
分解的反应为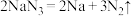 ,从而为气囊充气,用单线桥法标出该反应的电子转移方向和数目
,从而为气囊充气,用单线桥法标出该反应的电子转移方向和数目②产生的
 立即与
立即与 发生置换反应生成
发生置换反应生成 ,化学方程式是
,化学方程式是③
 是冷却剂,能吸收上述过程释放的热量,并使自身分解。
是冷却剂,能吸收上述过程释放的热量,并使自身分解。 起冷却作用时,发生分解反应的化学方程式为
起冷却作用时,发生分解反应的化学方程式为④假设一个安全气囊装有
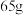
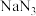 ,完全分解所释放的N2为
,完全分解所释放的N2为 。
。
您最近半年使用:0次



