已知NaNO2能发生如下反应(未配平):NaNO2+HI→NO+I2+NaI+H2O
(1)配平方程式,并用单线桥表示电子的转移方向和数目:_______ 。
NaNO2+_______HI—_______NO+_______I2+_______NaI+_______H2O
(2)反应中_______ 元素被氧化(填元素名称),_______ 是氧化剂(填化学式);
(3)氧化产物是_______ (填写化学式,下同),还原产物是_______ 。
(4)反应中,每生成1分子I2,转移的电子数为_______ ;消耗128g还原剂,生成还原产物的质量为_______ 。
(1)配平方程式,并用单线桥表示电子的转移方向和数目:
NaNO2+_______HI—_______NO+_______I2+_______NaI+_______H2O
(2)反应中
(3)氧化产物是
(4)反应中,每生成1分子I2,转移的电子数为
更新时间:2022-10-08 21:20:54
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】 为棕褐色固体,在化工生产中有许多应用。
为棕褐色固体,在化工生产中有许多应用。
(1) 元素有
元素有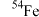 、
、 、
、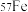 、
、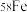 四种核素,它们互为
四种核素,它们互为___________ ,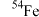 的中子数为
的中子数为___________ ,1个 原子的质量是
原子的质量是___________ 。
(2)书写利用单质反应制备氯化铁的化学方程式,并标出电子转移的方向和数目:___________ 。
(3)氯化铁溶于水后,电离方程式为___________ 。检验氧化铁溶液中的溶质负离子的操作、现象和结论是:___________ 。
(4)将少量饱和 溶液分别滴加到下列物质中,得到三种分散系甲、乙、丙。
溶液分别滴加到下列物质中,得到三种分散系甲、乙、丙。

用红色激光灯分别照射分散系甲和丙,现象的差异为:___________ 。向丙中加入少量稀盐酸,会出现和乙中相同的现象,原因是:___________ 。
(5)5.410g氧化铁晶体( )与100mL
)与100mL  溶液恰好完全沉淀,则
溶液恰好完全沉淀,则 溶液的物质的量浓度为
溶液的物质的量浓度为___________ 。
(6)若用氯化铁晶体( )配制100mL
)配制100mL 
 溶液,下列会造成所配溶液物质的量浓度偏高的是___________。
溶液,下列会造成所配溶液物质的量浓度偏高的是___________。
(7)将饱和氯化铁溶液与小苏打溶液混合时,会产生红褐色沉淀和一种无色无味且能使石灰水变浑浊的气体,则该气体在标况下的密度为___________ 。(保留三位小数)
 为棕褐色固体,在化工生产中有许多应用。
为棕褐色固体,在化工生产中有许多应用。(1)
 元素有
元素有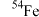 、
、 、
、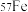 、
、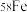 四种核素,它们互为
四种核素,它们互为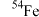 的中子数为
的中子数为 原子的质量是
原子的质量是(2)书写利用单质反应制备氯化铁的化学方程式,并标出电子转移的方向和数目:
(3)氯化铁溶于水后,电离方程式为
(4)将少量饱和
 溶液分别滴加到下列物质中,得到三种分散系甲、乙、丙。
溶液分别滴加到下列物质中,得到三种分散系甲、乙、丙。
用红色激光灯分别照射分散系甲和丙,现象的差异为:
(5)5.410g氧化铁晶体(
 )与100mL
)与100mL  溶液恰好完全沉淀,则
溶液恰好完全沉淀,则 溶液的物质的量浓度为
溶液的物质的量浓度为(6)若用氯化铁晶体(
 )配制100mL
)配制100mL 
 溶液,下列会造成所配溶液物质的量浓度偏高的是___________。
溶液,下列会造成所配溶液物质的量浓度偏高的是___________。| A.定容时,俯视凹液面最低点 |
| B.转移时,有少量液体溅出 |
C. 晶体已部分失水 晶体已部分失水 |
| D.烧杯、玻璃棒未洗涤 |
(7)将饱和氯化铁溶液与小苏打溶液混合时,会产生红褐色沉淀和一种无色无味且能使石灰水变浑浊的气体,则该气体在标况下的密度为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】常见消毒剂有:①医用酒精;②“84”消毒液(主要成分是NaClO);③漂白粉;④二氧化氯;⑤O3;⑥高铁酸钠。
(1)上述物质中,消毒原理和其他不同的是___________ (填序号,下同)。
(2)上述物质中,其有效成分属于电解质的是___________ 。
(3)臭氧和氧气互为___________ (填“同位素”或“同素异形体”),它们在一定条件下可以相互转化,该变化过程属于___________ 。(填“氧化还原反应”或“非氧化还原反应”)。
(4)“84”消毒液和洁厕剂(主要成分是稀盐酸)混合使用会发生中毒事件,原因是___________ (用离子方程式表示)。
(5)配平下列方程式并用双线桥在方程式中标出电子转移的情况:___________ 。
 KClO3+
KClO3+ HCl(浓)=
HCl(浓)= KCl+
KCl+ ClO2↑+Cl2↑+H2O
ClO2↑+Cl2↑+H2O
(6)高铁酸钠(Na2FeO4)还是一种新型的净水剂。从其组成的阳离子来看,高铁酸钠属于___________ 盐,其中Fe的化合价是___________ 。其净水过程中所发生的化学反应主要为:4Na2FeO4+10H2O=4Fe(OH)3(胶体)+3O2↑+8NaOH,证明有Fe(OH)3胶体生成的实验操作:___________ 。
(1)上述物质中,消毒原理和其他不同的是
(2)上述物质中,其有效成分属于电解质的是
(3)臭氧和氧气互为
(4)“84”消毒液和洁厕剂(主要成分是稀盐酸)混合使用会发生中毒事件,原因是
(5)配平下列方程式并用双线桥在方程式中标出电子转移的情况:
 KClO3+
KClO3+ HCl(浓)=
HCl(浓)= KCl+
KCl+ ClO2↑+Cl2↑+H2O
ClO2↑+Cl2↑+H2O(6)高铁酸钠(Na2FeO4)还是一种新型的净水剂。从其组成的阳离子来看,高铁酸钠属于
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】回答下列问题
(1)铝是地壳中含量最多的金属元素,画出铝原子结构示意图_______ 。在酒精灯的火焰上灼烧铝片,可观察到铝熔化但不滴落,说明铝的熔点比较_______ (高、低),外层氧化铝薄膜是_______ (疏松、致密)的。
(2)根据反应 ,回答下列问题:
,回答下列问题:
①画双线桥,请标出变价元素化合价、电子得失及转移数目_______ 。
②还原剂是_______ ,被_______ (氧化、还原)。
③当有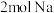 反应时,转移
反应时,转移_______  电子,生成
电子,生成
_______ L(标准状态下)。
(1)铝是地壳中含量最多的金属元素,画出铝原子结构示意图
(2)根据反应
 ,回答下列问题:
,回答下列问题:①画双线桥,请标出变价元素化合价、电子得失及转移数目
②还原剂是
③当有
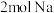 反应时,转移
反应时,转移 电子,生成
电子,生成
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】高铁酸钠(Na2FeO4)是水处理过程中使用的一种新型净水剂,它的氧化性比高锰酸钾、还强。工业上制取高铁酸钠的化学方程式是(未配平):Fe(NO3)3+NaOH+Cl2→Na2FeO4+NaNO3+NaCl+H2O。
(1)高铁酸钠中,铁元素的化合价是____ ;上述制取铁酸钠的反应过程中,铁元素被____ (填“还原”或“氧化”)。
(2)高铁酸钠(Na2FeO4)是水处理过程中常用的新型净水剂,原因是Na2FeO4被还原为Fe3+,形成Fe(OH)3胶体,使水中悬浮物沉聚,Fe(OH)3胶体微粒直径的范围是____ nm,高铁酸钠在水溶液中的电离方程式是____ 。
(3)某同学配制了一瓶K2FeO4溶液,但标签丢失了,测定该瓶溶液物质的量浓度的实验步骤如下:
步骤1:准确量取VmL溶液加入锥形瓶中;
步骤2:在强碱溶液中,用过量CrO 与FeO
与FeO  反应生成Fe(OH)3和CrO
反应生成Fe(OH)3和CrO  ;
;
步骤3:加足量稀硫酸,使CrO 转化为Cr2O
转化为Cr2O ,CrO
,CrO 转化为Cr3+,Fe(OH)3转化为Fe3+;
转化为Cr3+,Fe(OH)3转化为Fe3+;
步骤4:加入二苯胺磺酸钠作指示剂,用cmol·L-1(NH4)2Fe(SO4)2溶液滴加至终点,消耗(NH4)2Fe(SO4)2标准溶液V1mL,此时Cr2O 恰好完全转化为Cr3+。
恰好完全转化为Cr3+。
①写出步骤四发生反应的离子方程式为____ 。
②原溶液中K2FeO4的物质的量浓度为____ (用含字母的代数式表示)。
Ⅱ.次磷酸(H3PO2)是一种精细磷化工产品,是一元中强酸,具有较强还原性。
(4)H3PO2及NaH2PO2均可将溶液中的Ag+还原为银,从而可用于化学镀银。
①利用H3PO2进行化学镀银,氧化剂(Ag+)与还原剂(H3PO2)的物质的量之比为4:1,则氧化产物为____ (填化学式)。
②从分类来看,NaH2PO2属于____ 。
a.正盐 b.酸式盐 c.钠盐 d.氧化物
(5)H3PO2的工业制法如下方程式,请配平方程式____ 。
P4+ Ba(OH)2+ H2O→ Ba(H2PO2)2+ PH3↑
(1)高铁酸钠中,铁元素的化合价是
(2)高铁酸钠(Na2FeO4)是水处理过程中常用的新型净水剂,原因是Na2FeO4被还原为Fe3+,形成Fe(OH)3胶体,使水中悬浮物沉聚,Fe(OH)3胶体微粒直径的范围是
(3)某同学配制了一瓶K2FeO4溶液,但标签丢失了,测定该瓶溶液物质的量浓度的实验步骤如下:
步骤1:准确量取VmL溶液加入锥形瓶中;
步骤2:在强碱溶液中,用过量CrO
 与FeO
与FeO  反应生成Fe(OH)3和CrO
反应生成Fe(OH)3和CrO  ;
;步骤3:加足量稀硫酸,使CrO
 转化为Cr2O
转化为Cr2O ,CrO
,CrO 转化为Cr3+,Fe(OH)3转化为Fe3+;
转化为Cr3+,Fe(OH)3转化为Fe3+;步骤4:加入二苯胺磺酸钠作指示剂,用cmol·L-1(NH4)2Fe(SO4)2溶液滴加至终点,消耗(NH4)2Fe(SO4)2标准溶液V1mL,此时Cr2O
 恰好完全转化为Cr3+。
恰好完全转化为Cr3+。①写出步骤四发生反应的离子方程式为
②原溶液中K2FeO4的物质的量浓度为
Ⅱ.次磷酸(H3PO2)是一种精细磷化工产品,是一元中强酸,具有较强还原性。
(4)H3PO2及NaH2PO2均可将溶液中的Ag+还原为银,从而可用于化学镀银。
①利用H3PO2进行化学镀银,氧化剂(Ag+)与还原剂(H3PO2)的物质的量之比为4:1,则氧化产物为
②从分类来看,NaH2PO2属于
a.正盐 b.酸式盐 c.钠盐 d.氧化物
(5)H3PO2的工业制法如下方程式,请配平方程式
P4+ Ba(OH)2+ H2O→ Ba(H2PO2)2+ PH3↑
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】黄铁矿(主要成分为FeS2)的有效利用对环境具有重要意义。
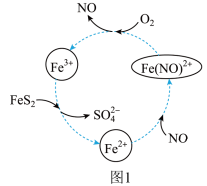
(1)在酸性条件下催化氧化黄铁矿的物质转化关系如图1所示。
①图1转化过程的总反应中,FeS2做__ (填“催化剂”“氧化剂”或“还原剂”,下同)。该转化过程中NO的作用是__ 。
②写出图1中Fe3+与FeS2反应的离子方程式:__ 。
(2)Fe2+被氧化为Fe3+的过程中,控制起始时Fe2+的浓度、溶液体积和通入O2的速率不变,改变其他条件时,Fe2+被氧化的转化率随时间的变化如图2所示。
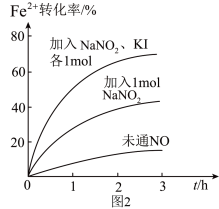
①加入NaNO2发生反应:2H++3NO =NO
=NO +2NO↑+H2O。该反应中若有6molNaNO2完全反应,转移电子的物质的量为
+2NO↑+H2O。该反应中若有6molNaNO2完全反应,转移电子的物质的量为__ mol。
②加入NaNO2、KI发生反应:4H++2NO +2I-=2NO↑+I2+2H2O。解释图2中该条件下能进一步提高单位时间内Fe2+转化率的原因:
+2I-=2NO↑+I2+2H2O。解释图2中该条件下能进一步提高单位时间内Fe2+转化率的原因:__ 。

(1)在酸性条件下催化氧化黄铁矿的物质转化关系如图1所示。
①图1转化过程的总反应中,FeS2做
②写出图1中Fe3+与FeS2反应的离子方程式:
(2)Fe2+被氧化为Fe3+的过程中,控制起始时Fe2+的浓度、溶液体积和通入O2的速率不变,改变其他条件时,Fe2+被氧化的转化率随时间的变化如图2所示。

①加入NaNO2发生反应:2H++3NO
 =NO
=NO +2NO↑+H2O。该反应中若有6molNaNO2完全反应,转移电子的物质的量为
+2NO↑+H2O。该反应中若有6molNaNO2完全反应,转移电子的物质的量为②加入NaNO2、KI发生反应:4H++2NO
 +2I-=2NO↑+I2+2H2O。解释图2中该条件下能进一步提高单位时间内Fe2+转化率的原因:
+2I-=2NO↑+I2+2H2O。解释图2中该条件下能进一步提高单位时间内Fe2+转化率的原因:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】利用物质类别及核心元素的化合价推测物质的性质是研究化学的重要手段。硫元素的常见化合价与部分物质类别的对应关系如图。回答下列问题:
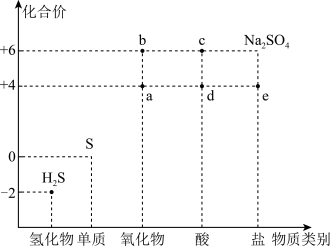
(1)将H2S与a混合,发生反应的氧化剂与还原剂的物质的量之比为_______ 。
(2)c的浓溶液能与H2S反应产生一种气体和淡黄色沉淀,写出此反应的化学方程式:_______ 。
(3)将a排入大气中会引起_______ 。
(4)硫元素还有一种常见的价态为-1价,如硫铁矿(主要成分为FeS2)中的硫元素。FeS2可以与Fe2(SO4)3溶液发生反应:7Fe2(SO4)3+FeS2+8H2O=15FeSO4+8H2SO4。该反应中的氧化剂是_______ (填化学式)。向反应后的溶液中通入空气能使Fe2(SO4)3溶液再生,写出再生反应的离子方程式:_______ 。
(5)常温下,c的浓溶液可用铁罐车或铝槽车运输,其原因是铁和铝在常温下遇到c的浓溶液会发生_______ 。
(6)若要验证木炭与c的浓溶液反应的产物中同时含有气体a和CO2,可选择以下试剂进行实验:
①NaOH溶液 ②品红溶液 ③溴水 ④Ca(OH)2溶液
选择合适试剂,并安排合理的顺序_______ (填序号)。

(1)将H2S与a混合,发生反应的氧化剂与还原剂的物质的量之比为
(2)c的浓溶液能与H2S反应产生一种气体和淡黄色沉淀,写出此反应的化学方程式:
(3)将a排入大气中会引起
(4)硫元素还有一种常见的价态为-1价,如硫铁矿(主要成分为FeS2)中的硫元素。FeS2可以与Fe2(SO4)3溶液发生反应:7Fe2(SO4)3+FeS2+8H2O=15FeSO4+8H2SO4。该反应中的氧化剂是
(5)常温下,c的浓溶液可用铁罐车或铝槽车运输,其原因是铁和铝在常温下遇到c的浓溶液会发生
(6)若要验证木炭与c的浓溶液反应的产物中同时含有气体a和CO2,可选择以下试剂进行实验:
①NaOH溶液 ②品红溶液 ③溴水 ④Ca(OH)2溶液
选择合适试剂,并安排合理的顺序
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】物质的类别和核心元素的化合价是研究物质化学性质的两个重要角度。硫元素的价类二维图如图所示(其中h、g的阳离子均为 ),请回答下列问题:
),请回答下列问题:

(1)e的化学式是___________ 。
(2)实验室常用g和f的浓溶液制备气体c,写出其化学方程式___________ 。
(3)将气体c通入a的水溶液,溶液变浑浊,用化学方程式解释___________ ,体现了c的___________ 性。
(4)过量的铜与f的浓溶液在加热条件下可以发生,化学方程式为___________ ,反应后铜片有剩余,为使剩余的铜片继续溶解,可在其中加入硝酸盐溶液(如 溶液),则该反应的离子方程式为
溶液),则该反应的离子方程式为___________ 。
 ),请回答下列问题:
),请回答下列问题:
(1)e的化学式是
(2)实验室常用g和f的浓溶液制备气体c,写出其化学方程式
(3)将气体c通入a的水溶液,溶液变浑浊,用化学方程式解释
(4)过量的铜与f的浓溶液在加热条件下可以发生,化学方程式为
 溶液),则该反应的离子方程式为
溶液),则该反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】“铜都”安徽铜陵有许多黄铜矿(主要成分为CuFeS2,含少量Al2O3、SiO2),黄铜矿是制取铜及其化合物的主要原料之一,还可制备硫及铁的化合物。
(1)火法炼铜首先要焙烧黄铜矿,其反应原理为2CuFeS2+O2 Cu2S+2FeS+SO2。CuFeS2中Cu和Fe元素的化合价均为+2价,被还原的元素是
Cu2S+2FeS+SO2。CuFeS2中Cu和Fe元素的化合价均为+2价,被还原的元素是_______ (填元素符号),若反应中转移0.3mol电子时,则标准状况下产生SO2的体积为_______ L。
(2)焙烧黄铜矿产生的Cu2S可被稀硝酸氧化为Cu2+ 和硫单质,HNO3的还原产物为NO,试写出Cu2S与稀硝酸反应的离子方程式_________________ ,该反应中稀硝酸体现____________ (填“氧化性”、“还原性”或“酸性”)。
(3)焙烧黄铜矿还可得到Cu2O。将21.6g Cu2O加入到500mL某浓度的稀硝酸中,固体物质完全反应,生成Cu(NO3)2和NO,在所得溶液中加入1.0mol∙L-1的NaOH溶液1.0L,此时溶液呈中性。原硝酸的物质的量浓度为__________ 。
(1)火法炼铜首先要焙烧黄铜矿,其反应原理为2CuFeS2+O2
 Cu2S+2FeS+SO2。CuFeS2中Cu和Fe元素的化合价均为+2价,被还原的元素是
Cu2S+2FeS+SO2。CuFeS2中Cu和Fe元素的化合价均为+2价,被还原的元素是(2)焙烧黄铜矿产生的Cu2S可被稀硝酸氧化为Cu2+ 和硫单质,HNO3的还原产物为NO,试写出Cu2S与稀硝酸反应的离子方程式
(3)焙烧黄铜矿还可得到Cu2O。将21.6g Cu2O加入到500mL某浓度的稀硝酸中,固体物质完全反应,生成Cu(NO3)2和NO,在所得溶液中加入1.0mol∙L-1的NaOH溶液1.0L,此时溶液呈中性。原硝酸的物质的量浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】Ⅰ.某实验小组为探究ClO-、I2、SO42-在酸性条件下的氧化性强弱,设计实验如下:
实验①:在淀粉-碘化钾溶液中加入少量次氯酸钠溶液,并加入少量的稀硫酸,溶液立即变蓝;
实验②:向实验①的溶液中加入4mL 0.5 mol·L-1的亚硫酸钠溶液,蓝色恰好完全褪去。
(1)写出实验①中发生反应的离子方程式:____ 。
(2)实验②的化学反应中转移电子的物质的量是____ 。
Ⅱ.(3)Cl2、H2O2、ClO2(还原产物为Cl-)、O3(1mol O3转化为1mol O2和1mol H2O)等物质常被用作消毒剂。等物质的量的上述物质消毒效率最高的是____ (填序号)。
A.Cl2 B.H2O2 C.ClO2 D.O3
(4)“84”消毒液(主要成分是NaClO)和洁厕剂(主要成分是浓盐酸)不能混用,原因是____ (用离子方程式表示)。
实验①:在淀粉-碘化钾溶液中加入少量次氯酸钠溶液,并加入少量的稀硫酸,溶液立即变蓝;
实验②:向实验①的溶液中加入4mL 0.5 mol·L-1的亚硫酸钠溶液,蓝色恰好完全褪去。
(1)写出实验①中发生反应的离子方程式:
(2)实验②的化学反应中转移电子的物质的量是
Ⅱ.(3)Cl2、H2O2、ClO2(还原产物为Cl-)、O3(1mol O3转化为1mol O2和1mol H2O)等物质常被用作消毒剂。等物质的量的上述物质消毒效率最高的是
A.Cl2 B.H2O2 C.ClO2 D.O3
(4)“84”消毒液(主要成分是NaClO)和洁厕剂(主要成分是浓盐酸)不能混用,原因是
您最近一年使用:0次



